17.有一未完成的离子方程式:( )+RO32-+6H+=3R+3H2O,据此判断,R元素的最高价氧化物对应的水化物的化学式为( )
| A. | H2RO3 | B. | H2RO4 | C. | HRO3 | D. | HRO4 |
16.下列结论错误的是( )
| A. | 氢化物的稳定性:HF>HCl>H2S>PH3>SiH4 | |
| B. | 微粒半径:K+>Al3+>S2->Cl- | |
| C. | 酸性:HClO4>H2SO4>H3PO4>H2SiO3 | |
| D. | 金属性:K>Ca>Mg>Be |
15.下列有关化学用语表达不正确的是( )
| A. | Na的原子结构示意图: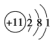 | |
| B. | 含有6个质子和7个中子的碳元素的核素符号:${\;}_{6}^{13}$C | |
| C. | 氮气的电子式::N:::N: | |
| D. | 用电子式表示氧化钠的形成过程: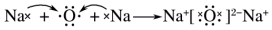 |
14.设NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 22.4L氘(D2)气体,含有中子数为2NA | |
| B. | 1.6gNH2-离子所含电子数为NA | |
| C. | 4g氦气所含分子数为0.5NA | |
| D. | NA个SO3分子在标准状况下的体积为22.4L |
13.下列物质中,既含离子键又含极性共价键的是( )
| A. | NaCl | B. | H2 | C. | H2O | D. | NaOH |
11.在一定的温度下,向一个容积为2L的恒容密闭容器中(事先装入催化剂),充入2molN2和3molH2,3min后测得密闭容器内的压强是起始时的0.9倍.在这段时间内,用H2表示该反应的平均反应速率是( )
| A. | 0.125mol•L-1•min-1 | B. | 0.100 mol•L-1•s-1 | ||
| C. | 0.200 mol•L-1•min-1 | D. | 0.375 mol•L-1•s-1 |
10.下列依据相关实验得出的结论正确的是( )
| A. | 向某溶液中加入稀盐酸,产生的气体通入足量澄清石灰水,石灰水变浑浊,该溶液一定是碳酸盐溶液 | |
| B. | 用洁净铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液 | |
| C. | 向某溶液中滴加KSCN 溶液,溶液不变色,滴加氯水后溶液显红色,该溶液中一定含Fe2+ | |
| D. | 将某气体通入溴水中,溴水颜色褪去,该气体一定是SO2 |
9.表是元素周期表的一部分,X、Y、Z、W均为短周期元素,Z元素原子最外层电子数与电子总数之比为1:3,则下列说法正确的是( )
| X | Y | ||
| Z | W |
| A. | 原子半径大小为W>Z>Y>X | |
| B. | W的最高价含氧酸的酸性最强 | |
| C. | X、Z、Y、W的最髙正价分别为+4、+5、+6、+7 | |
| D. | Z与W形成的所有化合物中.原子最外层电子均达到8e-稳定结构 |
8.一定量的稀盐酸跟过量锌粉反应时,为了加快反应速率又不影响生成H2的总量,可采取的措施是( )
0 162467 162475 162481 162485 162491 162493 162497 162503 162505 162511 162517 162521 162523 162527 162533 162535 162541 162545 162547 162551 162553 162557 162559 162561 162562 162563 162565 162566 162567 162569 162571 162575 162577 162581 162583 162587 162593 162595 162601 162605 162607 162611 162617 162623 162625 162631 162635 162637 162643 162647 162653 162661 203614
| A. | 加少量稀NaOH溶液 | B. | 加入少量NaNO3固体 | ||
| C. | 加入少量NaHSO4固体 | D. | 加入少量CuSO4溶液 |