7.根据表中信息,判断下列叙述中正确的是( )
| 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 | |
| ① | Cl2 | FeBr2 | Cl- | ||
| ② | KClO3 | 浓盐酸 | Cl2 | ||
| ③ | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
| A. | 氧化性强弱的比较:KClO3<Cl2 | |
| B. | 第②组事实可以推测:ClO-、Cl-不能在溶液中大量共存 | |
| C. | 第①组的反应,当Cl2与FeBr2物质的量之比≤1:2时,只有一种元素被氧化 | |
| D. | 第③组反应的离子方程式为:2MnO4-+3H2O2+6H+═2Mn2++4O2↑+6H2O |
5.下列图象错误的是( )
 | 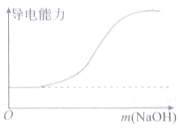 |
| A.向100mL 0.1mol•L-1H2SO4溶液中滴加 0.1mol•L-1Ba(OH)2溶液至过量 | B.向100mL 0.1mol•L-1H2SO4溶液中加入NaOH固体 |
 |  |
| C.向一定浓度的氯化钠溶液中加水 | D.向蒸馏水中通入HCl气体 |
| A. | A | B. | B | C. | C | D. | D |
4.已知标准状况下22.4LCO和CO2混合气体的质量为40g.将此混合气体通入1L1mol/LNaOH溶液充分反应,生成的盐用A、B表示.请将生成盐的化学式及质量填入右表(若只生成一种盐,此表不用填满).
| 生成的盐 | 化学式 | 质量/g |
| A | ||
| B |
2. 将2.32g Na2CO3、NaOH的固体混合物完全溶解于水,制成溶液,然后向该溶液中逐滴加入1mol/L的盐酸,所加盐酸的体积与产生CO2的体积(标准状况)关系如图所示,下列说法中错误的是( )
将2.32g Na2CO3、NaOH的固体混合物完全溶解于水,制成溶液,然后向该溶液中逐滴加入1mol/L的盐酸,所加盐酸的体积与产生CO2的体积(标准状况)关系如图所示,下列说法中错误的是( )
 将2.32g Na2CO3、NaOH的固体混合物完全溶解于水,制成溶液,然后向该溶液中逐滴加入1mol/L的盐酸,所加盐酸的体积与产生CO2的体积(标准状况)关系如图所示,下列说法中错误的是( )
将2.32g Na2CO3、NaOH的固体混合物完全溶解于水,制成溶液,然后向该溶液中逐滴加入1mol/L的盐酸,所加盐酸的体积与产生CO2的体积(标准状况)关系如图所示,下列说法中错误的是( )| A. | OA段发生反应的离子方程式为:H++OH-═H2O CO32-+H+═HCO3- | |
| B. | A点溶液中的溶质为NaCl、NaHCO3 | |
| C. | 混合物中NaOH的质量0.60 g | |
| D. | 当加入35 mL盐酸时,产生CO2的体积为224 mL |
20.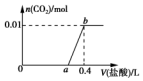 向NaOH和Na2CO3混合溶液中滴加0.1mol•L-1稀盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示.下列判断正确的是 ( )
向NaOH和Na2CO3混合溶液中滴加0.1mol•L-1稀盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示.下列判断正确的是 ( )
 向NaOH和Na2CO3混合溶液中滴加0.1mol•L-1稀盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示.下列判断正确的是 ( )
向NaOH和Na2CO3混合溶液中滴加0.1mol•L-1稀盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示.下列判断正确的是 ( )| A. | 在0~a范围内,只发生NaOH和HCl的反应 | |
| B. | ab段发生反应的离子方程式为:CO32-+2H+═CO2↑+H2O | |
| C. | a=0.3 | |
| D. | 原混合溶液中NaOH与Na2CO3的物质的量之比为1:2 |
19. 向含NaOH、Ba(OH)2、NaAlO2各1mol的混合溶液中,缓慢通入CO2气体,产生沉淀的量与通入CO2的量图象关系如图所示,下列说法错误的是( )
向含NaOH、Ba(OH)2、NaAlO2各1mol的混合溶液中,缓慢通入CO2气体,产生沉淀的量与通入CO2的量图象关系如图所示,下列说法错误的是( )
0 162458 162466 162472 162476 162482 162484 162488 162494 162496 162502 162508 162512 162514 162518 162524 162526 162532 162536 162538 162542 162544 162548 162550 162552 162553 162554 162556 162557 162558 162560 162562 162566 162568 162572 162574 162578 162584 162586 162592 162596 162598 162602 162608 162614 162616 162622 162626 162628 162634 162638 162644 162652 203614
 向含NaOH、Ba(OH)2、NaAlO2各1mol的混合溶液中,缓慢通入CO2气体,产生沉淀的量与通入CO2的量图象关系如图所示,下列说法错误的是( )
向含NaOH、Ba(OH)2、NaAlO2各1mol的混合溶液中,缓慢通入CO2气体,产生沉淀的量与通入CO2的量图象关系如图所示,下列说法错误的是( )| A. | a点对应的溶液中,Na+、Fe3+、SO42-、HCO3-能大量共存 | |
| B. | c、d两点对应的溶液中,沉淀的质量相等 | |
| C. | d点对应的溶液中,c(Na+)>c(HCO3-)>c(OH-)>c(H+) | |
| D. | d点与e点对比,e点溶液的导电性增强 |
 .
. (1)已知在常温常压下:
(1)已知在常温常压下: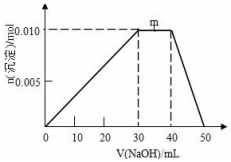 向盛有10mL1mol•L-1 NH4Al(SO4)2溶液的烧杯中滴加1mol•L-1NaOH溶液,沉淀物质的量随NaOH溶液体积变化示意图如下:
向盛有10mL1mol•L-1 NH4Al(SO4)2溶液的烧杯中滴加1mol•L-1NaOH溶液,沉淀物质的量随NaOH溶液体积变化示意图如下: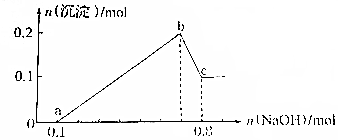 某溶液中可能含有H+、Mg2+、Al3+、Fe3+、Na+等阳离子中的一种或几种,当向该溶液中加入NaOH溶液时,产生沉淀的物质的量与所加NaOH物质的量之间的关系如图所示
某溶液中可能含有H+、Mg2+、Al3+、Fe3+、Na+等阳离子中的一种或几种,当向该溶液中加入NaOH溶液时,产生沉淀的物质的量与所加NaOH物质的量之间的关系如图所示