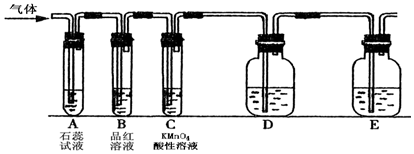
7.设NA为阿伏加德罗常数值.下列有关叙述正确的是( )
| A. | 标准状况下,2.24 LCCl4含有的共价键数为0.4NA | |
| B. | 1 molN2与4 mol H2反应生成的NH3分子数为2NA | |
| C. | 1 molFe溶于过量硝酸,电子转移数为2NA | |
| D. | 34g H2O2和H2S混合物中的氢原子数为2NA |
6.化学在生产、生活中应用广泛,下列说法正确的是( )
| A. | 晶体硅是良好的半导体材料 | |
| B. | 铁、铝合金的熔点高于铁的熔点,硬度小 | |
| C. | 氨常用作制冷剂利用了氨的化学性质 | |
| D. | 漂白粉、明矾都可用于污水的净化,其原理是相同的 |
3.下列说法正确的是( )
0 162456 162464 162470 162474 162480 162482 162486 162492 162494 162500 162506 162510 162512 162516 162522 162524 162530 162534 162536 162540 162542 162546 162548 162550 162551 162552 162554 162555 162556 162558 162560 162564 162566 162570 162572 162576 162582 162584 162590 162594 162596 162600 162606 162612 162614 162620 162624 162626 162632 162636 162642 162650 203614
| A. | 已知2C(s)+O2(g)═2CO(g)△H=-221 kJ•mol-1,则C(碳)的燃烧热为-110.5 kJ•mol-1 | |
| B. | 在101KPa下氢气的燃烧热△H=-285.5 kJ•mol-1,则水分解的热化学方程式为:2H2O(l)=2H2(g)+O2(g)△H=+285.5 kJ•mol-1 | |
| C. | 已知中和热△H=-57.3 kJ•mol-1,若将含0.5 mol H2SO4的稀溶液与含1 mol NaOH的稀溶液混合,放出的热量为57.3 kJ | |
| D. | 含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出热量28.7 kJ,则稀醋酸和稀NaOH溶液反应的热化学方程式为:NaOH(aq)+CH3COOH(aq)═CH3COONa(aq)+H2O(l)△H=-57.4 kJ•mol-1 |
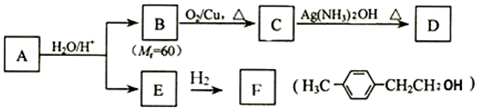
 .
. (其中一种).
(其中一种). )的合成路线.
)的合成路线.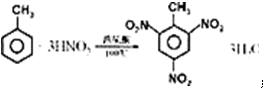 .
.