18.NA表示阿伏加德罗常数的值,下列有关叙述正确的是( )
| A. | 常温下,4.6gNO2和N2O4混合气体中所含原子总数为0.3NA | |
| B. | 4.2g乙烯和丙烯混合气体中含有的极性键数目为0.8NA | |
| C. | 常温下,1L0.5mol/LNH4Cl溶液与2L0.25mol/LNH4Cl溶液所含NH4+的数目相同 | |
| D. | 1mol铁粉在1mol氯气中充分燃烧,转移的电子数为3NA |
17.亚硫酸盐在工业生产中冇广泛的应用,某同学在实验中对亚硫酸盐的制备和性质进行探究.
(1)Cu2SO3•CuSO3•2H2O是一种深红色固体,不溶于水和乙醇,100℃时发生分解,其制备实验装置如图所示.
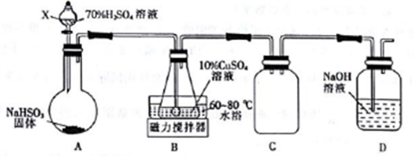
①仪器X的名称是分液漏斗.常温下用装置A制取SO2时,用较浓的硫酸而不用稀硫酸,其原因是SO2易溶于水,用较浓的硫酸有利于SO2的逸出.
②装置C的作用是防止倒吸.
③装置B中发生反应的离子方程式为3Cu2++3SO2+6H2O═Cu2SO3•CuSO3•2H2O↓+8H++SO42-.
④从装置B中获得的固体需先用蒸馏水充分洗涤,再真空干燥,而不直接用烘干的方式得到产品,其原因是防止Cu2SO3•CuSO3•2H2O发生分解和被氧化.
(2)向NaHSO3溶液中加入NaClO溶液时,反应有三种可能的情况:
I.NaHSO3和NaClO恰好反应;II.NaHSO3过量;III.NaClO过量.甲同学欲通过下列实验确定该反应属于哪一种情况,请完成表:
(3)请设计简单实验方案比较室温下NaHSO3浓液中HSO3-的电离平衡常数Ka与水解平衡常数Kb的相对大小:常温下,用pH试纸(或pH计)测定NaHSO3溶液的pH,若PH<7,则Ka>Kb;若pH>7,则Ka<Kb.
(1)Cu2SO3•CuSO3•2H2O是一种深红色固体,不溶于水和乙醇,100℃时发生分解,其制备实验装置如图所示.

①仪器X的名称是分液漏斗.常温下用装置A制取SO2时,用较浓的硫酸而不用稀硫酸,其原因是SO2易溶于水,用较浓的硫酸有利于SO2的逸出.
②装置C的作用是防止倒吸.
③装置B中发生反应的离子方程式为3Cu2++3SO2+6H2O═Cu2SO3•CuSO3•2H2O↓+8H++SO42-.
④从装置B中获得的固体需先用蒸馏水充分洗涤,再真空干燥,而不直接用烘干的方式得到产品,其原因是防止Cu2SO3•CuSO3•2H2O发生分解和被氧化.
(2)向NaHSO3溶液中加入NaClO溶液时,反应有三种可能的情况:
I.NaHSO3和NaClO恰好反应;II.NaHSO3过量;III.NaClO过量.甲同学欲通过下列实验确定该反应属于哪一种情况,请完成表:
| 实验操作 | 预期现象及结论 |
| 取上述反应后的混合溶液于试管 A中,滴加稀硫酸 | 若有气泡产生,则①II(填“I”“II”或“III”,下同)成立,若没有气泡产生,则②I或III成立 |
| 另取上述反应后的混合溶液于试管B中,滴加几滴淀粉KI溶液,充分振荡 | ③溶液变为蓝色,则III成立 |
16.下列实验操作、现象和解释或结论均正确的是( )
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 将铝片分別加入浓HNO3和NaOH浓溶液中 | NaOH浓溶液中的铝片溶解 | 铝不与浓HNO3反应 |
| B | 向紫色石蕊试液中通入足量二氧化硫 | 溶液由紫色变为红色 | 二氧化硫与水反应有酸性物质生成 |
| C | 将分别蘸有浓氨水和浓硝酸的两根玻璃棒相互靠近 | 有白烟生成 | 浓硝酸具有强氧化性 |
| D | 向待测液中加入盐酸酸化的硝酸钡溶液 | 有白色沉淀生成 | 待测液中含有SO42- |
| A. | A | B. | B | C. | C | D. | D |
15.设NA为阿伏加德罗常数的数值,下列说法错误的是( )
| A. | 1 LpH=l Ba(OH)2溶液中所含OH-的数目为0.2NA | |
| B. | 28g聚乙烯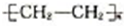 中含有的碳原子数为2NA 中含有的碳原子数为2NA | |
| C. | 1 mol CH3COONa和少量CH3COOH形成的中性溶液中,CH3COO-的数目为NA | |
| D. | 1 mol Na与O2完全反应生成Na2O和Na2O2的混合物,转移的电子总数为NA |
14.下列关于有机物说法正确的是( )
| A. | C7H8与C6H6互为同系物 | |
| B. | 由乙酸与乙醇制备乙酸乙酯的反位属于加成反位 | |
| C. | C3H6Br2有4种同分异构体 | |
| D. | 油脂在人体内最终分解为甘油和高级脂肪酸 |
13.化学与生产、生活、社会发展等息息相关.下列说法正确的是( )
| A. | 为补充土壤中的钾元素,可在田间焚烧秸秆 | |
| B. | 煤经过气化、液化等物理变化可转变为清洁燃料 | |
| C. | 聚乙烯、聚氯乙烯均可作包装材料,且不会造成环境污染 | |
| D. | 在食品包装时放入盛有铁粉的透气小袋可防止食品氧化变质 |
12.短周期主族元素X、Y、Z、W的原子序数依次增大,X、Y的原子序数之和等于Z的原子序数;Y、Z为同周期相邻元素,X、W、Y分别排列在三个连续的奇数族.下列说法正确的是( )
| A. | 简单离子半径:W>Y>Z | |
| B. | 最高价氧化物对应水化物的酸性:Y<Z | |
| C. | 工业上制备W单质的方法为热还原法 | |
| D. | X分别与Y、Z形成的简单化合物所含化学键类型相同 |
10.下列离子组能大量共存且加入相应试剂后发生反应的离子方程式正确的是( )
| 离子组 | 加入试剂 | 加入试剂后发生反应 | |
| A | K+、Fe2+、I- | 少量的酸性KMnO4溶液 | 5Fe2++MnO4-+8H+═5Fe3++Mn2++4H2O |
| B | Fe3+、I-、SO42- | NaOH溶液 | Fe3++3OH-═Fe(OH)3↓ |
| C | Ba2+、HCO3-、Cl- | NaOH溶液 | HCO3-+OH-═CO32-+H2O |
| D | Al3+、Cl-、NO3- | 过量浓氨水 | Al3++3NH3•H2O═Al(OH)3↓+3NH4+ |
| A. | A | B. | B | C. | C | D. | D |
9.设NA为阿伏加德罗常数的值,下列说法正确的是( )
0 162445 162453 162459 162463 162469 162471 162475 162481 162483 162489 162495 162499 162501 162505 162511 162513 162519 162523 162525 162529 162531 162535 162537 162539 162540 162541 162543 162544 162545 162547 162549 162553 162555 162559 162561 162565 162571 162573 162579 162583 162585 162589 162595 162601 162603 162609 162613 162615 162621 162625 162631 162639 203614
| A. | 100g 98%的浓硫酸中含有的氢原子数目为2NA | |
| B. | 常温下,2.7gAI与足量浓度为18mo1/L的浓硫酸反应时,转移的电子数为0.3NA | |
| C. | 标准状况下,22.4L的CCI4含有的CCl4分子数大于NA | |
| D. | 1 mol笨完全转化为环己烷,参与反应的碳碳双键数为3NA |