7.已知:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H
现在体积为1L的密闭容器中,充入CO2和H2.实验测得反应体系中物质的物质的量与时间关系如下表,
回答下列问题:
(1)表格中的n1=0.75mol
(2)0-5min内 v (H2)=0.3mol•L-1•min-1
(3)该条件下CO2的平衡转化率为75%.
现在体积为1L的密闭容器中,充入CO2和H2.实验测得反应体系中物质的物质的量与时间关系如下表,
| n(CO2) | n(H2) | n(CH3OH(g) | n(H2O(g) | |
| 0 | 1.00mol | 3.25mol | 0.00 | 0.00 |
| 5min | 0.50mol | 0.50mol | ||
| 10min | 0.25mol | 0.75mol | ||
| 15min | 0.25mol | n1 |
(1)表格中的n1=0.75mol
(2)0-5min内 v (H2)=0.3mol•L-1•min-1
(3)该条件下CO2的平衡转化率为75%.
6.向恒温恒容的密闭容器中充入amolX和bmolY,发生反应X(g)+3Y(g)?2Z(g)达到平衡时,测得X和Y的转化率分别为25%和37.5%.则a:b为( )
| A. | 1:3 | B. | 3:1 | C. | 3:2 | D. | 1:2 |
5.已知:H-Cl和H-I键能分别为431KJ/mol和297KJ/mol,下列性质比较正确且可用键能数据说明原因的是( )
| A. | 稳定性:HI>HCl | B. | 熔、沸点:HI>HCl | ||
| C. | 同浓度的HI和HCl的酸性:HI>HCl | D. | 还原性:HI>HCl |
4.下列各选项所述的两个量,前者一定大于后者的是( )
| A. | Ag+、Cu2+与NH3形成配合物时的配位数 | |
| B. | NaCl的晶格能与MgO的晶格能 | |
| C. | H-F键的极性与H-O键的极性 | |
| D. | BF3的键角CS2的键角 |
3.有A、B、C三种主族元素,已知A元素原子的价电子构型为nsn,B元素原子的M层上有两个未成对电子,C元素原子L层的p轨道上有一对成对电子,由这三种元素组成的化合物的化学式不可能是( )
| A. | A3BC4 | B. | A2BC4 | C. | A2BC3 | D. | A4BC4 |
1.短周期A、B、C、D、E五种主族元素,原子序数依次增大,B、C、E最外层电子数之和为11,A原子最外层电子数是次外层电子数的2倍,C是同周期中原子半径最大的元素,工业上一般通过电解氧化物的方法获得D的单质,E单质是制备太阳能电池的重要材料.下列说法正确的是( )
| A. | 相同质量的C和D单质分別与足量稀盐酸反应时,后者生成的氢气多 | |
| B. | C与D的最高价氧化物对应的水化物的碱性相比,后者更强 | |
| C. | 不用电解氯化物的方法制备单质D是由于其氯化物的熔点高 | |
| D. | 简单离子半径:B<C |
20. 元素R、X、T、Z、Q在元素周期表中的相对位置如表所示,其中R单质在暗处与H2剧烈化合并发生爆炸,则下列判断正确的是( )
元素R、X、T、Z、Q在元素周期表中的相对位置如表所示,其中R单质在暗处与H2剧烈化合并发生爆炸,则下列判断正确的是( )
 元素R、X、T、Z、Q在元素周期表中的相对位置如表所示,其中R单质在暗处与H2剧烈化合并发生爆炸,则下列判断正确的是( )
元素R、X、T、Z、Q在元素周期表中的相对位置如表所示,其中R单质在暗处与H2剧烈化合并发生爆炸,则下列判断正确的是( )| A. | 非金属性:X<T<Z | B. | 第一电离能:X<T<Z | ||
| C. | 气态氢化物的还原性:X<T<R | D. | 最高价氧化物的水化物酸性:Q<T<R |
19.将过量的CO2分别通入
①CaCl2溶液
②Na2SiO3溶液
③Ca(ClO)2溶液
④饱和Na2CO3溶液
⑤NaAlO2 最终有沉淀析出的是( )
0 162442 162450 162456 162460 162466 162468 162472 162478 162480 162486 162492 162496 162498 162502 162508 162510 162516 162520 162522 162526 162528 162532 162534 162536 162537 162538 162540 162541 162542 162544 162546 162550 162552 162556 162558 162562 162568 162570 162576 162580 162582 162586 162592 162598 162600 162606 162610 162612 162618 162622 162628 162636 203614
①CaCl2溶液
②Na2SiO3溶液
③Ca(ClO)2溶液
④饱和Na2CO3溶液
⑤NaAlO2 最终有沉淀析出的是( )
| A. | ②④⑤ | B. | ①②③④ | C. | ②③④⑤ | D. | ②③④ |
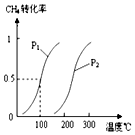 在容积为100L的密闭容器中,加入1.0molCH4和2.0molH2O(g).一定条件下发生反应:CH4(g)+H2O(g)?CO(g)+3H2(g)△H
在容积为100L的密闭容器中,加入1.0molCH4和2.0molH2O(g).一定条件下发生反应:CH4(g)+H2O(g)?CO(g)+3H2(g)△H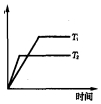 研究表明,在CuZnO2催化剂存在下,CO2和H2可发生两个平行反应,分别生成CH3OH和CO,反应的热化学方程式如下:
研究表明,在CuZnO2催化剂存在下,CO2和H2可发生两个平行反应,分别生成CH3OH和CO,反应的热化学方程式如下: