7.下列关于离子共存或离子检验的说法正确的是( )
| A. | 某无色溶液中可能大量存在H+、Cl-、MnO4-、Al3+ | |
| B. | pH=2的溶液中可能大量存在Na+、NH4+、SiO32-、CO32- | |
| C. | 含有大量AlO2-的溶液中:K+、HCO3-、Br-、Na+可共存 | |
| D. | 在某钠盐溶液中含有等物质的量的Cl-、I-、AlO2-、CO32-、NO3-、SiO32-中若干种,当加入过量的盐酸产生气泡,溶液颜色变深,最终溶液中无沉淀,阴离子种数减少3种,则原溶液中一定有CO32- |
5.要配制物质的量浓度约为2mol/L NaOH溶液100mL,下面的操作中,正确的是( )
| A. | 称取8 g NaOH固体,放入250 mL烧杯中,用100 mL量筒量取100 mL蒸馏水,加入烧杯中,同时不断搅拌至固体溶解 | |
| B. | 称取8 g NaOH固体,放入100 mL量筒中,边搅拌,边慢慢加入蒸馏水,待固体完全溶解后用蒸馏水稀释至100 mL | |
| C. | 称取8 g NaOH固体,放入100 mL容量瓶中,加入适量蒸馏水,振荡容量瓶使固体溶解,再加入水到刻度,盖好瓶塞,反复摇匀 | |
| D. | 用100 mL量筒量取40 mL 5 mol/L NaOH溶液,倒入250 mL烧杯中,再用同一量筒量取60 mL蒸馏水,不断搅拌下,慢慢倒入烧杯中 |
4.下列实验方案设计中,能达到实验目的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 检验FeCl3溶液中是否存在FeCl2 | 向溶液中滴加KSCN溶液后再滴加氯水 |
| B | 证明H2CO3酸性比H2SiO3强 | Na2CO3和SiO2在高温下熔融反应 |
| C | 除去Cu粉中混有的CuO | 向混合物中滴加适量稀硫酸并过滤 |
| D | 检验未知溶液一定含有CO32- | 加入稀盐酸有无色无味的气体生成 |
| A. | A | B. | B | C. | C | D. | D |
3.Q、W、X、Y、Z是原子序数依次增大的短周期元素,X、Y是金属元素,X的焰色反应呈黄色.五种元素核电荷数之和为54,W、Z最外层电子数相同,Z的核电荷数是W的2倍.工业上一般通过电解氧化物的方法获得Y的单质.则下列说法不正确的是( )
| A. | 原子半径:X>Y>Z>Q>W | |
| B. | 最高价氧化物对应的水化物的酸性:Z<Q | |
| C. | Q和W可形成原子个数比为1:1和2:1的化合物 | |
| D. | X、Y和W三种元素形成的化合物的水溶液呈碱性 |
2.用NA表示阿伏加德罗常数的值.下列判断错误的是( )
| A. | NA个H+的质量为1 g | |
| B. | 2 L 0.5 mol/L Na2SO4溶液中含NA个Na+ | |
| C. | 32 g O2中含有2NA个氧原子 | |
| D. | 标准状况下,1 mol H2O中含有NA个分子 |
1.工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁[Fe(OH)SO4]的工艺流程如下:
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH如下表: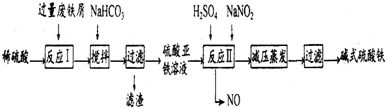
回答下列问题:
(1)反应I溶液中存在的金属阳离子有Fe2+、Al3+.
(2)加入NaHCO3的目的是调节pH,使溶液中的Al3+(填“Fe3+”、“Fe2+”或“A13+”)沉淀.该工艺流程中“搅拌”的作用是加快反应速率.
(3)反应II的离子方程式为2H++Fe2++NO2-=Fe3++NO↑+H2O.在实际生产中,反应II常同时通入O2以减少NaNO2的用量,O2与NaNO2在反应中均作为氧化剂.若参与反应的O2有11.2L(标准状况),则相当于节约NaNO2物质的量为2mol.
(4)碱式硫酸铁溶于水后产生的[Fe(OH)]2+离子,可部分水解生成${[{F{e_2}{{({OH})}_4}}]^{2+}}$聚合离子.该水解反应的离子方程式为2Fe(OH)2++2H2O?Fe2(OH)42++2H+.
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH如下表:

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
(1)反应I溶液中存在的金属阳离子有Fe2+、Al3+.
(2)加入NaHCO3的目的是调节pH,使溶液中的Al3+(填“Fe3+”、“Fe2+”或“A13+”)沉淀.该工艺流程中“搅拌”的作用是加快反应速率.
(3)反应II的离子方程式为2H++Fe2++NO2-=Fe3++NO↑+H2O.在实际生产中,反应II常同时通入O2以减少NaNO2的用量,O2与NaNO2在反应中均作为氧化剂.若参与反应的O2有11.2L(标准状况),则相当于节约NaNO2物质的量为2mol.
(4)碱式硫酸铁溶于水后产生的[Fe(OH)]2+离子,可部分水解生成${[{F{e_2}{{({OH})}_4}}]^{2+}}$聚合离子.该水解反应的离子方程式为2Fe(OH)2++2H2O?Fe2(OH)42++2H+.
11.下列实验操作与预期实验目的或所得实验结论一致的是( )
| 实验操作 | 实验目的或结论 | |
| A | 蘸有浓硝酸的玻璃棒靠近浓氨水时冒白烟 | NH3具有还原性 |
| B | 将一块Na放入乙醇溶液中,有气泡产生 | Na能置换乙醇中的氢 |
| C | 可将58.5gNaCl加入盛有500mL水的烧杯中,搅拌、溶解 | 粗略配置浓度为2mol•L-1的NaCl溶液 |
| D | 向氯仿中加入NaOH溶液,加热充分反应后,再加入AgNO3 | 验证氯仿中含有的氯元素 |
| A. | A | B. | B | C. | C | D. | D |
10.除去下列括号内杂质的试剂和方法正确的是( )
0 162436 162444 162450 162454 162460 162462 162466 162472 162474 162480 162486 162490 162492 162496 162502 162504 162510 162514 162516 162520 162522 162526 162528 162530 162531 162532 162534 162535 162536 162538 162540 162544 162546 162550 162552 162556 162562 162564 162570 162574 162576 162580 162586 162592 162594 162600 162604 162606 162612 162616 162622 162630 203614
| A. | Fe3+(Al3+),加过量的氨水,过滤 | |
| B. | KCl溶液(BaCl2),加入足量K2SO4溶液,过滤 | |
| C. | CO2(SO2),饱和碳酸钠溶液,浓硫酸,洗气 | |
| D. | MgCl2溶液(Fe3+):加MgO固体,过滤 |