11.下列说法正确的是( )
| A. | 日常生活中常用75%的乙醇溶液来杀菌消毒 | |
| B. | 可用淀粉溶液来检测食盐中是否含碘 | |
| C. | 发酵粉中主要含有碳酸钠,能使焙制出的糕点疏松多孔 | |
| D. | 医院中常用碳酸钡作为内脏造影剂 |
10.下述实验设计或操作正确的是( )
| 选项 | 实验目的 | 实验设计 |
| A | 除去铝箔上少量的氧化膜 | 将铝箔放入 NaOH 溶液中洗涤 |
| B | 排水法收集 KMnO4分解产生的 O2 | 先熄灭酒精灯,后移出导管 |
| C | 检验溶液中是否含有 Fe2+ | 向溶液中滴入氯水后,再滴加 KSCN 溶液 |
| D | 证明 H2SO4酸性比 H2CO3 强 | 把稀 H2SO4 滴入 NaHCO3 溶液 |
| A. | A | B. | B | C. | C | D. | D |
9.下列说法不正确的是( )
| A. | 石英是制造光导纤维的原料,也是常用的半导体材料 | |
| B. | 氧化铝是冶炼金属铝的原料,也是较好的耐火材料 | |
| C. | 天然氨基酸能溶于强碱或强酸溶液,是两性化合物 | |
| D. | 船舶外壳装上锌块,是牺牲阳极的阴极保护法进行防腐 |
8.某化学兴趣小组要完成中和热的测定.回答下列问题:
实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、0.5mol•L-1盐酸、0.55mol•L-1NaOH溶液,实验尚缺少的玻璃用品是量筒、温度计.
(2)已知:反应后溶液的比热容c为4.18J•℃-1•g-1,0.5mol•L-1盐酸和0.55mol•L-1NaOH溶液的密度均为1g•c
m-3.实验时记录的实验数据如表:
①盐酸和氢氧化钠反应的中和热△H1=-56.8kJ•mol-1(保留两位小数)
②已知:CH3COOH(aq)?CH3COO-(aq)+H+(aq)△H2>0,
CH3COOH(aq)+OH-(aq)=CH3COO-(aq)+H20(l)△H3 则△H3>△H1(填“>”、“<”、“=”)
实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、0.5mol•L-1盐酸、0.55mol•L-1NaOH溶液,实验尚缺少的玻璃用品是量筒、温度计.
(2)已知:反应后溶液的比热容c为4.18J•℃-1•g-1,0.5mol•L-1盐酸和0.55mol•L-1NaOH溶液的密度均为1g•c
m-3.实验时记录的实验数据如表:
| 实验 次数 | 反应物及用量 | 溶 液 温 度 | ||
| t1 | t2 | |||
| 1 | 50mL0.55mol•L-1NaOH溶液 | 50mL.0.5mol•L-1HCl溶液 | 20℃ | 23.3℃ |
| 2 | 50mL0.55mol•L-1NaOH溶液 | 50mL.0.5mol•L-1HCl溶液 | 20℃ | 23.5℃ |
②已知:CH3COOH(aq)?CH3COO-(aq)+H+(aq)△H2>0,
CH3COOH(aq)+OH-(aq)=CH3COO-(aq)+H20(l)△H3 则△H3>△H1(填“>”、“<”、“=”)
7.在10L定容密闭容器中,A、B、C三种气态物质构成了可逆反应的体系,当在某一温度时,A、B、C物质的量与时间的关系如图1,C的百分含量与温度的关系如图2.下列分析不正确的是( )
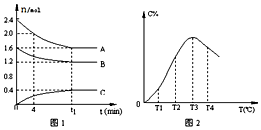

| A. | t1时刻前,混合气体的密度减小,t1时刻后,混合气体的密度不变 | |
| B. | 该反应的平衡常数表达式K=$\frac{c(C)}{{c}^{2}(A)•c(B)}$ | |
| C. | 由T1向T2变化时,V正>V逆 | |
| D. | 此反应的正反应为放热反应 |
6.下列对分子结构及其性质的解释中,不正确的是( )
| A. | 碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释 | |
| B. | 乳酸[CH3CH(OH)COOH]属于手性分子,因分子中存在手性碳原子 | |
| C. | 配合物中一定含有过渡金属原子或离子,因为过渡金属原子或离子存在空轨道 | |
| D. | 酸性H3PO4>HClO,是因为H3PO4分子非羟基氧原子数目比HClO多 |
5.下列微粒的立体结构的名称正确的是( )
| A. | SO2 直线形 | B. | NH4+正四面体形 | C. | CS2 平面三角形 | D. | BF3 三角锥形 |
4.PH3 是一种无色剧毒气体.下列判断错误的是( )
| A. | PH3 分子是非极性分子 | |
| B. | PH3分子中有一对电子孤对 | |
| C. | PH3 分子VSEPR模型的名称是四面体 | |
| D. | PH3 分子稳定性低于 NH3 分子 |
3.设NA为阿伏伽德罗常数的值,下列叙述不正确的是( )
| A. | 含16g氧原子的二氧化硅晶体中含有的δ键数目为2NA | |
| B. | 1mol甲基(-CH3)所含电子数为9NA | |
| C. | 12克石墨中含有的共价键数目为1.5NA | |
| D. | 2molSO2和1molO2在一定条件下反应所得混合气体分子数等于2 NA |
2.下列有关叙述或化学用语表示正确的是( )
0 162409 162417 162423 162427 162433 162435 162439 162445 162447 162453 162459 162463 162465 162469 162475 162477 162483 162487 162489 162493 162495 162499 162501 162503 162504 162505 162507 162508 162509 162511 162513 162517 162519 162523 162525 162529 162535 162537 162543 162547 162549 162553 162559 162565 162567 162573 162577 162579 162585 162589 162595 162603 203614
| A. | S2-的结构示意图: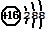 | |
| B. | 过氧化氢的电子式: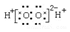 | |
| C. | Ge原子的简化电子排布式:[Ar]4s24p2 | |
| D. | 氯化钠的分子式:NaCl |