11.利用如图所示装置进行下列实验,其中丙中实验现象描述正确的是( )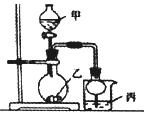

| 实验 | 试剂甲 | 试剂乙 | 试剂丙 | 丙中的现象 |
| A | 浓硫酸 | Na2SO3 | 紫色石蕊试液 | 溶液先变红红褪色 |
| B | 浓盐酸 | KMnO4 | 淀粉-Kl溶液 | 溶液变蓝 |
| C | 稀盐酸 | CaCO3 | BaCl2溶液 | 有白色沉淀生成 |
| D | 浓氨水 | CaO | AlCl3溶液 | 先生成白色沉淀然后沉淀溶解 |
| A. | A | B. | B | C. | C | D. | D |
10.下列离子或分子组中,在相应的环境中一定能大量共存的是( )
| 选项 | 环境要求 | 离子或分子 |
| A | Al2(SO4)3溶液中 | K+,AlO${\;}_{2}^{-}$,Cl-,NO${\;}_{3}^{-}$ |
| B | 滴加石蕊试液显蓝色的溶液中 | Na+,K-,SO${\;}_{3}^{2-}$,S2- |
| C | 水电离产生的c(OH-)=10-12mol•L-1的溶液 | ClO-,CO${\;}_{3}^{2-}$,NH${\;}_{4}^{+}$,K- |
| D | 氯气中 | O2,NH3,CO2,HCl |
| A. | A | B. | B | C. | C | D. | D |
9.下列关于有机化合物的说法正确的是( )
| A. | 乙烯和苯都能使溴水褪色,褪色的原因相同 | |
| B. | 化合物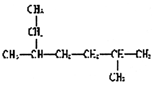 的名称为2-甲基-5-乙基己烷 的名称为2-甲基-5-乙基己烷 | |
| C. | 纤维素和油脂都是能发生水解反应的高分子化合物 | |
| D. | 甲烷、苯、乙醇、乙酸和酯类都可以发生取代反应 |
8.下列有关试剂保持或实验操作的叙述正确的是( )
| A. | 浓硝酸保存在棕色橡胶塞的试剂瓶中 | |
| B. | 用溴的四氯化碳溶液除去甲烷中的乙烯杂质 | |
| C. | 酸碱中和滴定实验中,锥形瓶用蒸馏水洗涤后,不需要干燥 | |
| D. | 配制NH4Fe(SO4)2标准溶液时,加入一定量HCl以防水解 |
7.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 136g熔融的KHSO4中含有2NA个阳离子 | |
| B. | 40gH218O与40gD2O所含的中子数均为20NA | |
| C. | 1molFe分别与足量的稀硫酸和稀硝酸反应转移电子数均为2NA | |
| D. | 标准状况下,22.4LNO和11.2LO2混合后气体的分子总数为NA |
6.下列关于NO的说法正确的是( )
| A. | 为红棕色气体 | B. | 只有氧化性 | ||
| C. | 是汽车尾气的有害成分之一 | D. | 易溶于水生成硝酸 |
4.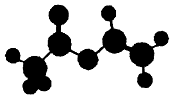 法国、美国、荷兰的三位科学家因研宄“分子机器的设计与合成”获得2016年诺贝尔化学奖.轮烷是一种分子机器的“轮子”,轮烷的一种合成原料由C、H、O三种元素组成,其球棍模型如图所示,下列说法正确的是( )
法国、美国、荷兰的三位科学家因研宄“分子机器的设计与合成”获得2016年诺贝尔化学奖.轮烷是一种分子机器的“轮子”,轮烷的一种合成原料由C、H、O三种元素组成,其球棍模型如图所示,下列说法正确的是( )
0 162407 162415 162421 162425 162431 162433 162437 162443 162445 162451 162457 162461 162463 162467 162473 162475 162481 162485 162487 162491 162493 162497 162499 162501 162502 162503 162505 162506 162507 162509 162511 162515 162517 162521 162523 162527 162533 162535 162541 162545 162547 162551 162557 162563 162565 162571 162575 162577 162583 162587 162593 162601 203614
 法国、美国、荷兰的三位科学家因研宄“分子机器的设计与合成”获得2016年诺贝尔化学奖.轮烷是一种分子机器的“轮子”,轮烷的一种合成原料由C、H、O三种元素组成,其球棍模型如图所示,下列说法正确的是( )
法国、美国、荷兰的三位科学家因研宄“分子机器的设计与合成”获得2016年诺贝尔化学奖.轮烷是一种分子机器的“轮子”,轮烷的一种合成原料由C、H、O三种元素组成,其球棍模型如图所示,下列说法正确的是( )| A. | 该化合物的名称为乙酸乙酯 | |
| B. | 该化合物与Br2的四氯化碳溶液不反应 | |
| C. | 该化合物既能发生水解反应,又能发生氧化反应 | |
| D. | 该化合物的同分异构体中,能与NaHCO3反应放出CO2的只有2种 |
