1.有关电解质溶液下列说法正确的是( )
| A. | 常温下同浓度的强酸、强碱等体积混合后由水电离出的c(H+)=10-7mol•L-1 | |
| B. | 将AlCl3溶液、Na2SO3溶液蒸干并灼烧可以得到Al2O3、Na2SO3 | |
| C. | 常温下0.1mol•L-1的Na2A溶液的pH=10,则该溶液中由水电离的c(OH-)=10-10mol•L-1 | |
| D. | 常温下pH=2的盐酸和pH=12的氨水等体积混合后c(Cl-)+c(H+)<c(NH4+)+c(OH-) |
20.有关电解质溶液的叙述正确的是( )
| A. | 向0.2mol•L-1CH3COOH溶液中加入等体积0.1mol•L-1NaOH溶液,测得溶液中c(CH3COO-)>c(Na+),则水的电离程度比纯水的大 | |
| B. | 向0.1 mol•L-1氨水中滴加0.1 mol•L-1盐酸,刚好完全中和时溶液pH=a,则由水电离产生的c(OH-)=10a-14mol•L-1 | |
| C. | 将0.1 mol•L-1Na2CO3和0.1 mol•L-1NaHCO3溶液等体积混合,所得溶液有:c(CO32-)+2c(OH-)=2c(H+)+c(HCO3-)+3c(H2CO3) | |
| D. | 对于难溶电解质:相同温度时,Ksp大的饱和溶液的物质的量浓度一定比Ksp小的饱和溶液物质的量浓度大 |
19.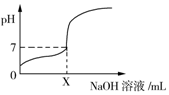 常温下,用0.1mol/L的NaOH溶液滴定20mL同浓度的一元弱酸HA,滴定过程中溶液pH随NaOH溶液体积变化曲线如图所示(忽略中和热效应),下列说法正确的是( )
常温下,用0.1mol/L的NaOH溶液滴定20mL同浓度的一元弱酸HA,滴定过程中溶液pH随NaOH溶液体积变化曲线如图所示(忽略中和热效应),下列说法正确的是( )
 常温下,用0.1mol/L的NaOH溶液滴定20mL同浓度的一元弱酸HA,滴定过程中溶液pH随NaOH溶液体积变化曲线如图所示(忽略中和热效应),下列说法正确的是( )
常温下,用0.1mol/L的NaOH溶液滴定20mL同浓度的一元弱酸HA,滴定过程中溶液pH随NaOH溶液体积变化曲线如图所示(忽略中和热效应),下列说法正确的是( )| A. | X=20 | |
| B. | HA溶液加水稀释后,溶液中$\frac{c(HA)}{{c({A^-})}}$的值减小 | |
| C. | 0.1 mol/L的NaOH溶液中,由水电离出的c(OH-)=0.1 mol/L | |
| D. | 加入NaOH溶液体积为X mL时,溶液中c(A-)=0.05 mol/L |
17.已知:2CO(g)+O2(g)=2CO2(g)△H=-566KJ/mol
Na2O2(s)+CO2(g)=Na2CO3(s)+$\frac{1}{2}$O2(g)△H=-266KJ/mol
根据以上热化学方程式判断,下列说法正确的是( )
Na2O2(s)+CO2(g)=Na2CO3(s)+$\frac{1}{2}$O2(g)△H=-266KJ/mol
根据以上热化学方程式判断,下列说法正确的是( )
| A. | 2Na2O2(s)+2CO2( s)=2Na2CO3(s)+O2(g)△H>-452 kJ/mol | |
| B. | CO的燃烧热为283 kJ | |
| C. | 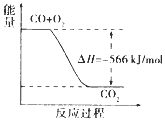 如图可表示由CO生成CO2的反应过程和能量关系 | |
| D. | CO(g)与Na2O2(s)反应放出509kJ热量时,电子转移数为6.02×l023 |
12.常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如表:
下列对混合后溶液的有关说法重,不正确的是( )
0 162406 162414 162420 162424 162430 162432 162436 162442 162444 162450 162456 162460 162462 162466 162472 162474 162480 162484 162486 162490 162492 162496 162498 162500 162501 162502 162504 162505 162506 162508 162510 162514 162516 162520 162522 162526 162532 162534 162540 162544 162546 162550 162556 162562 162564 162570 162574 162576 162582 162586 162592 162600 203614
| 实验编号 | c(HA)/mol•L-1) | c(NaOH)/mol•L-1 | 混合后溶液的pH |
| 甲 | 0.2 | 0.2 | pH=a |
| 乙 | b | 0.2 | pH=7 |
| 丙 | 0.2 | 0.1 | pH<7 |
| 丁 | 0.1 | 0.1 | pH=c |
| A. | 甲中:若a=7,则HA是强酸 | |
| B. | 乙中:若b≠0.2,则c(A-)=C(Na+) | |
| C. | 丙中:若HA是弱酸,则$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$<1 | |
| D. | 丁中:若 c=9,则c(OH-)-c(HA)=10-9mol/L |
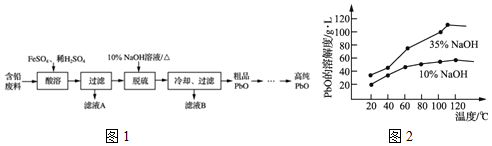
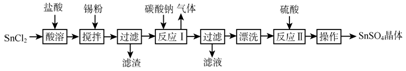
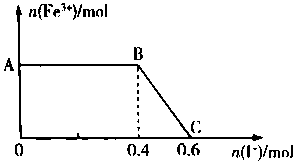 将FeC12溶液与过量氯水(视溶质为Cl2)混合,发生反应:Cl2+ZFeCl2=2FeCl3,得到溶液X.向溶液X中加入KI溶液,混合溶液中Fe3+的物质的量随加入KI的物质的量的变化关系如图所示.已知Cl2、FeCl3均可将I-氧化为I2,其自身分别被还原为Cl-、Fe2+.回答下列问题:
将FeC12溶液与过量氯水(视溶质为Cl2)混合,发生反应:Cl2+ZFeCl2=2FeCl3,得到溶液X.向溶液X中加入KI溶液,混合溶液中Fe3+的物质的量随加入KI的物质的量的变化关系如图所示.已知Cl2、FeCl3均可将I-氧化为I2,其自身分别被还原为Cl-、Fe2+.回答下列问题: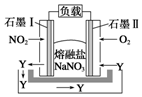 燃煤废气中的氮氧化物(NOx)、二氧化碳等气体,常用下列方法处理,以实现节能减排、废物利用等.
燃煤废气中的氮氧化物(NOx)、二氧化碳等气体,常用下列方法处理,以实现节能减排、废物利用等.