1.根据要求回答下列问题
(1)T0C时,向一容积为2升的密闭容器中充入2molA、0.6molC和一定量的B三种气体,一定条件下发生反应.其相关信息如下:图1中t0~t1阶段c(B)未画出;图2中t2、t3、t4改变的条件是温度、压强、催化剂中的一种
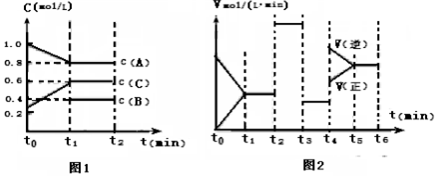
①B的起始物质的量为1mol;t2时刻改变的条件是加催化剂
②图2中各阶段平衡时对应的平衡常数如表所示:
K2> K4(填“>或<或.=”);其理由是t2-t4 平衡未移动,从图象知K4是温度升高平衡逆向移动后的常数,所以变小
③T0C时,该反应的平衡常数是0.84(保留两位小数);维持温度不变,在t1时刻再向该容器中加入1molA,0.5molB,0.3molC,重新达平衡后α(A)=20%
(2)硅是重要的半导体材料.工业上由粗制纯硅的过程如下:
Si(粗)$→_{460℃}^{Cl_{2}}$SiCl4$\stackrel{蒸馏}{→}$SiCl4(纯)$→_{1100℃}^{H_{2}}$Si(纯)
实验测得上述由SiCl4制纯硅的反应中,测得每生成1.12kg纯硅(Si的相对原子质量为28)需吸收aKJ热量,则该反应的热化学方程式SiCl4(g)+2H2(g)=Si(s)+4HCl(g)△=+Q/40 KJ/mol.
(1)T0C时,向一容积为2升的密闭容器中充入2molA、0.6molC和一定量的B三种气体,一定条件下发生反应.其相关信息如下:图1中t0~t1阶段c(B)未画出;图2中t2、t3、t4改变的条件是温度、压强、催化剂中的一种

①B的起始物质的量为1mol;t2时刻改变的条件是加催化剂
②图2中各阶段平衡时对应的平衡常数如表所示:
| 时间段 | t1~t2 | t2~t3 | t3~t4 | t5~t6 |
| 平衡常数 | K1 | K2 | K3 | K4 |
③T0C时,该反应的平衡常数是0.84(保留两位小数);维持温度不变,在t1时刻再向该容器中加入1molA,0.5molB,0.3molC,重新达平衡后α(A)=20%
(2)硅是重要的半导体材料.工业上由粗制纯硅的过程如下:
Si(粗)$→_{460℃}^{Cl_{2}}$SiCl4$\stackrel{蒸馏}{→}$SiCl4(纯)$→_{1100℃}^{H_{2}}$Si(纯)
实验测得上述由SiCl4制纯硅的反应中,测得每生成1.12kg纯硅(Si的相对原子质量为28)需吸收aKJ热量,则该反应的热化学方程式SiCl4(g)+2H2(g)=Si(s)+4HCl(g)△=+Q/40 KJ/mol.
20..某校化学兴趣小组探究SO2的一些性质.
[探究一]:SO2能否被BaCl2溶液吸收.
甲.乙两同学分别设计如图装置甲和装置乙进行探究
甲、乙两同学实验时观察到各仪器中的现象如下:
回答下列问题:
(1)甲同学经过后续实验确证了B中白色沉淀是BaSO4.甲同学的后续实验操作是打开B试管的胶塞,向其中滴加稀盐酸,若白色沉淀不消失,证明白色沉淀是BaSO4

(2)乙同学分析装置甲中产生BaSO4的可能原因有:
①A中产生的白雾是硫酸的酸雾,进入B中与BaCl2溶液反应生成BaSO4沉淀.
②2SO2+O2+2H2O+2Ba2+=2BaSO4+4H+(用离子方程式表示).
(3)装置乙中B中所盛试剂是饱和NaHSO3溶液;乙同学在滴加浓硫酸之前的操作是打开弹簧夹向A中通往一段时间的N2,然后关闭弹簧夹
(4)通过上述实验,得出的结论是SO2不能被BaCl2溶液吸收
[探究二]:SO2与FeCl3溶液的反应
查阅资料:①Fe(HSO3)2+离子为红棕色,它可以将Fe3+还原为Fe2+;②生成Fe(HSO3)2+离子的反应为可逆反应.实验步骤为:
回答下列问题:
(5)当SO2通入到FeCl3(未用盐酸酸化)溶液至饱和时,同学们观察到的现象是溶液由棕黄色变成红棕色,没有观察到丁达尔现象.将混合液放置12小时,溶液才变成浅绿色.
则溶液由棕黄色变成红棕色的原因是二氧化硫溶于水SO2+H2O?HSO3-+H+,Fe3++HSO3-?Fe(HSO3)2+;写出溶液由红棕色变为浅绿色时发生反应的离子方程式Fe3++Fe(HSO3)2++H2O=2Fe2++SO42-+3H+
(6)通过实验可知加热和增加FeCl3溶液的酸度可缩短浅绿色出现的时间.
[探究一]:SO2能否被BaCl2溶液吸收.
甲.乙两同学分别设计如图装置甲和装置乙进行探究
甲、乙两同学实验时观察到各仪器中的现象如下:
| A | B | C | D | |
| 装置甲中的现象 | Na2SO3固体表面有气泡.瓶中白雾 | 白色沉淀 | ----- | ------ |
| 装置乙中的现象 | Na2SO3固体表面有气泡.瓶中白雾 | 有气泡 | 有气泡 | 品红褪色 |
(1)甲同学经过后续实验确证了B中白色沉淀是BaSO4.甲同学的后续实验操作是打开B试管的胶塞,向其中滴加稀盐酸,若白色沉淀不消失,证明白色沉淀是BaSO4

(2)乙同学分析装置甲中产生BaSO4的可能原因有:
①A中产生的白雾是硫酸的酸雾,进入B中与BaCl2溶液反应生成BaSO4沉淀.
②2SO2+O2+2H2O+2Ba2+=2BaSO4+4H+(用离子方程式表示).
(3)装置乙中B中所盛试剂是饱和NaHSO3溶液;乙同学在滴加浓硫酸之前的操作是打开弹簧夹向A中通往一段时间的N2,然后关闭弹簧夹
(4)通过上述实验,得出的结论是SO2不能被BaCl2溶液吸收
[探究二]:SO2与FeCl3溶液的反应
查阅资料:①Fe(HSO3)2+离子为红棕色,它可以将Fe3+还原为Fe2+;②生成Fe(HSO3)2+离子的反应为可逆反应.实验步骤为:
| 步骤I | 往5mL1mol•L-1 FeCl3溶液中通入SO2气体,溶液立即变为红棕色.微热3min,溶液颜色变为浅绿色. |
| 步骤II | 往5mL重新配制的1mol•L-1 FeCl3溶液(用浓盐酸酸化)中通入SO2气体,溶液立即变为红棕色.几分钟后,发现溶液颜色变成浅绿色. |
(5)当SO2通入到FeCl3(未用盐酸酸化)溶液至饱和时,同学们观察到的现象是溶液由棕黄色变成红棕色,没有观察到丁达尔现象.将混合液放置12小时,溶液才变成浅绿色.
则溶液由棕黄色变成红棕色的原因是二氧化硫溶于水SO2+H2O?HSO3-+H+,Fe3++HSO3-?Fe(HSO3)2+;写出溶液由红棕色变为浅绿色时发生反应的离子方程式Fe3++Fe(HSO3)2++H2O=2Fe2++SO42-+3H+
(6)通过实验可知加热和增加FeCl3溶液的酸度可缩短浅绿色出现的时间.
19.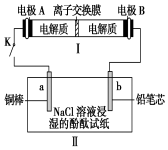 如图所示装置Ⅰ是可充电电池.已知:该充电电池充电时的反应为:
如图所示装置Ⅰ是可充电电池.已知:该充电电池充电时的反应为:
Na2Sx+3NaBr→2Na2Sy+NaBr3,闭合开关K时,装置Ⅱ中b极附近变红色.下列说法正确的是( )
 如图所示装置Ⅰ是可充电电池.已知:该充电电池充电时的反应为:
如图所示装置Ⅰ是可充电电池.已知:该充电电池充电时的反应为:Na2Sx+3NaBr→2Na2Sy+NaBr3,闭合开关K时,装置Ⅱ中b极附近变红色.下列说法正确的是( )
| A. | 闭合开关K时,电极B上发生的反应是:Br3-+2e-═3Br- | |
| B. | 闭合开关K时,I中Na+移向A极,II中Na+移向a极 | |
| C. | 当有0.01 mol Na+通过离子交换膜时,b电极上析出标准状况下的气体112 mL | |
| D. | 闭合开关K时,Ⅱ中发生反应的离子方程式为:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑ |
18.已知:CH3C≡CH+CO+CH3OH$\stackrel{一定条件}{→}$X;X+H2O$\stackrel{一定条件}{→}$Y+CH3OH下列说法正确的是( )
| A. | X的分子式为C5H10O2 | |
| B. | X可能的结构有两种 | |
| C. | Y中含有的官能团有羧基和碳碳双键 | |
| D. | X与Y相对分子质量相差14,则X与Y互为同系物 |
17.X、Y、Z、W均为元素周期表中前20号元素,其原子序数依次增大.已知:X与Y可形成原子个数比为1:1的化合物.Z、W简单离子的电子层结构相同.下列说法正确的是( )
| A. | 若X为IA族时,Y不可能是第三周期VIA族元素 | |
| B. | 由X、Y、Z、W四种元素不可能形成其原子个数比为1:3:1:1的化合物 | |
| C. | Z元素的原子半径一定小于W元素的原子半径 | |
| D. | 若X为IVA族元素时,X、Y两元素可形成含有共价键的离子化合物 |
16.某有机高分子化合物的结构简式如图所示.该有机高分子化合物的单体不能发生的反应是( )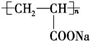
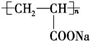
| A. | 酯化反应 | B. | 氧化反应 | C. | 加成反应 | D. | 水解反应 |
15.常温下,取铝土矿(含有Al2O3、FeO、Fe2O3、SiO2等物质)用硫酸浸出后的溶液,分别向其中加入指定物质,反应后的溶液中能大量共存的一组离子正确的是( )
| A. | 加入过量NaOH溶液:Na+、AlO2-、OH-、SO42- | |
| B. | 加入过量氨水:NH4+、Al3+、OH-、SO42- | |
| C. | 通入过量Cl2:Fe2+、Na+、Cl-、SO42- | |
| D. | 通入过量SO2:Fe2+、H+、SO32-、SO42- |
14.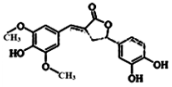 天然有机化合物甲的结构简式如图,该物质具有一定的除草功效,有关该化合物的说法正确的是( )
天然有机化合物甲的结构简式如图,该物质具有一定的除草功效,有关该化合物的说法正确的是( )
 天然有机化合物甲的结构简式如图,该物质具有一定的除草功效,有关该化合物的说法正确的是( )
天然有机化合物甲的结构简式如图,该物质具有一定的除草功效,有关该化合物的说法正确的是( )| A. | 既能与FeCl3发生显色反应,也能和NaHCO3反应放出CO2 | |
| B. | 1 mol该化合物最多能与6 mol NaOH 反应 | |
| C. | 1 mol 该化合物最多能与含5 mol Br2的浓溴水反应 | |
| D. | 该化合物分子中含有三种含氧官能团 |
13.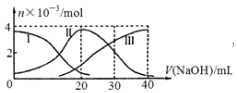 手持技术是基于数据采集器、传感器和多媒体计算机构成的一种新兴掌上试验系统,具有实时、定量、直观等特点,如图是利用手持技术得到的微粒的物质的量的变化图,常温下向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液,其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-,下列说法正确的是( )
手持技术是基于数据采集器、传感器和多媒体计算机构成的一种新兴掌上试验系统,具有实时、定量、直观等特点,如图是利用手持技术得到的微粒的物质的量的变化图,常温下向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液,其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-,下列说法正确的是( )
0 162398 162406 162412 162416 162422 162424 162428 162434 162436 162442 162448 162452 162454 162458 162464 162466 162472 162476 162478 162482 162484 162488 162490 162492 162493 162494 162496 162497 162498 162500 162502 162506 162508 162512 162514 162518 162524 162526 162532 162536 162538 162542 162548 162554 162556 162562 162566 162568 162574 162578 162584 162592 203614
 手持技术是基于数据采集器、传感器和多媒体计算机构成的一种新兴掌上试验系统,具有实时、定量、直观等特点,如图是利用手持技术得到的微粒的物质的量的变化图,常温下向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液,其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-,下列说法正确的是( )
手持技术是基于数据采集器、传感器和多媒体计算机构成的一种新兴掌上试验系统,具有实时、定量、直观等特点,如图是利用手持技术得到的微粒的物质的量的变化图,常温下向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液,其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-,下列说法正确的是( )| A. | H2A在水中的电离方程式是:H2A═2H++A2- | |
| B. | 当V(NaOH)=40mL时,其溶液中水的电离受到抑制 | |
| C. | 当V(NaOH)=20mL时,则有:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) | |
| D. | 当V(NaOH)=30mL时,则有:c(H+)+c(Na+)═c(A2-)+c(OH-)+c(HA-) |