11.碱式氧化镍(NiOOH)可用作镍氢电池的正极材料,可用废镍催化剂(主要含Ni、Al,少量Cr、FeS等)来制备,其工艺流程如图1:
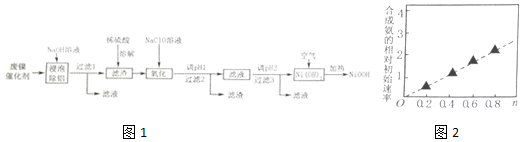
回答下列问题:
(1)“浸泡除铝”时,发生反应的化学方程式为2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
(2)“溶解”时放出的气体为H2、H2S(填化学式).硫酸镍溶液可用于制备合成氨的催化剂ConNi(1-n)Fe2O4.如图2表示在其他条件相同时合成氨的相对初始速率随催化剂中n值变化的曲线,由图分析可知Co2+、Ni2+两种离子中催化效果更好的是Co2+.
(3)“氧化”时,酸性条件下,溶液中的Fe2+被氧化为Fe3+,其离子方程式为2Fe2++ClO-+2H+=2Fe3++Cl-+H2O
(4)已知该条件下金属离子开始沉淀和完全沉淀的pH如表:
“调pH1”时,溶液pH范围为5.6~6.2;过滤2所得滤渣的成分Cr(OH)3和Fe(OH)3(填化学式).
(5)写出在空气中加热Ni(OH)2制取NiOOH的化学方程式4Ni(OH)2+O2$\frac{\underline{\;加热\;}}{\;}$4NiOOH+2H2O.
(6)含镍金属氢化物MH-Ni燃料电池是一种绿色环保电池,广泛应用于电动汽车.其中M代表储氢合金,MH代表金属氢化物,电解质溶液可以是KOH水溶液.它的充、放电反应为:xNi(OH)2+M$?_{充电}^{放电}$MHx+xNiOOH;电池充电过程中阳极的电极反应式为Ni(OH)2+OH--e-=NiOOH+H2O;放电时负极的电极反应式为MHx+xOH--xe-=M++xH2O.

回答下列问题:
(1)“浸泡除铝”时,发生反应的化学方程式为2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
(2)“溶解”时放出的气体为H2、H2S(填化学式).硫酸镍溶液可用于制备合成氨的催化剂ConNi(1-n)Fe2O4.如图2表示在其他条件相同时合成氨的相对初始速率随催化剂中n值变化的曲线,由图分析可知Co2+、Ni2+两种离子中催化效果更好的是Co2+.
(3)“氧化”时,酸性条件下,溶液中的Fe2+被氧化为Fe3+,其离子方程式为2Fe2++ClO-+2H+=2Fe3++Cl-+H2O
(4)已知该条件下金属离子开始沉淀和完全沉淀的pH如表:
| 开始沉淀的pH | 完全沉淀的pH | |
| Ni2+ | 6.2 | 8.6 |
| Fe2+ | 7.6 | 9.1 |
| Fe3+ | 2.3 | 3.3 |
| Cr3+ | 4.5 | 5.6 |
(5)写出在空气中加热Ni(OH)2制取NiOOH的化学方程式4Ni(OH)2+O2$\frac{\underline{\;加热\;}}{\;}$4NiOOH+2H2O.
(6)含镍金属氢化物MH-Ni燃料电池是一种绿色环保电池,广泛应用于电动汽车.其中M代表储氢合金,MH代表金属氢化物,电解质溶液可以是KOH水溶液.它的充、放电反应为:xNi(OH)2+M$?_{充电}^{放电}$MHx+xNiOOH;电池充电过程中阳极的电极反应式为Ni(OH)2+OH--e-=NiOOH+H2O;放电时负极的电极反应式为MHx+xOH--xe-=M++xH2O.
10.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,22.4 L SO3与水反应生成1 mol硫酸 | |
| B. | 1 L 1mol/L醋酸溶液中离子总数为2 NA | |
| C. | 78 g苯中含有的碳碳双键的数目为3 NA | |
| D. | 1 mol N2与3 mol H2在一定条件下充分反应生成的NH3分子数小于2 NA |
9.实验是化学研究的基础,下图关于各实验装置(夹持装置已略去)的叙述,正确的是( )
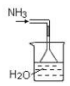
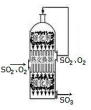
| A. | 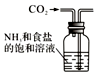 装置可用于模拟侯氏制碱法制取碳酸氢钠 | |
| B. | 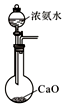 装置可用于制备少量NH3 | |
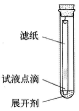
| C. |  装置可用于准确量取一定体积K2Cr2O7标准溶液 | |
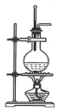
| D. | 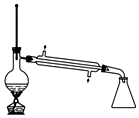 装置常用于分离互不相溶的液体混合物 |
8.下列有关说法错误的是( )
| A. | 裂化汽油不能用于萃取溴水中的溴 | |
| B. | 分子式为C5H10O2并能与饱和NaHCO3溶液反应放出气体的有机物有(不含立体异构)4种 | |
| C. | 实验室中,可用金属钠检验乙醇中是否含有水 | |
| D. | 油脂在碱性条件下的水解反应称为皂化反应 |
7.以下关于中国化学史的表述错误的是( )
| A. | 杜康用高粱酿酒的原理是通过蒸馏法将高粱中的乙醇分离出来 | |
| B. | 蔡伦利用树皮、碎布(麻布)、麻头等原料精制出优质纸张 | |
| C. | 《本草纲目》中记载“(火药)乃焰消(KNO3)、硫磺、杉木炭所合,以为烽燧铳机诸药者”这是利用了KNO3的氧化性 | |
| D. | 英文的“中国”(China)又指“瓷器”,说明我国很早就应用化学技术制作陶瓷 |
6.下列反应的离子方程式书写正确的是( )
| A. | 铁粉与稀H2SO4反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | Na2CO3溶液与足量盐酸反应:CO32-+2H+═CO2↑+H2O | |
| C. | Cu(OH)2固体与稀硫酸反应:OH-+H+═H2O | |
| D. | 铝片与NaOH溶液反应:Al+OH-+H2O═AlO2-+H2↑ |
5.已知氯气、溴蒸气分别跟氢气反应的热化学方程式如下(Q1、Q2均为正值):H2(g)+Cl2(g)→2HCl(g)+Q1KJ H2(g)+Br2(g)→2HBr(g)+Q2KJ 根据上述反应做出的判断不正确的是( )
| A. | Q1>Q2 | |
| B. | 生成物总能量均低于反应物总能量 | |
| C. | 生成 2mol HCl(g)放出 Q1KJ 热量 | |
| D. | 若反应生成 2mol 液态溴化氢,放出的热量低于 Q2KJ |
3.实验室制备乙酸丁酯的叙述正确的是( )
| A. | 采用水浴加热法控制温度 | |
| B. | 采用边反应边蒸馏的方法提高产率 | |
| C. | 制取装置中有冷凝回流措施 | |
| D. | 用水和氢氧化钠溶液洗涤后分液分离出产品 |
2.化学在生活中有着广泛的应用.下列对应关系错误的是( )
0 162395 162403 162409 162413 162419 162421 162425 162431 162433 162439 162445 162449 162451 162455 162461 162463 162469 162473 162475 162479 162481 162485 162487 162489 162490 162491 162493 162494 162495 162497 162499 162503 162505 162509 162511 162515 162521 162523 162529 162533 162535 162539 162545 162551 162553 162559 162563 162565 162571 162575 162581 162589 203614
| 选项 | 化学性质 | 实际应用 |
| A | Al2(SO4)3和小苏打反应 | 泡沫灭火器灭火 |
| B | 铁比铜金属性强 | FeCl3腐蚀Cu刻制印刷电路板 |
| C | 次氯酸盐具有氧化性 | 漂白粉漂白织物 |
| D | 乙酸具有酸性 | 常用于去除水垢 |
| A. | A | B. | B | C. | C | D. | D |