10.(1)在同一个原子中,离核越近、n越小的能层中的电子能量越低.理论研究证明,多电子原子中,同一能层的电子,能量也可能不同,还可以把它们分成能级,第三能层有3个能级,分别为3s、3p和3d.现代物质结构理论证实,原子的电子排布遵循构造原理能使整个原子的能量处于最低状态,处于最低能量的原子叫做基态原子.
(2)写出下列基态原子的简化电子排布式:
①14Si1s22s22p63s23p2 或[Ne]3s23p2;②26Fe1s22s22p63s23p63d64s2或[Ar]3d64s2 .
(3)按所示格式填写表中的空格:
(4)N≡N的键能为942kJ•mol-1,N-N单键的键能为247kJ•mol-1,计算说明N2中的π键更稳定(填“σ”或“π”).
(5)在配离子[Fe(SCN)]2+中,提供空轨道接受孤电子对的微粒是Fe3+,配离子[Cu(NH3)4]2+的配体是NH3.
(6)根据价层电子对互斥理论判断:
①NH3分子中,中心原子上的σ键电子对数为3,孤电子对数为1,价层电子对数为4,中心原子的杂化方式为sp3杂化,VSEPR构型为四面体形,分子的立体构型为三角锥形.
②BF3分子中,中心原子的杂化方式为sp2杂化,分子的立体构型为平面(正)三角形.
(2)写出下列基态原子的简化电子排布式:
①14Si1s22s22p63s23p2 或[Ne]3s23p2;②26Fe1s22s22p63s23p63d64s2或[Ar]3d64s2 .
(3)按所示格式填写表中的空格:
| 原子序数 | 原子的价电子排布式 | 周期 | 族 |
| 17 | 第三 | ||
| 3d54s1 | ⅥB |
(5)在配离子[Fe(SCN)]2+中,提供空轨道接受孤电子对的微粒是Fe3+,配离子[Cu(NH3)4]2+的配体是NH3.
(6)根据价层电子对互斥理论判断:
①NH3分子中,中心原子上的σ键电子对数为3,孤电子对数为1,价层电子对数为4,中心原子的杂化方式为sp3杂化,VSEPR构型为四面体形,分子的立体构型为三角锥形.
②BF3分子中,中心原子的杂化方式为sp2杂化,分子的立体构型为平面(正)三角形.
9.下列分离或提纯物质的方法、操作正确的是( )
| A. | 用溶解、过滤的方法提纯含有少量BaSO4的BaCO3 | |
| B. | 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| C. | 用过滤的方法除去NaCl溶液中含有的少量淀粉胶体 | |
| D. | 将制得晶体转移到新制过滤器中用大量水进行洗涤 |
6.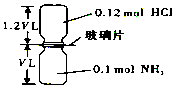 如图,抽去如图所示装置中的玻璃片,使两种气体充分反应(整个过程中认为装置气密性良好),等温度恢复到原来温度.(已知反应:HCl+NH3═NH4Cl(固体))下列说法正确的是( )
如图,抽去如图所示装置中的玻璃片,使两种气体充分反应(整个过程中认为装置气密性良好),等温度恢复到原来温度.(已知反应:HCl+NH3═NH4Cl(固体))下列说法正确的是( )
 如图,抽去如图所示装置中的玻璃片,使两种气体充分反应(整个过程中认为装置气密性良好),等温度恢复到原来温度.(已知反应:HCl+NH3═NH4Cl(固体))下列说法正确的是( )
如图,抽去如图所示装置中的玻璃片,使两种气体充分反应(整个过程中认为装置气密性良好),等温度恢复到原来温度.(已知反应:HCl+NH3═NH4Cl(固体))下列说法正确的是( )| A. | 反应后瓶内压强是反应前的$\frac{1}{10}$ | |
| B. | 装置中氢元素的总质量为0.42g | |
| C. | 生成物的分子数目为0.1NA | |
| D. | 反应结束后,两个集气瓶很容易分开 |
5.如表是元素周期表的一部分,表中所列的字母分别代表某一化学元素
(1)表中所列元素中属于主族元素的有a、b、c、d、f、g、h、i、j、k、l;属于金属元素的有b、c、d、e、f、h;e在元素周期表中的位置是第四周期 VIII族.
(2)下列AC组元素的单质可能都是电的良导体.
A.d、e、f B.b、c、i C.c、d、g D.a、g、k
(3)表中某元素的最高价氧化物对应水化物呈两性的化学式是Al(OH)3,
它与短周期元素b的最高价氧化物对应水化物发生反应的离子方程式是Al(OH)3+OH-=AlO2-+2H2O;
(4)b、a与j形成原子个数比为1:1:1的化合物中含有的化学键类型是离子键和共价键.
| a | ||||||||||||||||||
| g | j | |||||||||||||||||
| b | c | f | i | l | m | |||||||||||||
| e | h | k | ||||||||||||||||
(2)下列AC组元素的单质可能都是电的良导体.
A.d、e、f B.b、c、i C.c、d、g D.a、g、k
(3)表中某元素的最高价氧化物对应水化物呈两性的化学式是Al(OH)3,
它与短周期元素b的最高价氧化物对应水化物发生反应的离子方程式是Al(OH)3+OH-=AlO2-+2H2O;
(4)b、a与j形成原子个数比为1:1:1的化合物中含有的化学键类型是离子键和共价键.
4.一定量的甲烷燃烧后得到的产物为二氧化碳、一氧化碳和水蒸气,将产生的气体按顺序通过装有无水氯化钙和氢氧化钠的硬质玻璃管,氢氧化钠管的质量增加了4.4g,则甲烷在标准状况下的体积是多少,无水氯化钙的质量增加了 ( )
| A. | 0.56L 1.8g | B. | 1.12L 3.6g | C. | 2.24L 1.8g | D. | 2.24L 3.6g |
3.当足量的CO通过玻璃管内灼热的某一氧化物后,充分反应,管内物质质量减少了27.5%,则氧化物为( )
| A. | CuO | B. | MnO2 | C. | Fe2O3 | D. | Fe3O4 |
2.向60mLNa2SO4溶液中加入BaCl2溶液,有关数据见表( )
0 162391 162399 162405 162409 162415 162417 162421 162427 162429 162435 162441 162445 162447 162451 162457 162459 162465 162469 162471 162475 162477 162481 162483 162485 162486 162487 162489 162490 162491 162493 162495 162499 162501 162505 162507 162511 162517 162519 162525 162529 162531 162535 162541 162547 162549 162555 162559 162561 162567 162571 162577 162585 203614
| 实验编号 | 1 | 2 | 3 | 4 | 5 |
| BaCl2溶液体积/mL | 0 | 30 | 60 | 100 | 120 |
| 沉淀质量/g | 0 | 0.699 | x | 2.097 | 2.097 |
| A.混合前,BaCl2溶液的物质的量浓度为0.10mol•L-1 |
| B.混合前,Na2SO4溶液的物质的量浓度为0.15mol•L-1 |
| C.3号实验中沉淀的质量x为1.398g |
| D.完全沉淀60mL Na2SO4溶液消耗BaCl2溶液的体积为80mL |
| A. | A | B. | B | C. | C | D. | D |