7.下列过程放出热量的是( )
| A. | 冰的融化 | B. | 水的分解 | C. | 硝酸铵溶于水 | D. | 浓硫酸稀释 |
6.如图所示可逆反应在使用和未使用催化剂时,反应过程和能量的对应关系.下列说法正确的是( )


| A. | 反应物的总能量大于生成物的总能量 | |
| B. | 反应产生的热效应Q=E1-E2 | |
| C. | a与b相比,反应的平衡常数一定不同 | |
| D. | a与b相比,a的反应速率更快 |
5.向 0.1mol/L 醋酸溶液中加水稀释,下列变化叙述错误的是( )
| A. | 溶液的 pH 逐渐增大 | B. | 溶液中的 c(OH-)逐渐减小 | ||
| C. | 醋酸的电离程度逐渐增大 | D. | 溶液的导电能力逐渐减小 |
4.下列说法中正确的是( )
| A. | 丙烯所有原子均在同一平面上 | |
| B. | 利用粮食酿酒经历了淀粉→葡萄糖→乙醇的化学变化过程 | |
| C. | 乙烯和苯加入溴水中,都能观察到褪色现象,原因是都发生了加成反应 | |
| D. | 分子式为C8H10的某芳香烃的一氯代物可能只有一种 |
3.原子序数依次递增的四种短周期元素可形成简单离子X2-、Y+、Z3+、M2-,下列说法错误的是( )
| A. | 工业上常采用电解法冶炼Z单质 | |
| B. | 气态氢化物的稳定性:H2X>H2M | |
| C. | 离子半径由大到小:M2->Y+>Z3+>X2- | |
| D. | X、Y形成的化合物中阳离子、阴离子个数比一定是2:1 |
1.X、Y、Z、W为四种短周期主族元素,且原子序数依次递增,其中X、Z同主族,Y原子半径是短周期主族元素中最大的,X原子最外层电子数是核外电子层数的3倍,下列说法正确的是( )
| A. | 原子半径:rW>rZ>rY>rX | |
| B. | Z的氢化物比X的氢化物稳定 | |
| C. | X、Y、Z三种元素组成的化合物不止2种 | |
| D. | W元素氧化物对应水化物的酸性一定强于Z |
20.元素X、Y、Z、W、Q、M在元素周期表的相对位置如表所示,其中Z元素是目前发现的非金属性最强的元素,下列说法正确的是( )
| X | Y | Z | |
| W | Q | M |
| A. | 对应氢化物的沸点Y>Q是因为Y的非金属性比Q强 | |
| B. | XM4的比例模型为  其二氢取代物有两种 其二氢取代物有两种 | |
| C. | W的氧化物,常温下可以和Z、M的氢化物反应 | |
| D. | Z的单质能将Y的单质从其氢化物中置换出来 |
19.下列关于有机物的说法正确的是( )
| A. | C4H8Cl2有9种同分异构体 | |
| B. | 糖类、油脂、蛋白质均能发生水解反应 | |
| C. | 通过乙烯的取代反应可制得氯乙烷 | |
| D. | 乙醇、乙酸均能与NaOH 溶液反应 |
18. 现代煤化工产生的H2S是一种重要的工业资源.请回答:
现代煤化工产生的H2S是一种重要的工业资源.请回答:
(1)用过量的NaOH吸收H2S,请写出该反应的离子方程式:H2S+2OH-=S 2-+2H2O.硫化钠又称臭碱,其溶液盛装在带橡胶塞的试剂瓶中,请用离子方程式解释其溶液呈碱性的原因为:S 2-+H2O?HS-+OH-.己知:25℃时,H2S的Ka1=1×10-7,Ka2=1×10-12,计算此温度时1mol/LNa2S溶液的pH=12.(结果取整数)
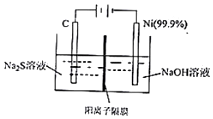
(2)用电解法处理Na2S溶液是处理硫化氢废气的一个重要环节.实验装置如图:
已知阳极的反应为xS2--2(x-1)e-=Sx2-,则阴极的电极反应式是2H++2e-=H2↑或2H2O+2e-=2OH-+H2↑,当反应转移nmole-时,产生标准状况下的气休体积为11.2 n L.
(3)H2S是煤化工原料气脱硫过程的重要中间体.反应原理为:
①COS(g)+H2(g)?H2S(g)+CO(g)△H=+7KJ/mol
②CO(g)+H2O(g)?CO2(g)+H2(g)△H=-42KJ/mol
已知断裂1mol气态分子中的化学键所需能量如表所示.
计算表中x=1074.
(4)向2L容积不变的密闭容器中充入2molCOS(g),2molH2(g)和2molH2O(g),进行(3)中所述两个反应,其他条件不变,随着温度升高,CO的平衡体积分数增大,解释其原因为反应①吸热反应,升高温度,平衡正向动,CO的平衡体积分数增大,反应②是放热反应,升温平衡逆向进行,一氧化碳的平衡体积分数也增大.平衡体系中COS的物质的量为1.6mol时,CO的体积分数为5%,则H2O的平衡转化率为5%,反应②的平衡常数为0.30(保留两位有效数字).
0 162376 162384 162390 162394 162400 162402 162406 162412 162414 162420 162426 162430 162432 162436 162442 162444 162450 162454 162456 162460 162462 162466 162468 162470 162471 162472 162474 162475 162476 162478 162480 162484 162486 162490 162492 162496 162502 162504 162510 162514 162516 162520 162526 162532 162534 162540 162544 162546 162552 162556 162562 162570 203614
 现代煤化工产生的H2S是一种重要的工业资源.请回答:
现代煤化工产生的H2S是一种重要的工业资源.请回答:(1)用过量的NaOH吸收H2S,请写出该反应的离子方程式:H2S+2OH-=S 2-+2H2O.硫化钠又称臭碱,其溶液盛装在带橡胶塞的试剂瓶中,请用离子方程式解释其溶液呈碱性的原因为:S 2-+H2O?HS-+OH-.己知:25℃时,H2S的Ka1=1×10-7,Ka2=1×10-12,计算此温度时1mol/LNa2S溶液的pH=12.(结果取整数)
(2)用电解法处理Na2S溶液是处理硫化氢废气的一个重要环节.实验装置如图:
已知阳极的反应为xS2--2(x-1)e-=Sx2-,则阴极的电极反应式是2H++2e-=H2↑或2H2O+2e-=2OH-+H2↑,当反应转移nmole-时,产生标准状况下的气休体积为11.2 n L.
(3)H2S是煤化工原料气脱硫过程的重要中间体.反应原理为:
①COS(g)+H2(g)?H2S(g)+CO(g)△H=+7KJ/mol
②CO(g)+H2O(g)?CO2(g)+H2(g)△H=-42KJ/mol
已知断裂1mol气态分子中的化学键所需能量如表所示.
| 分子 | COS | H2 | H2O | CO | H2S | CO2 |
| 能量/KJ/mol | 1323 | 436 | 926 | X | 678 | 1606 |
(4)向2L容积不变的密闭容器中充入2molCOS(g),2molH2(g)和2molH2O(g),进行(3)中所述两个反应,其他条件不变,随着温度升高,CO的平衡体积分数增大,解释其原因为反应①吸热反应,升高温度,平衡正向动,CO的平衡体积分数增大,反应②是放热反应,升温平衡逆向进行,一氧化碳的平衡体积分数也增大.平衡体系中COS的物质的量为1.6mol时,CO的体积分数为5%,则H2O的平衡转化率为5%,反应②的平衡常数为0.30(保留两位有效数字).