7.草酸是植物(特别是草本植物)常具有的成分,具有广泛的用途.草酸晶体(H2C2O4•2H2O)无色,熔点为101℃,易溶于水,受热易脱水、升华,170℃以上分解.常温下它的电离常数K1=5.4×10-2,K2=5.4×10-5.回答下列问题:
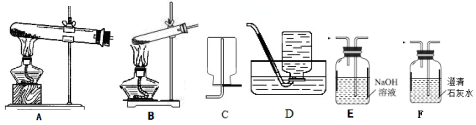
(1)拟用下列装置分解草酸制备少量纯净的CO,其合理的连接顺序为B-E-D(填字母序号).
(2)相同温度条件下,分别用3支试管按下列要求完成实验:
写出试管B的离子方程式2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O;上述实验能否说明“相同条件下,反应物浓度越大,反应速率越快”?能(选填“能”或“不能”);简述你的理由:实验中KMnO4的浓度cB>cA,且其反应速率νB>νA.
(3)设计实验证明草酸为弱酸的方案及其现象均正确的有AC(填序号).
A.室温下,取0.010mol/L的H2C2O4溶液,测其pH=2;
B.室温下,取0.010mol/L的NaHC2O4溶液,测其pH>7;
C.室温下,取pH=a(a<3)的H2C2O4溶液稀释100倍后,测其pH<a+2;
D.标况下,取0.10mol/L的H2C2O4溶液100mL与足量锌粉反应,收集到H2体积为224mL;
(4)为测定某H2C2O4溶液的浓度,取20.00mL H2C2O4溶液于锥形瓶中,滴入2-3滴指示剂,用0.1000mol/L的NaOH溶液进行滴定,并进行3次平行实验,所用NaOH溶液体积分别为19.98mL、20.02mL和22.02mL.
①所用指示剂为酚酞;滴定终点时的现象为锥形瓶内溶液由无色变成(粉)红色,且半分钟内不变化;
②H2C2O4溶液物质的量浓度为0.05000mol/L;
③下列操作会引起测定结果偏高的是AD(填序号).
A.滴定管在盛装NaOH溶液前未润洗
B.滴定过程中,锥形瓶震荡的太剧烈,以致部分液体溅出
C.滴定前读数正确,滴定终点时俯视读数
D.滴定前读数正确,滴定终点时仰视读数.
(1)拟用下列装置分解草酸制备少量纯净的CO,其合理的连接顺序为B-E-D(填字母序号).

(2)相同温度条件下,分别用3支试管按下列要求完成实验:
| 试管 | A | B | C |
加入试剂 | 4mL 0.01mol/L KMnO4 1ml 0.1moL/L H2SO4 2mL 0.1mol/L H2C2O4 | 4mL 0.02mol/L KMnO4 1ml 0.1moL/L H2SO4 2mL 0.1mol/L H2C2O4 | 4mL 0.03mol/L KMnO4 1ml 0.1moL/L H2SO4 2mL 0.1mol/L H2C2O4 |
| 褪色时间 | 28秒 | 30秒 | 不褪色 |
(3)设计实验证明草酸为弱酸的方案及其现象均正确的有AC(填序号).
A.室温下,取0.010mol/L的H2C2O4溶液,测其pH=2;
B.室温下,取0.010mol/L的NaHC2O4溶液,测其pH>7;
C.室温下,取pH=a(a<3)的H2C2O4溶液稀释100倍后,测其pH<a+2;
D.标况下,取0.10mol/L的H2C2O4溶液100mL与足量锌粉反应,收集到H2体积为224mL;
(4)为测定某H2C2O4溶液的浓度,取20.00mL H2C2O4溶液于锥形瓶中,滴入2-3滴指示剂,用0.1000mol/L的NaOH溶液进行滴定,并进行3次平行实验,所用NaOH溶液体积分别为19.98mL、20.02mL和22.02mL.
①所用指示剂为酚酞;滴定终点时的现象为锥形瓶内溶液由无色变成(粉)红色,且半分钟内不变化;
②H2C2O4溶液物质的量浓度为0.05000mol/L;
③下列操作会引起测定结果偏高的是AD(填序号).
A.滴定管在盛装NaOH溶液前未润洗
B.滴定过程中,锥形瓶震荡的太剧烈,以致部分液体溅出
C.滴定前读数正确,滴定终点时俯视读数
D.滴定前读数正确,滴定终点时仰视读数.
6.下列实验操作、现象和结论均正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向硝酸银溶液中滴加过量氨水 | 溶液澄清 | Ag+与NH3•H2O能大量共存 |
| B | 向某溶液中滴加CCl4,振荡静置 | 下层溶液显紫色 | 原溶液中含有I- |
| C | 向25mL沸水中分别滴入5~6滴FeCl3饱和溶液,继续煮沸至出现红褐色沉淀,用激光笔照射 | 形成一条光亮通路 | 制得Fe(OH)3胶体 |
| D | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体 | 溶液颜色变浅 | Na2CO3溶液中存在水解平衡 |
| A. | A | B. | B | C. | C | D. | D |
5.X、Y、Z、W四种短周期元素,化合物XZ可刻蚀玻璃,Y元素原子的最外层电子数是内层电子数的3倍,W+与Z的简单离子有相同的电子层排布.下列说法正确的是( )
| A. | 气态氢化物的热稳定性:Y>Z | |
| B. | W与另外三种元素均可形成离子键 | |
| C. | 简单离子半径:W>Y>Z | |
| D. | W和Y可形成阴阳离子个数比是1:1的化合物 |
4.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 过氧化钠与二氧化碳反应时,生成0.1mol氧气转移的电子数为0.4NA | |
| B. | 标准状况下,22.4LH2O含有2NA个共价键 | |
| C. | 常温下,23g NO2含有NA个氧原子 | |
| D. | 1mol ${\;}_{8}^{18}$O2的中子数是20 NA |
3.下述实验操作与预期实验目的或所得实验结论不一致的是( )
| 编号 | 实验操作 | 实验目的或结论 |
| A | 将SO2气体通入紫色石蕊试液中,观察溶液是否褪色 | 证明SO2有漂白性 |
| B | 向试管中加入等体积的0.005mol/L的FeCl3溶液和0.01mol/L的KSCN溶液,再滴加几滴饱和FeCl3溶液,观察颜色变化 | 探究增大反应物浓度时平衡移动的方向 |
| C | 将装有NO2和N2O4气体的联通球,一个置于冰水中,一个置于热水中,观察颜色变化 | 探究温度对化学平衡的影响 |
| D | 向硫酸铝溶液中滴加过量的氢氧化钡溶液 产生白色沉淀 | 证明氢氧化铝不溶于过量的氢氧化钡溶液 |
| A. | A | B. | B | C. | C | D. | D |
2.下列说法正确的是( )
| A. | 氯气、液氯和氯水是同一种物质 | |
| B. | Na2O、Na2O2组成元素相同,与CO2都能发生氧化还原反应 | |
| C. | 硫酸钡难溶于水,但硫酸钡是电解质 | |
| D. | 新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色 |
1.水溶液中能大量共存的一组离子是( )
| A. | K+、Ca2+、OH-、HCO3- | B. | Fe2+、H+、CO32-、Cl- | ||
| C. | Mg2+、NH4+、Cl-、SO42- | D. | K+、Fe3+、NO3-、SCN- |
20.下列离子方程式正确的是( )
| A. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| B. | 氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| C. | 过量二氧化硫通入氢氧化钠溶液中:SO2+OH-═SO32-+H2O | |
| D. | 氯化铁溶液与铜粉反应:Cu+2Fe3+═2Fe2++Cu2+ |
19.下列表示物质或微粒的化学用语或模型正确的是( )
| A. | 氮分子的结构式:N-N | B. | H2O2的电子式: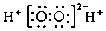 | ||
| C. | 14C的原子结构示意图: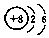 | D. | 钙离子的电子式:Ca2+ |
18.环丙烷叉环丙烷结构为: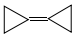 ,由于其具有特殊的电子结构一直受到理论化学家的关注.下列关于环丙烷叉环丙烷的说法错误的是( )
,由于其具有特殊的电子结构一直受到理论化学家的关注.下列关于环丙烷叉环丙烷的说法错误的是( )
0 162374 162382 162388 162392 162398 162400 162404 162410 162412 162418 162424 162428 162430 162434 162440 162442 162448 162452 162454 162458 162460 162464 162466 162468 162469 162470 162472 162473 162474 162476 162478 162482 162484 162488 162490 162494 162500 162502 162508 162512 162514 162518 162524 162530 162532 162538 162542 162544 162550 162554 162560 162568 203614
 ,由于其具有特殊的电子结构一直受到理论化学家的关注.下列关于环丙烷叉环丙烷的说法错误的是( )
,由于其具有特殊的电子结构一直受到理论化学家的关注.下列关于环丙烷叉环丙烷的说法错误的是( )| A. | 一氯取代物有1种 | B. | 不可能是环丙烷的同系物 | ||
| C. | 与环己二烯(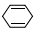 )是同分异构体 )是同分异构体 | D. | 所有的原子均在同一平面内 |