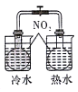
5.某同学探究NaHCO3的性质,部分实验报吿记录如下:
下列说法不正确的是( )
| ①常温下,配制0.10moI/L NaHCO3溶液,测其pH为8.4; ②取少量该溶液于试管中,向其中滴加CaCl2溶液至中性,滴加过程中只产生一种白色沉淀(能与盐酸作用产生气体),但无气体放出. |
| A. | NaHCO3溶液呈碱性的原因是HCO3-的水解程度大于电离程度 | |
| B. | 加入CaCl2促进了HCO3-的水解 | |
| C. | 反应的离子方程式是2HCO3-+Ca2+═CaCO3↓+H2CO3 | |
| D. | 反应后的溶液中存在:c(Na+)+2c(Ca2+)═c(HCO3-)+2c(CO32-)+c(Cl-)、 |
4.下列说法正确的是( )
| A. | 制氢弹用到的D、T互为同位素 | |
| B. | 苛性钠溶液可用于治疗胃酸过多 | |
| C. | 硅胶可防止月饼等食品氧化变质 | |
| D. | 向海水中加入净水剂明矾可以使海水淡化 |
3.CoCl2•6H2O是一种饲料营养强化剂.一种利用水钴矿(主要成分为Co2O3、Co(OH)3,还含少量Fe2O3、A12O3、MnO等)制取CoCl2•6H2O的工艺流程如图1:
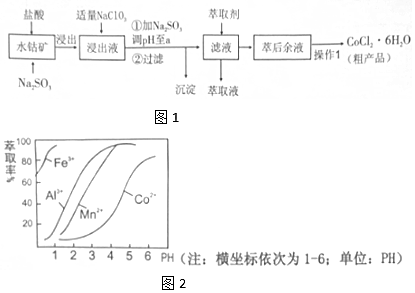
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表(金属离子浓度为0.01mol/L);
③CoCl2•6H2O熔点为86℃,加热至110〜120℃时,失去结晶水生成无水氯化钴.
(1)写出浸出过程中Co2O3发生反应的离子方程式:Co2O3+SO32-+4H+=2Co2++SO42-+2H2O.
(2)若不慎向“浸出液”中加过量NaClO2时,可能会生成有毒气体,写出生成该有毒气体的离子方程式:ClO3-+5Cl-+6H+=3Cl2↑+3H2O.
(3)“操作1”中包含3个基本实验操作,它们依次是蒸发浓缩、冷却结晶和过滤.制得的CoCl2•6H2O在烘干需减压烘干的原因是降低烘干温度,防止产品分解.
(4)萃取剂对金属离子的萃取率与pH的关系如图2向“滤液”中加入萃取剂的目的是除去溶液中的Mn2+,其使用的最佳pH范围是B.
A.2.0~2.5 B.3.0~3.5 C.4.0~4.5 D.5.0~5.5
(5)为测定粗产品中CoCl2•6H2O的含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2•6H2O的质量分数大于100%,其原因可能是粗产品含有可溶性氯化物或晶体失去了部分结晶水.(答条即可)

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表(金属离子浓度为0.01mol/L);
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)写出浸出过程中Co2O3发生反应的离子方程式:Co2O3+SO32-+4H+=2Co2++SO42-+2H2O.
(2)若不慎向“浸出液”中加过量NaClO2时,可能会生成有毒气体,写出生成该有毒气体的离子方程式:ClO3-+5Cl-+6H+=3Cl2↑+3H2O.
(3)“操作1”中包含3个基本实验操作,它们依次是蒸发浓缩、冷却结晶和过滤.制得的CoCl2•6H2O在烘干需减压烘干的原因是降低烘干温度,防止产品分解.
(4)萃取剂对金属离子的萃取率与pH的关系如图2向“滤液”中加入萃取剂的目的是除去溶液中的Mn2+,其使用的最佳pH范围是B.
A.2.0~2.5 B.3.0~3.5 C.4.0~4.5 D.5.0~5.5
(5)为测定粗产品中CoCl2•6H2O的含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2•6H2O的质量分数大于100%,其原因可能是粗产品含有可溶性氯化物或晶体失去了部分结晶水.(答条即可)
20.下列关于有机化合物的说法不正确的是( )
| A. | 二甲苯和四甲苯均有三种 | |
| B. | C3H8和C5H12一定互为同系物 | |
| C. | 石油裂解和油脂皂化均是由高分子物质生成小分子物质的过程 | |
| D. | 乙醇的酯化反应和酯的水解均属于取代反应 |
19.设NA为阿伏加德罗常数的数值,下列有关叙述正确的是( )
| A. | 100g 98%的浓硫酸中含有的氢原子数目为2NA | |
| B. | 16g16O2和18O2的混合物中含有的质子数目为8NA | |
| C. | 电解精炼铜的过程中,若阳极减重64g,则电路中一定通过2NA个电子 | |
| D. | 取50ml14.0mol/L浓硝酸与足量的铜片反应,生成气体分子的数目可能为0.25NA |
18.下列实验操作能达到相应实验目的是( )
| 选项 | 实验操作 | 实验目的 |
| A | 将C2H4和SO2的混合气体通入足量酸性KmnO4试液中 | 得到纯净的C2H4 |
| B | 向5mL 0.1mol•L-1AgNO3溶液中加1mL0.1mol•L-1NH3•H2O | 制备银氨溶液 |
| C | 向含少量FeBr2的FeCl2溶液中滴入适量新制氯水,并加入CCl4萃取分液 | 制备纯净的FeCl2溶液 |
| D | 向NaCl饱和溶液中先通入NH3至饱和,再通入足量CO2,过滤并洗涤 | 制备NaHCO3固体 |
| A. | A | B. | B | C. | C | D. | D |
16.下列有关实验操作、实验现象和所得结论均正确的是( )
0 162363 162371 162377 162381 162387 162389 162393 162399 162401 162407 162413 162417 162419 162423 162429 162431 162437 162441 162443 162447 162449 162453 162455 162457 162458 162459 162461 162462 162463 162465 162467 162471 162473 162477 162479 162483 162489 162491 162497 162501 162503 162507 162513 162519 162521 162527 162531 162533 162539 162543 162549 162557 203614
| 实验操作 | 实验现象 | 结论 | |
| A | 将SO2通人溴水中 | 溴水颜色褪去 | SO2具有漂白性 |
| B | 将铁屑放入稀HNO3中 | 放出无色气体 | Fe比H2活泼 |
| C | 将澄清石灰水滴入某溶液 | 生成白色沉淀 | 溶液中存CO32- |
| D | 将乙烯通入KMnO4酸性溶液 | KMnO4颜色褪去 | 乙烯具有还原性 |
| A. | A | B. | B | C. | C | D. | D |