14.设NA为阿伏伽德罗常数值,下列叙述不正确的是( )
| A. | 淀粉可用于酿酒 | |
| B. | 13g苯中含C-H键的数目是NA | |
| C. | C4H10O的醇有5种 | |
| D. | 标准状况下,11.2L甲烷和乙烯的混合物含氢原子数是2NA |
13.下列有关苯乙烯( 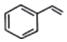 )的说法错误的是( )
)的说法错误的是( )
 )的说法错误的是( )
)的说法错误的是( )| A. | 苯乙烯与乙烯互为同系物 | B. | 所有原子可能在同一平面 | ||
| C. | 可使酸性KMnO4溶液褪色 | D. | 可发生加成反应 |
12.下列过程不涉及氧化还原反应的是( )
| A. | 钢铁腐蚀 | B. | 游泳池加漂白精消毒 | ||
| C. | 防毒面具中加Na2O2供氧 | D. | 纯碱去油污 |
10.25℃时,将浓度均为0.1mol/L、体积分别为Va 和Vb 的HA溶液与BOH溶液按不同体积比混合,保持Va+Vb=100mL,Va、Vb与混合液的pH的关系如图所示. 下列说法正确的是( )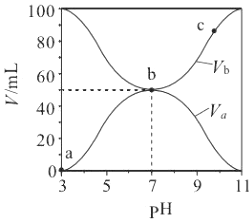

| A. | Ka(HA)的值与 Kb(BOH) 的值不相等 | |
| B. | b 点时,水电离出的 c(H+)=10-7mol/L | |
| C. | c 点时,c(A-)>c(B+) | |
| D. | a→c 过程中$\frac{c({A}^{-})}{c(O{H}^{-})•c(HA)}$不变 |
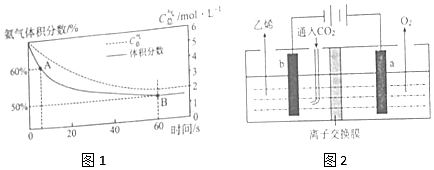
8.常温下,向1LpH=10的KOH溶液中持续通入CO2,与溶液中水电离出的c(OH-)与通入的CO2的体积(V)关系如图所示.下列叙述不正确的是( )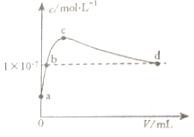

| A. | b点溶液呈中性 | |
| B. | d点溶液中:c(K+)=2c(CO32-)+c(HCO3-) | |
| C. | c点溶液中:2c(H2CO3)+c(H+)+c(HCO3-)=c(OH-) | |
| D. | a点溶液中:水电离出的c(H+)=1×10-10mol•L-1 |
7.常温下,向1L 0.1mol•L-1NH4Cl溶液中,不断加入固体NaOH后,NH4+与NH3•H2O的变化趋势如图所示(不考虑溶液体积的变化和氨的挥发),下列说法正确的是( )

| A. | M点溶液中水的电离程度比原溶液大 | |
| B. | a=0.05 | |
| C. | 当n(NaOH)=0.05mol时溶液中有:c(Cl-)>c(Na+)>c(NH4+)>c(OH-)>c(H+) | |
| D. | 在M点时,n(OH-)-n(H+)=(a-0.05)mol |
6.下列说法不正确的是( )
0 162358 162366 162372 162376 162382 162384 162388 162394 162396 162402 162408 162412 162414 162418 162424 162426 162432 162436 162438 162442 162444 162448 162450 162452 162453 162454 162456 162457 162458 162460 162462 162466 162468 162472 162474 162478 162484 162486 162492 162496 162498 162502 162508 162514 162516 162522 162526 162528 162534 162538 162544 162552 203614
| A. | 0.02 mol•L-1醋酸与0.02 mol•L-1NaOH等体积混合后的溶液中加少量的CH3COONa固体,则$\frac{c(C{H}_{3}CO{O}^{-})}{C(N{a}^{+})}$ 增大 | |
| B. | t℃时,恒容密闭容器中反应:NO2(g)+SO2(g)?NO(g)+SO3(g),通入少量O2,$\frac{c(NO)•c(S{O}_{3})}{c(N{O}_{2})•c(S{O}_{2})}$ 的值及SO2转化率不变 | |
| C. | 常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H>0 | |
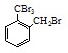
| D. | lmol该化合物( 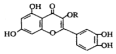 )与NaOH溶液作用消耗NaOH的物质的量以及与氢气加成所需的氢气的物质的量分别是4mol、8mol )与NaOH溶液作用消耗NaOH的物质的量以及与氢气加成所需的氢气的物质的量分别是4mol、8mol |




 ;
; ;
;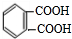 .
.