5.常温下,用浓度为0.1000mol/L的盐酸分别逐滴加入到20.00mL 0.1000mol/L的两种一元碱MOH、ROH溶液中,PH随盐酸溶液体积的变化如图所示.下列说法正确的是( )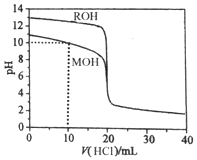

| A. | pH=10时,c(M+)>c(MOH)>c(Cl-)>c(OH-)>c(H+) | |
| B. | 将上述MOH、ROH溶液等体积混合后,用盐酸滴定至MOH恰好反应时:c(R+)>c(M+)>c(H+)>c(OH-) | |
| C. | 10mL<V(HCl)<20mL时,c(M+)+c(MOH)<c(Cl-) | |
| D. | V(HCl)>20mL时,不可能存在:c(Cl-)>c(M+)=c(H+)>c(OH-) |
3.食醋(主要成分CH3COOH)、纯碱(Na2CO3)和小苏打(NaHCO3)均为家庭厨房中常用的物质.己知:
请回答下列问题:
(1)25℃时,0.10mol•L-1Na2CO3溶液的pH=11,则溶液中由水电离出的c(OH-)=10-3
(2)常温下,将20mL0.10mol•L-1CH3COOH溶液和 20mL0.10mol•L-1HNO2 溶液分别与 20mL 0.10mol•L-1NaHCO3溶液混合(混合后溶液体积变化忽略不计).
①反应开始时,v (CH3COOH )<v (HNO2)(填“>”、“<”或“:”).
②充分反应后.两溶液中c(CH3COO-)< c(NO2-)(填“>”、“<”或“=”).
(3)25℃时,向CH3COOH溶液中加入一定量的NaHCO3,所得混合液的pH=6,则混合液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$=18;
(4)常温下,下列方法可以使0.1mol•L-1CH3COOH的电离程度增大的是bc.
a.加入少量的稀盐酸
b.加热溶液
c.加水稀释
d.加入少量冰醋酸.
| 弱酸 | CH3COOH | H2CO3 | HNO2 |
| 电离常数 | K=1.8×10-5 | K=4.3×10-7 K=5.6×10-11 | K=5.0×10-4 |
(1)25℃时,0.10mol•L-1Na2CO3溶液的pH=11,则溶液中由水电离出的c(OH-)=10-3
(2)常温下,将20mL0.10mol•L-1CH3COOH溶液和 20mL0.10mol•L-1HNO2 溶液分别与 20mL 0.10mol•L-1NaHCO3溶液混合(混合后溶液体积变化忽略不计).
①反应开始时,v (CH3COOH )<v (HNO2)(填“>”、“<”或“:”).
②充分反应后.两溶液中c(CH3COO-)< c(NO2-)(填“>”、“<”或“=”).
(3)25℃时,向CH3COOH溶液中加入一定量的NaHCO3,所得混合液的pH=6,则混合液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$=18;
(4)常温下,下列方法可以使0.1mol•L-1CH3COOH的电离程度增大的是bc.
a.加入少量的稀盐酸
b.加热溶液
c.加水稀释
d.加入少量冰醋酸.
2.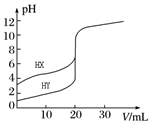 常温下,用0.10mol•L-1 NaOH溶液分别滴定20.00mL 0.10mol•L-1 的HX和HY溶液,滴定曲线如图所示.下列说法正确的是( )
常温下,用0.10mol•L-1 NaOH溶液分别滴定20.00mL 0.10mol•L-1 的HX和HY溶液,滴定曲线如图所示.下列说法正确的是( )
 常温下,用0.10mol•L-1 NaOH溶液分别滴定20.00mL 0.10mol•L-1 的HX和HY溶液,滴定曲线如图所示.下列说法正确的是( )
常温下,用0.10mol•L-1 NaOH溶液分别滴定20.00mL 0.10mol•L-1 的HX和HY溶液,滴定曲线如图所示.下列说法正确的是( )| A. | pH=7时,滴定HX消耗NaOH溶液体积等于20.00 mL | |
| B. | 将上述HX、HY溶液各加水稀释10倍,稀释后溶液的pH:pH(HY)>pH (HX) | |
| C. | 当NaOH溶液体积为20.00 mL时,HX溶液中离子浓度:c(Na+)>c(X-)>c(H+)>c(OH-) | |
| D. | 将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时,c(H+)+c(HX)=c(OH-) |
1.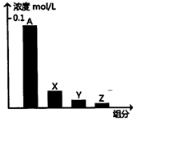 常温下,0.2mol/L的乙酸与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是( )
常温下,0.2mol/L的乙酸与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是( )
 常温下,0.2mol/L的乙酸与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是( )
常温下,0.2mol/L的乙酸与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是( )| A. | A可能表示Na+ | |
| B. | A可能表示乙酸分子 | |
| C. | 若图中A表示CH3COO-,可以证明乙酸是弱酸 | |
| D. | 该混合溶液中:c(A)+c(Y)=c(X)+c(Z) |
20.用中和滴定法测定某烧碱的纯度.
(1)配制待测液 将0.85g含有少量杂质(不与盐酸反应)的固体烧碱样品配制成100mL溶液,所用的主要仪器有烧杯、玻璃棒、100mL容量瓶、量筒、胶头滴管.
(2)滴定 ①盛装0.20mol/L盐酸标准液应该用酸式滴定管.
②滴定时,应先向锥形瓶中加酚酞作为指示剂;滴定过程中两眼应该注视锥形瓶内溶液的颜色变化和滴定速度,滴定终点时,锥形瓶中的溶液的颜色变化是C.(填编号)
A.由黄色变为红色 B.由黄色变为橙色 C.由浅红色变为无色 D.由无色变为红色
③有关数据记录如表:
(3)纯度计算 NaOH溶液的浓度为0.201mol/L,烧碱样品的纯度为94.6%
(4)对几种假定情况的讨论:(填无影响、偏高、偏低)
①若用蒸馏水冲洗锥形瓶,则会使测定的结果无影响
②若在滴定过程中不慎将数滴酸液滴在锥形瓶外,则会使测定结果偏高.
③若刚见到指示剂局部的颜色有变化就停止滴定,则会使测定结果偏低.
④读数时,若滴定前仰视,滴定后俯视,则会使测定结果偏低.
0 162357 162365 162371 162375 162381 162383 162387 162393 162395 162401 162407 162411 162413 162417 162423 162425 162431 162435 162437 162441 162443 162447 162449 162451 162452 162453 162455 162456 162457 162459 162461 162465 162467 162471 162473 162477 162483 162485 162491 162495 162497 162501 162507 162513 162515 162521 162525 162527 162533 162537 162543 162551 203614
(1)配制待测液 将0.85g含有少量杂质(不与盐酸反应)的固体烧碱样品配制成100mL溶液,所用的主要仪器有烧杯、玻璃棒、100mL容量瓶、量筒、胶头滴管.
(2)滴定 ①盛装0.20mol/L盐酸标准液应该用酸式滴定管.
②滴定时,应先向锥形瓶中加酚酞作为指示剂;滴定过程中两眼应该注视锥形瓶内溶液的颜色变化和滴定速度,滴定终点时,锥形瓶中的溶液的颜色变化是C.(填编号)
A.由黄色变为红色 B.由黄色变为橙色 C.由浅红色变为无色 D.由无色变为红色
③有关数据记录如表:
| 滴定序号 | 待测液体积(ml) | 所消耗盐酸标准液的体积(ml) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.50 | 20.70 |
| 2 | 20.00 | 6.00 | 26.00 |
(4)对几种假定情况的讨论:(填无影响、偏高、偏低)
①若用蒸馏水冲洗锥形瓶,则会使测定的结果无影响
②若在滴定过程中不慎将数滴酸液滴在锥形瓶外,则会使测定结果偏高.
③若刚见到指示剂局部的颜色有变化就停止滴定,则会使测定结果偏低.
④读数时,若滴定前仰视,滴定后俯视,则会使测定结果偏低.
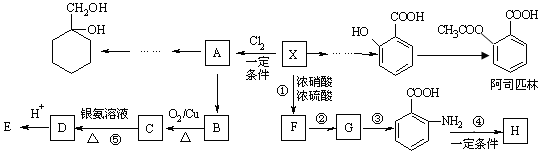

 ,反应①~⑤中属于取代反应的有①.
,反应①~⑤中属于取代反应的有①. .
.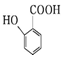 有多种同分异构体,请写出符合下列条件的同分异构体的结构简式
有多种同分异构体,请写出符合下列条件的同分异构体的结构简式 (或
(或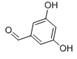 )(任写一种)
)(任写一种)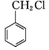 和其他无机试剂合成
和其他无机试剂合成 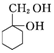 最合理的方案.
最合理的方案. 纯铜在工业上主要用来制造导线、电器元件等,铜能形成+1和+2的化合物.回答下列问题:
纯铜在工业上主要用来制造导线、电器元件等,铜能形成+1和+2的化合物.回答下列问题: 氟元素是电负性最大的非金属元素,且氟原子的半径小,因此氟单质极易和金属单质反应且把它们氧化到最高价态,如MnF7、VF5、CaF2等.氟元素还可以和氧元素形成氟化物,如OF2等.
氟元素是电负性最大的非金属元素,且氟原子的半径小,因此氟单质极易和金属单质反应且把它们氧化到最高价态,如MnF7、VF5、CaF2等.氟元素还可以和氧元素形成氟化物,如OF2等.