4.14C 常用于测定年代,关于其说法正确的是( )
| A. | 比 12C 多两个质子 | B. | 与 12C 化学性质相似 | ||
| C. | 与 12C 互为同素异形体 | D. | 质子数与中子数相等 |
2.设NA表示阿伏加徳罗常数的值.下列说法中不正确的是( )
| A. | 0.1mol-NH2(氨基)中所含有的电子数为0.9NA | |
| B. | lmol D218O所含的中子数为12NA | |
| C. | 14 g聚乙烯与聚丙烯的混合物中含H原子的数目为2NA | |
| D. | 一定条件下,0.2 mol SO2与足量O2充分反应,生成的SO3分子数为0.2NA |
20.NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 14g分子式为CnH2n的链烃中含有的C-H键的数目为2NA | |
| B. | 0.1molCl2与足量石灰乳反应,转移电子的数目为0.2NA | |
| C. | 室温下,l L pH=13的NaOH溶液中,由水电离出的OH-离子数目为0.1NA | |
| D. | 标准状况下,2.24 LNO2和N2O4混合气体中含有氧原子数目为0.2NA |
19.化学与生产、生活、社会密切相关,下列说法错误的是( )
| A. | 人造纤维、合成纤维和光导纤维都是有机高分子化合物 | |
| B. | 利用CO2合成聚碳酸酯类可降解塑料,有利于减少白色污染 | |
| C. | 黄河入海口沙洲的形成与用卤水点豆腐,都体现了胶体聚沉的性质 | |
| D. | 我国汽油标准由“国III”提高到“国1V”,目的是减少有害气体的排放,改善环境质量 |
16.下列脱水过程中不属于取代反应的是( )
①高级脂肪酸与甘油脱水形成油脂 ②乙醇在浓H2SO4作用下脱水制乙烯
③氨基酸在酶的作用下脱水形成二肽 ④葡萄糖在浓H2SO4作用下脱水成焦炭.
①高级脂肪酸与甘油脱水形成油脂 ②乙醇在浓H2SO4作用下脱水制乙烯
③氨基酸在酶的作用下脱水形成二肽 ④葡萄糖在浓H2SO4作用下脱水成焦炭.
| A. | ①② | B. | ①③ | C. | ②③ | D. | ②④ |
15.化学与生活、社会发展息息相关,下列有关说法不正确的是( )
0 162353 162361 162367 162371 162377 162379 162383 162389 162391 162397 162403 162407 162409 162413 162419 162421 162427 162431 162433 162437 162439 162443 162445 162447 162448 162449 162451 162452 162453 162455 162457 162461 162463 162467 162469 162473 162479 162481 162487 162491 162493 162497 162503 162509 162511 162517 162521 162523 162529 162533 162539 162547 203614
| A. | 海水淡化的方法有蒸馏法、电渗析法等 | |
| B. | “青蒿一握,以水二升渍,绞取汁”,屠呦呦提取青蒿素的过程中发生了化学变化 | |
| C. | “静电除尘”、“燃煤固硫”、“汽车尾气催化净化”都能提高空气质量 | |
| D. | 用CO2合成聚碳酸酯可降解塑料,实现“碳”的循环利用 |
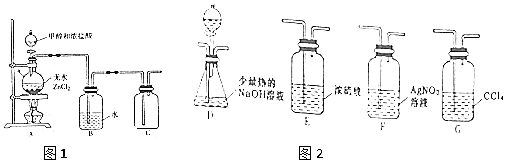
 无水MgBr2可用作催化剂.实验室采用镁屑与液溴为原料制备无水MgBr2,装置如图(夹持仪器略去),主要步骤如下:
无水MgBr2可用作催化剂.实验室采用镁屑与液溴为原料制备无水MgBr2,装置如图(夹持仪器略去),主要步骤如下: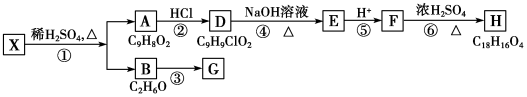
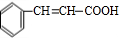 ,检验A中非含氧官能团所用的试剂为溴水或溴的四氯化碳溶液.
,检验A中非含氧官能团所用的试剂为溴水或溴的四氯化碳溶液.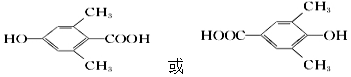 .
.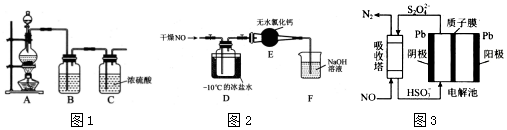
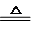 MnCl2+Cl2↑+H2O.装置B中盛放的试剂为饱和食盐水,其作用为除去氯气中的氯化氢气体.
MnCl2+Cl2↑+H2O.装置B中盛放的试剂为饱和食盐水,其作用为除去氯气中的氯化氢气体. .
.