20.下列溶液一定呈中性的是( )
| A. | PH=7的溶液 | |
| B. | 非电解质溶于水得到的溶液 | |
| C. | 由强酸和强碱等物质的量反应得到的物质 | |
| D. | c (H+)=c (OH-) |
19.下列实验操作中错误的是( )
| A. | 用规格为10 mL的量筒量取6mL的液体 | |
| B. | 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| C. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
18.向 10mL0.2mol/L 的氯化铝溶液中逐滴加入未知浓度的氢氧化钡溶液,测得加入15mL 和加入45mL 时,所得沉淀一样多.则原氢氧化钡溶液的浓度为( )
| A. | 0.03mol/L | B. | 0.16mol/L | C. | 0.08mol/L | D. | 0.04mol/L |
17.镁铝合金4.08g溶于250mL2mol/L的盐酸中,标准状况下放出气体的体积为4.48L,向反应后的溶液中加入500mLNaOH溶液,充分反应后最终产生白色沉淀.下列有关说法不正确的是( )
| A. | 4.08g镁铝合金中含有镁和铝的质量分别为1.92g、2.16g | |
| B. | 生成沉淀的最大质量为10.88g | |
| C. | 若白色沉淀只有Mg(OH)2,该NaOH溶液的浓度至少为0.96mol/L | |
| D. | 溶解4.08 g镁铝合金时,剩余盐酸的物质的量为0.1 mol |
16.现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ③碘水溶液,分离以上各混合液的正确方法依次是( )
| A. | 分液、萃取、蒸馏 | B. | 萃取、蒸馏、分液 | C. | 分液、蒸馏、萃取 | D. | 蒸馏、萃取、分液 |
15.五种主族元素在周期表中的位置如表所示.L的单质在常温常压下呈液态,且保存时需要用水液封.下列推断正确的是( )
| X | Y | Z | T | |
| L |
| A. | 原子半径:X<Y<Z<T<L | |
| B. | 气态氢化物的还原性:L>Z>T | |
| C. | 含x的两种盐溶液混合可能生成沉淀 | |
| D. | Y的含氧酸的酸性小于T的含氧酸 |
14.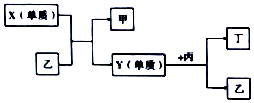 现有W、X、Y、Z四种短周期元素,W分别与X、Y、Z结合生成甲、乙、丙三种化合物,且甲、乙、丙均为10电子的分子.Y、Z结合生成化合物丁.有关元素的单质和甲、乙、丙、丁四种化合物的转化关系如图,下列说法正确的是( )
现有W、X、Y、Z四种短周期元素,W分别与X、Y、Z结合生成甲、乙、丙三种化合物,且甲、乙、丙均为10电子的分子.Y、Z结合生成化合物丁.有关元素的单质和甲、乙、丙、丁四种化合物的转化关系如图,下列说法正确的是( )
 现有W、X、Y、Z四种短周期元素,W分别与X、Y、Z结合生成甲、乙、丙三种化合物,且甲、乙、丙均为10电子的分子.Y、Z结合生成化合物丁.有关元素的单质和甲、乙、丙、丁四种化合物的转化关系如图,下列说法正确的是( )
现有W、X、Y、Z四种短周期元素,W分别与X、Y、Z结合生成甲、乙、丙三种化合物,且甲、乙、丙均为10电子的分子.Y、Z结合生成化合物丁.有关元素的单质和甲、乙、丙、丁四种化合物的转化关系如图,下列说法正确的是( )| A. | 原子半径的大小:W<Y<Z<X | B. | 单质与H2化合的难易程度:X>Y | ||
| C. | 甲与丙反应不可能生成离子化合物 | D. | Z的最高价氧化物的水化物为强酸 |
13.在①、②、③容积不等的恒容密闭容器中,均充入0.lmol CO和0.2mol H2,在催化剂的作用下发生反应:CO(g)+2H2(g)?CH3OH(g).测得三个容器中平衡混合物中CH3OH的体积分数随温度的变化如图所示:下列说法正确的是( )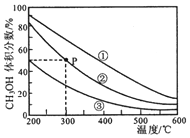

| A. | 该反应的正反应为放热反应 | |
| B. | 三个容器容积:①>②>③ | |
| C. | 在P点,CO转化率为75% | |
| D. | 在P点,向容器②中再充入CO、H2 及 CH3OH 各 0.025mol,此时 v(CO)正<v (CO)逆 |
12.下列指定微粒的个数比等于2:1的是( )
0 162336 162344 162350 162354 162360 162362 162366 162372 162374 162380 162386 162390 162392 162396 162402 162404 162410 162414 162416 162420 162422 162426 162428 162430 162431 162432 162434 162435 162436 162438 162440 162444 162446 162450 162452 162456 162462 162464 162470 162474 162476 162480 162486 162492 162494 162500 162504 162506 162512 162516 162522 162530 203614
| A. | ${\;}_{1}^{2}$H原子中的中子数和质子数 | |
| B. | ${\;}_{18}^{36}$Ar原子中的质量数与中子数 | |
| C. | ${\;}_{4}^{8}$Be2+中的质子数和电子数 | |
| D. | ${\;}_{12}^{26}$Mg2+中的中子数和电子数 |