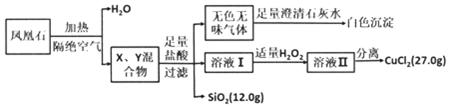
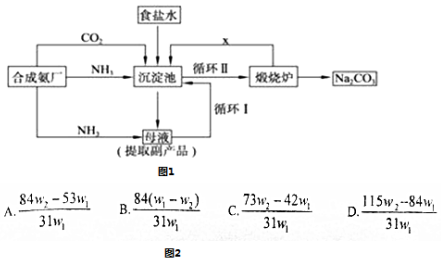
20.关于某溶液中所含物质的鉴别,下列判断正确的是( )
| A. | 加入Ca(OH)2溶液,有白色沉淀生成,则溶液中一定存在CO32- | |
| B. | 加入Ba(NO3)2 溶液,生成白色沉淀,加入稀盐酸后沉淀不溶解时,可确定有SO42-存在 | |
| C. | 加入CCl4,振荡,静置,下层溶液呈紫色,则原溶液中存在碘单质 | |
| D. | 加入AgNO3溶液,生成白色沉淀,加入稀盐酸沉淀不溶解时,可确定有Cl-存在 |
19.下列关于溶液和胶体的叙述,正确的是( )
| A. | “血液透析”利用了胶体的性质 | |
| B. | 溶液是电中性的,胶体是带电的 | |
| C. | 一束光线分别通过溶液和胶体时,前者会出现明显的光带,后者则没有 | |
| D. | 浓NaOH溶液中滴加FeCl3饱和溶液可制得Fe(OH)3胶体 |
18.如图是a、b两种固体物质的溶解度曲线,下列说法中正确的是( )
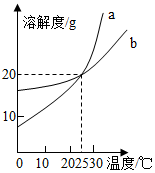

| A. | a的溶解度大于b的溶解度 | |
| B. | 在20℃时,a、b的溶液中溶质的质量分数相同 | |
| C. | b的溶解度都随温度升高而增大 | |
| D. | b都属于易溶物质 |
15.O3在水中易分解生成O2,一定条件下,O3的浓度减少一半所需的时间(t)如下表所示.已知:O3的起始浓度为0.02mol•L-1.
(1)pH增大能加速(填“加速”或“减缓”)O3分解,其中对O3分解起催化作用的是OH-(填“OH-”或“H+”).
(2)在30℃、pH=5.0条件下,O3的分解速率为2.00×10-4 mol•L-1•min-1,O2的浓度为0.015mol/L.
(3)据表中的递变规律,推测O3在下列条件下分解速率的关系:Ⅰ<(填“>”“<”或“=”)Ⅱ.
Ⅰ.40℃,pH=3.0
Ⅱ.30℃,pH=7.0.
| pH t/min T/℃ | 3.0 | 4.0 | 5.0 | 6.0 |
| 20 | 300 | 230 | 169 | 58 |
| 30 | 158 | 108 | 50 | 15 |
| 50 | 31 | 26 | 15 | 7 |
(2)在30℃、pH=5.0条件下,O3的分解速率为2.00×10-4 mol•L-1•min-1,O2的浓度为0.015mol/L.
(3)据表中的递变规律,推测O3在下列条件下分解速率的关系:Ⅰ<(填“>”“<”或“=”)Ⅱ.
Ⅰ.40℃,pH=3.0
Ⅱ.30℃,pH=7.0.
14.已知反应2N2O5(g)?4NO2(g)+O2(g)的分解速率表达式为v正=k正.cm(N2O5),k正是与温度有关的常数,340K时实验测得的有关数据如下:
请回答下列问题:
(1)该速率表达式中,m=1,k正=0.35min-1.
(2)若某时刻c(N2O5)=0.100mol•L-1,则v正≈0.035mol.L-1.min-1.
(3)第4min时,该可逆反应v正≥(填“>”“<”或“=”或“≥”)v逆.
| t/min | 1 | 2 | 3 | 4 |
| c(N2O5)/mol.L-1 | 0.133 | 0.080 | 0.057 | 0.040 |
| v正/mol.L-1.min-1 | 0.0466 | 0.028 | 0.020 | 0.014 |
(1)该速率表达式中,m=1,k正=0.35min-1.
(2)若某时刻c(N2O5)=0.100mol•L-1,则v正≈0.035mol.L-1.min-1.
(3)第4min时,该可逆反应v正≥(填“>”“<”或“=”或“≥”)v逆.
12.设NA表示阿伏加德罗常数,下列叙述正确的是( )
0 162316 162324 162330 162334 162340 162342 162346 162352 162354 162360 162366 162370 162372 162376 162382 162384 162390 162394 162396 162400 162402 162406 162408 162410 162411 162412 162414 162415 162416 162418 162420 162424 162426 162430 162432 162436 162442 162444 162450 162454 162456 162460 162466 162472 162474 162480 162484 162486 162492 162496 162502 162510 203614
| A. | 0.5 mol O2含氧原子数为0.5NA | B. | 1.8 g的NH4+中含有的电子数为NA | ||
| C. | 48 g O3含有的氧原子数为NA | D. | 1 mol H2O2中含NA个H2和NA个O2 |