10.设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 22.4 L乙烷分子中的碳原子数目为2NA | |
| B. | 高温下,0.2 mol Fe与足量水蒸气反应,生成的H2分子数目为0.3 NA | |
| C. | 含NA个Na+的Na2O溶解于1 L水中,Na+的物质的量浓度为1 mol/L | |
| D. | 5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$2HNO3+4N2↑+9H2O反应中,生成28 g N2时,转移的电子数目为3.75NA |
9.下列有关物质相互转化的说法正确的是( )
| A. | 石墨转变成碳纳米管为物理变化 | |
| B. | “滴水石穿,绳锯木断”不包含化学变化 | |
| C. | 232Th转化为233U是化学变化 | |
| D. | 将地沟油制成肥皂是化学变化 |
7.下面关于电解质的叙述中错误的是( )
| A. | 在水溶液中或熔融状态下均不导电的化合物叫非电解质 | |
| B. | 电解质、非电解质都指化合物而言,单质不属于此范畴 | |
| C. | 电解质在水中一定能导电,在水中导电的化合物一定是电解质 | |
| D. | 纯水的导电性很差,所以水不是电解质 |
6.在一定温度下,向饱和的烧碱溶液中放入一定量的过氧化钠,充分反应后恢复到原温度,下列说法正确的是( )
| A. | 溶液中有晶体析出,Na+数目不变 | |
| B. | 溶液中的OH- 物质的量浓度不变,有O2放出 | |
| C. | 溶质的质量分数增大 | |
| D. | 溶液中NaOH的浓度减小,有O2放出 |
4.恒定温度下,在固定容积的器皿中,反应2NO2(g)?N2O4(g)达到平衡后,再向容器内通入一定量NO2,又达到平衡时,NO2的转化率( )
| A. | 不变 | B. | 增大 | C. | 减小 | D. | 无法判断 |
3.下列说法正确的是( )
| A. | 标准状况下,22.4L水的物质的量为1摩尔 | |
| B. | 常温常压下,32g O3气体物质的量为1摩尔 | |
| C. | 标准状况下,a L的氧气和氮气的混合物含有的分子数约为$\frac{a}{22.4}$×6.02×1023 | |
| D. | 2.24L CO2中含有的原子数为0.3×6.02×1023 |
2.实验中的下列操作正确的是( )
| A. | 用试管取出试剂瓶中的Na2CO3溶液,发现取量过多,为不浪费,又把过量的试剂倒入试剂瓶中 | |
| B. | 用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中 | |
| C. | 用蒸发方法使NaCl从溶液中析出时,应将蒸发皿中NaCl 溶液全部加热蒸干 | |
| D. | Ba(NO3)2溶于水,可将含有Ba(NO3)2的废液倒入水槽中,再用水冲入下水道 |
1.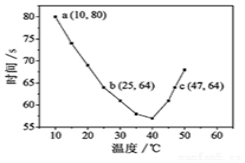 NaHSO3溶液在不同温度下均可被过量KIO3氧化,当NaHSO3完全消耗即有I2析出,根据I2析出所需时间可以求得NaHSO3的反应速率.将浓度均为0.020mol•L-1NaHSO3(含少量淀粉)10.0ml、KIO3(过量)酸性溶液40.0ml混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如图.据图分析,下列判断不正确的是( )
NaHSO3溶液在不同温度下均可被过量KIO3氧化,当NaHSO3完全消耗即有I2析出,根据I2析出所需时间可以求得NaHSO3的反应速率.将浓度均为0.020mol•L-1NaHSO3(含少量淀粉)10.0ml、KIO3(过量)酸性溶液40.0ml混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如图.据图分析,下列判断不正确的是( )
0 162307 162315 162321 162325 162331 162333 162337 162343 162345 162351 162357 162361 162363 162367 162373 162375 162381 162385 162387 162391 162393 162397 162399 162401 162402 162403 162405 162406 162407 162409 162411 162415 162417 162421 162423 162427 162433 162435 162441 162445 162447 162451 162457 162463 162465 162471 162475 162477 162483 162487 162493 162501 203614
 NaHSO3溶液在不同温度下均可被过量KIO3氧化,当NaHSO3完全消耗即有I2析出,根据I2析出所需时间可以求得NaHSO3的反应速率.将浓度均为0.020mol•L-1NaHSO3(含少量淀粉)10.0ml、KIO3(过量)酸性溶液40.0ml混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如图.据图分析,下列判断不正确的是( )
NaHSO3溶液在不同温度下均可被过量KIO3氧化,当NaHSO3完全消耗即有I2析出,根据I2析出所需时间可以求得NaHSO3的反应速率.将浓度均为0.020mol•L-1NaHSO3(含少量淀粉)10.0ml、KIO3(过量)酸性溶液40.0ml混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如图.据图分析,下列判断不正确的是( )| A. | 40℃之前与40℃之后溶液变蓝的时间随温度的变化趋势相反 | |
| B. | 不能比较图中b、c两点对应的NaHSO3反应速率的大小 | |
| C. | 图中b点对应的NaHSO3反应速率为3.125×10-4mol•L-1•s-1 | |
| D. | 温度高于40℃时,淀粉不宜用作该试验的指示剂 |