7.表是稀硫酸与某金属反应的实验数据:
分析上述数据,回答下列问题:
(1)实验4和5表明,固体反应物的表面积对反应速率有影响,接触面积越大反应速率越快,能表明同一规律的实验还有1和2(填实验序号);
(2)本实验中影响反应速率的其他因素还有温度和硫酸的浓度.
(3)实验中的所有反应,反应前后溶液的温度变化值相近约为15℃,推测未测数据可能为45℃,分析△t相近的原因金属的质量和硫酸的用量均相等,且与硫酸反应完全,能量的变化相同.
(4)经仔细辨认,数据模糊为25、35、125、250,则数据模糊A、B、C分别为250、25、125.
| 实验序号 | 金属 质量/g | 金属状态 | C(H2SO4) /mol•L-1 | V(H2SO4) /mL | 溶液温度/℃ | 金属消失的时间/s | |
| 反应前 | 反应后 | ||||||
| 1 | 0.10 | 丝 | 0.5 | 50 | 20 | 34 | 500 |
| 2 | 0.10 | 粉末 | 0.5 | 50 | 20 | 35 | 50 |
| 3 | 0.10 | 丝 | 0.7 | 50 | 20 | 36 | 数据模糊A |
| 4 | 0.10 | 丝 | 0.8 | 50 | 20 | 35 | 200 |
| 5 | 0.10 | 粉末 | 0.8 | 50 | 20 | 35 | 数据模糊B |
| 6 | 0.10 | 丝 | 1.0 | 50 | 20 | 35 | 数据模糊C |
| 7 | 0.10 | 丝 | 1.0 | 50 | 数据模糊D | 50 | 50 |
| 8 | 0.10 | 丝 | 1.1 | 50 | 20 | 34 | 100 |
| 9 | 0.10 | 丝 | 1.1 | 50 | 30 | 未测数据 | 40 |
(1)实验4和5表明,固体反应物的表面积对反应速率有影响,接触面积越大反应速率越快,能表明同一规律的实验还有1和2(填实验序号);
(2)本实验中影响反应速率的其他因素还有温度和硫酸的浓度.
(3)实验中的所有反应,反应前后溶液的温度变化值相近约为15℃,推测未测数据可能为45℃,分析△t相近的原因金属的质量和硫酸的用量均相等,且与硫酸反应完全,能量的变化相同.
(4)经仔细辨认,数据模糊为25、35、125、250,则数据模糊A、B、C分别为250、25、125.
6.提纯下列物质除去其中的杂质(括号中为杂质),所用试剂和方法一定正确的是( )
| A. | H2SO4(HCl):AgNO3溶液、过滤 | B. | KNO3(K2SO4):Ba(NO3)2溶液、过滤 | ||
| C. | Cu(CuO):盐酸、过滤 | D. | CaCO3(CaO):加一些水、过滤 |
5.以硫铁矿为原料生产硫酸所得的酸性废水中砷元素含量极高,为控制砷的排放,采用化学沉降法处理含砷废水,相关数据如下表,若混合溶液中Ca2+、Al3+、Fe3+的浓度均为1.0×10-3mol•L-1,c(AsO43-)最大是( )
| 难溶物 | Ksp |
| Ca3(AsO4)2 | 6.8×10-19 |
| AlAsO4 | 1.6×10-16 |
| FeAsO4 | 5.7×10-21 |
| A. | 5.7×10-18 mol•L-1 | B. | 2.6×10-5mol•L-1 | ||
| C. | 1.6×10-13mol•L-1 | D. | 5.7×10-24mol•L-1 |
4.下列不能说明化学具有创造性和实用性的是( )
| A. | 化学家哈伯用催化法合成氨后,就能生产硝酸铵 | |
| B. | 化学家合成碳纳米管,用作分子导线和超小型电子器件 | |
| C. | 俄国科学家门捷列夫发现元素周期律 | |
| D. | 诺贝尔用硝化甘油制成了炸药,并用于工业生产 |
1.在体积为2L的密闭容器中,充入6mol N2,10mol H2,发生反应:N2(g)+3H2(g)?2NH3(g)反应进行5min时,测得NH3的浓度为1mol•L-1,在此时间内,下列反应速率表示正确的是( )
| A. | v(NH3)=0.1mol•L-1•min-1 | B. | v(N2)=0.7 mol•L-1•min-1 | ||
| C. | v(NH3)=0.2mol•L-1•min-1 | D. | v(H2)=0.3mol•L-1•min-1 |
20.海水中含有丰富的镁资源.某同学设计了从模拟海水中制备MgO的实验方案:
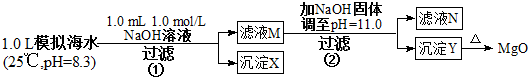
注:溶液中某种离子的浓度小于1.0×10-5 mol/L,可认为该离子不存在;
实验过程中,假设溶液体积不变.
已知:Ksp(CaCO3)=4.96×10-9;Ksp(MgCO3)=6.82×10-6;
Ksp[Ca(OH)2]=4.68×10-6;Ksp[Mg(OH)2]=5.61×10-12.
下列说法正确的是( )
0 162254 162262 162268 162272 162278 162280 162284 162290 162292 162298 162304 162308 162310 162314 162320 162322 162328 162332 162334 162338 162340 162344 162346 162348 162349 162350 162352 162353 162354 162356 162358 162362 162364 162368 162370 162374 162380 162382 162388 162392 162394 162398 162404 162410 162412 162418 162422 162424 162430 162434 162440 162448 203614

| 海水中的离子浓度(mol/L) | Na+ | Mg2+ | Ca2+ | Cl- | HCO3 |
| 0.439 | 0.050 | 0.011 | 0.560 | 0.001 |
实验过程中,假设溶液体积不变.
已知:Ksp(CaCO3)=4.96×10-9;Ksp(MgCO3)=6.82×10-6;
Ksp[Ca(OH)2]=4.68×10-6;Ksp[Mg(OH)2]=5.61×10-12.
下列说法正确的是( )
| A. | 沉淀物X为CaCO3,MgCO3 | |
| B. | 滤液M中存在Mg2+,不存在Ca2+ | |
| C. | 滤液N中存在Mg2+、Ca2+ | |
| D. | 步骤②中若改为加入8 g NaOH固体,沉淀物Y为Ca(OH)2和Mg(OH)2的混合物 |

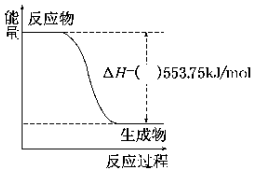 广州亚运会“潮流”火炬采用具有广州民间特色的象牙雕镂空工艺,以水的和谐与火的激情交相凝聚为理念,寄托了亚洲人民共同推进和平与发展的期望.火炬内熊熊大火来源于丙烷的燃烧,丙烷是一种优良的燃料.试回答下列问题:
广州亚运会“潮流”火炬采用具有广州民间特色的象牙雕镂空工艺,以水的和谐与火的激情交相凝聚为理念,寄托了亚洲人民共同推进和平与发展的期望.火炬内熊熊大火来源于丙烷的燃烧,丙烷是一种优良的燃料.试回答下列问题: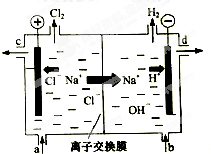 氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品.如图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过.
氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品.如图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过.