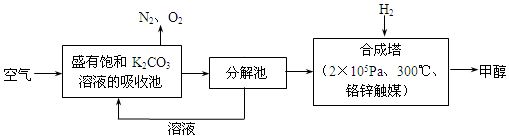
4.生活中处处有化学,下列说法不正确的是( )
| A. | 铁表面镀锌可增强其抗腐蚀性 | |
| B. | 为防止月饼等富脂食品氧化变质,常在包装袋中放入生石灰 | |
| C. | “青蒿一握,以水二升渍,绞取汁”,上述对青篙素的提取过程属于物理变化 | |
| D. | 含重金属离子的电镀废液不能随意排放 |
3.下列实验中,对应的现象以及结论都正确且两者具有因果关系的是( )
| 选项 | 实验 | 现象 | 结论 |
| A | 将滴有酚酞的0.1mol•L-1氨水系稀释成0.01mol•L-1 | 溶液颜色变浅 | 稀释后NH3•H2O的电离程度减小 |
| B | 将铜粉加入1.0mol•L-1Fe2(SO4)3溶液中 | 溶液变蓝、有黑色固体出现 | 金属铁比铜活泼 |
| C | 用溴乙烷与NaOH乙醇溶液共热产生的气体通入酸性KMnO4溶液中 | 溶液褪色 | 产生的气体为乙烯 |
| D | 向1mL0.1mol•L-1 MgSO4溶液滴入2滴等浓度的NaOH溶液,片刻后再滴加2滴0.1mol•L-1 CuSO4溶液 | 先有白色沉淀生成,后变为蓝色沉淀 | Cu(OH)2的溶度积常数比Mg(OH)2的小 |
| A. | A | B. | B | C. | C | D. | D |
2.由硫铁矿烧渣(主要成分:Fe3O4、Fe2O3和FeO)得到绿矾(主FeSO4•7H2O),再通过绿矾制备铁黄[FeO(OH)]的流程如下:烧渣$→_{①}^{酸液}$$→_{②}^{FeS_{2}}$溶液$\stackrel{③}{→}$绿矾$→_{④}^{氨水/空气}$铁黄
已知:FeS2和铁黄均难溶于水下列说法不正确的是( )
已知:FeS2和铁黄均难溶于水下列说法不正确的是( )
| A. | 步骤①,最好用硫酸来溶解烧渣 | |
| B. | 步骤②,涉及的离子反应为FeS2+14Fe3++8H2O═15Fe2++2SO42-+16H+ | |
| C. | 步骤③,将溶液加热到有较多固体析出,再用余热将液体蒸干,可得纯净绿矾 | |
| D. | 步骤④,反应条件控制不当会使铁黄中混有Fe(OH)3 |
1.硫酰氯(SO2Cl2)常作氯化剂或氯磺化剂,用于制作药品、染料、表面活性剂等.其部分性质如下表:
回答下列问题:
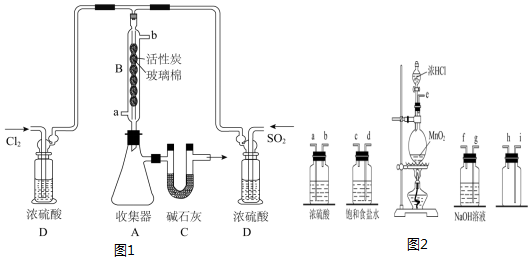
I.实验室合成硫酰氯需要先制取干燥氯气,制备干燥纯净的氯气所用仪器如图1:
(1)上述仪器的连接顺序是:e接d,c接a,b接i,h接j(按气流方向,用小写字母表示).
II.催化合成硫酰氯的实验装置如图 2(夹持仪器已省略):
(2)仪器B冷却水的进口为a(填“a””或“b”),活性炭的作用是催化剂.
(3)装置D除干燥气体外,另一作用是通过观察气泡控制气体流速.若缺少D,则硫酰氯会水解,该反应的化学方程式为SO2Cl2+2H2O═H2SO4+2HCl.
(4)某同学建议将收集器A放在冰水中冷却,你认为该同学的建议是否合理,为什么?合理,防止硫酰氯分解
(5)C处U形管中碱石灰的作用是吸收多余二氧化硫、氯气,防止污染;防止水蒸气进入收集器使产品水解.
III.在氯磺酸中加入四氯化锡加热煮沸,使氯磺酸分解,可用于制取少量硫酰氯.化学方程式为:2ClSO3H$\frac{\underline{催化剂}}{△}$H2SO4+SO2Cl2,此法得到的产品中混有硫酸.
(6)①从分解产物中分离出硫酰氯的方法是蒸馏.
②请设计实验方案检验产品中硫酸的存在(可选试剂:稀盐酸、稀硝酸、BaCl2溶液、蒸馏水、石蕊溶液):
取适量产品充分加热后加水稀释,分成两份,一份滴加紫色石蕊试液变红,另一份加入BaCl2溶液产生白色沉淀,说明含有H2SO4.
| 物质 | 熔点/℃ | 沸点/℃ | 其它性质 |
| SO2Cl2 | -54.1 | 69.1 | ①易水解产生大量白雾 ②易分解:SO2Cl2$\frac{\underline{\;△\;}}{\;}$SO2↑+Cl2↑ |

I.实验室合成硫酰氯需要先制取干燥氯气,制备干燥纯净的氯气所用仪器如图1:
(1)上述仪器的连接顺序是:e接d,c接a,b接i,h接j(按气流方向,用小写字母表示).
II.催化合成硫酰氯的实验装置如图 2(夹持仪器已省略):
(2)仪器B冷却水的进口为a(填“a””或“b”),活性炭的作用是催化剂.
(3)装置D除干燥气体外,另一作用是通过观察气泡控制气体流速.若缺少D,则硫酰氯会水解,该反应的化学方程式为SO2Cl2+2H2O═H2SO4+2HCl.
(4)某同学建议将收集器A放在冰水中冷却,你认为该同学的建议是否合理,为什么?合理,防止硫酰氯分解
(5)C处U形管中碱石灰的作用是吸收多余二氧化硫、氯气,防止污染;防止水蒸气进入收集器使产品水解.
III.在氯磺酸中加入四氯化锡加热煮沸,使氯磺酸分解,可用于制取少量硫酰氯.化学方程式为:2ClSO3H$\frac{\underline{催化剂}}{△}$H2SO4+SO2Cl2,此法得到的产品中混有硫酸.
(6)①从分解产物中分离出硫酰氯的方法是蒸馏.
②请设计实验方案检验产品中硫酸的存在(可选试剂:稀盐酸、稀硝酸、BaCl2溶液、蒸馏水、石蕊溶液):
取适量产品充分加热后加水稀释,分成两份,一份滴加紫色石蕊试液变红,另一份加入BaCl2溶液产生白色沉淀,说明含有H2SO4.
19.下列说法正确的是( )
| A. | 某烷烃的命名为:2-甲基-3-乙基丁烷 | |
| B. | 分子式为 C4H8O2的酯有 4 种 | |
| C. | 乙烯分别使溴水和酸性 KMnO4 溶液褪色,反应类型相同 | |
| D. | 油脂是能发生水解反应的高分子化合物 |
18.化学与生活、生产、环境密切相关. 下列说法不正确的是( )
| A. | 工厂排放 CO2会导致酸雨的形成 | |
| B. | 使用含有氯化钙的融雪剂会加速桥梁的腐蚀 | |
| C. | “山东疫苗案”涉及疫苗未冷藏储运而失效,这与蛋白质变性有关 | |
| D. | 《黄白第十六》中有“曾青涂铁,铁赤如铜”,这与化学变化有关 |
17.已知苏糖的结构简式为: 有关苏糖的说法不正确的是( )
有关苏糖的说法不正确的是( )
 有关苏糖的说法不正确的是( )
有关苏糖的说法不正确的是( )| A. | 苏糖能发生银镜反应 | |
| B. | 苏糖属于单糖 | |
| C. | 苏糖在一定条件下,能发生加成和取代反应 | |
| D. | 苏糖与葡萄糖互为同分异构体 |
16.分子式为C5H12O,能发生催化氧化生成醛,符合此要求的醇的种类为( )
| A. | 3种 | B. | 4 种 | C. | 5 种 | D. | 8种 |
15.原子晶体中可能存在的化学键是( )
0 162223 162231 162237 162241 162247 162249 162253 162259 162261 162267 162273 162277 162279 162283 162289 162291 162297 162301 162303 162307 162309 162313 162315 162317 162318 162319 162321 162322 162323 162325 162327 162331 162333 162337 162339 162343 162349 162351 162357 162361 162363 162367 162373 162379 162381 162387 162391 162393 162399 162403 162409 162417 203614
| A. | 离子键 | B. | 氢键 | C. | 极性键 | D. | 金属键 |