12.将一定量的镁和铜组成的混合物加入到稀硝酸中,金属恰好完全溶解(假设反应中还原产物只有NO).向反应后的溶液中加入3mol/L NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加 5.1g.下列叙述不正确的是( )
| A. | 当金属全部溶解时,参加反应的硝酸的物质的量一定是0.4 mol | |
| B. | 参加反应的金属的总质量 3.6 g<m<9.6 g | |
| C. | 当生成的沉淀量达到最大时,消耗NaOH溶液的体积V=200 mL | |
| D. | 当金属全部溶解时收集到NO气体的体积在标况下为 2.24 L |
10.下列离子方程式中能表示多个化学反应的是( )
①Fe+Cu2+═Fe2++Cu ②Ba2++OH-+H++SO42-═BaSO4↓+H2O
③Ba2++OH-+H++SO42-═BaSO4↓+2H2O ④Cl2+H2O═H+Cl-+HClO
⑤CO32-+2H+═CO2+H2O ⑥Ag++Cl-═AgCl↓
①Fe+Cu2+═Fe2++Cu ②Ba2++OH-+H++SO42-═BaSO4↓+H2O
③Ba2++OH-+H++SO42-═BaSO4↓+2H2O ④Cl2+H2O═H+Cl-+HClO
⑤CO32-+2H+═CO2+H2O ⑥Ag++Cl-═AgCl↓
| A. | ①②⑤⑥ | B. | ①②③⑤⑥ | C. | ③④ | D. | 只有④ |
9.下列说法中正确的一组是( )
| A. |  互为同分异构体 互为同分异构体 | |
| B. |  与 与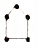 两种烃互为同系物 两种烃互为同系物 | |
| C. | 甲苯与溴蒸汽的反应产物受反应条件的影响而不同 | |
| D. | H2和D2互为同位素 |
8.如图,将铁棒(Fe)和石墨棒(C)插入盛有饱和NaCl溶液的U型管中,下列分析正确的是( ) 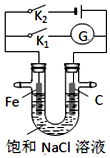

| A. | K1闭合,石墨棒周围溶液pH逐渐升高 | |
| B. | K1闭合,铁棒上发生的反应为2H++2e→H2↑ | |
| C. | K2闭合,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法 | |
| D. | K2闭合,电路中通过0.002 NA个电子时,两极共产生0.001 mol气体 |
4.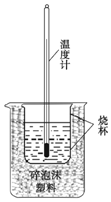 实验室利用如图装置进行中和热的测定. 回答下列问题:
实验室利用如图装置进行中和热的测定. 回答下列问题:
(1)该图中有两处未画出,它们是环形玻璃搅拌棒和烧杯上方盖硬纸板.
(2)把温度为13℃,浓度为1.0mol•L-1的盐酸和1.1mol•L-1的碱溶液 各 50mL混合,轻轻搅动,测得酸碱混合液的温度变化数据如表:
则a>b(填“>”“<”“=”);实验中碱液过量的目的是使盐酸充分反应,提高实验的准确度.已知:稀溶液的密度近似为1g/mL,其比热容约为4.18J/(g•℃),则a=56.8.
0 162192 162200 162206 162210 162216 162218 162222 162228 162230 162236 162242 162246 162248 162252 162258 162260 162266 162270 162272 162276 162278 162282 162284 162286 162287 162288 162290 162291 162292 162294 162296 162300 162302 162306 162308 162312 162318 162320 162326 162330 162332 162336 162342 162348 162350 162356 162360 162362 162368 162372 162378 162386 203614
 实验室利用如图装置进行中和热的测定. 回答下列问题:
实验室利用如图装置进行中和热的测定. 回答下列问题:(1)该图中有两处未画出,它们是环形玻璃搅拌棒和烧杯上方盖硬纸板.
(2)把温度为13℃,浓度为1.0mol•L-1的盐酸和1.1mol•L-1的碱溶液 各 50mL混合,轻轻搅动,测得酸碱混合液的温度变化数据如表:
| 反应物 | 起始温度(℃) | 终了温度(℃) | 中和热(kJ•mol-1) |
| ①HCl+NaOH | 13 | 19.8 | -a |
| ②HCl+NH3•H2O | 13 | 19.3 | -b |
 根据已学物质结构与性质的有关知识,回答下列问题:
根据已学物质结构与性质的有关知识,回答下列问题: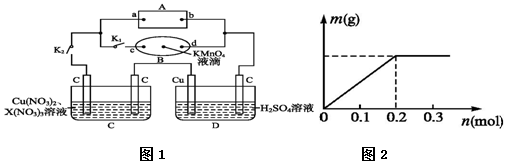
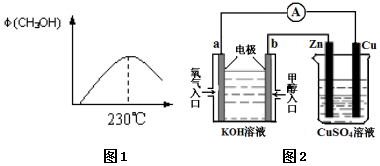 能源问题是人类社会面临的重大课题,甲醇是未来重要的能源物质之一.
能源问题是人类社会面临的重大课题,甲醇是未来重要的能源物质之一.