7.下表是部分城市某日空气质量日报:
(1)由上表可知,空气质量日报中涉及的污染物主要是SO2、NO2和可吸入颗粒物(PM10);四座城市中,最容易出现酸雨的城市是A.
(2)汽车尾气则是城市大气中氮氧化物的主要来源之一.治理方法之一是在汽车排气管上加装“催化转化器”,使CO与NOx反应生成可参与大气生态环境循环的无毒气体,这些无毒气体是CO2、N2.
(3)SO2的排放是造成酸雨的主要因素.
①若用足量的氢氧化钠溶液吸收含二氧化硫的工业废气,写出该反应的化学反应方程式2NaOH+SO2=Na2SO3+H2O.
②若将含二氧化硫的废气通入水中,在一段时间内连续不断测定溶液的pH值,发现pH值变小,这是由于空气中的氧气也参与了相关反应,表示该变化的化学方程式是2H2SO3+O2=2H2SO4.
| 城市 | 污染指数 | 首要污染物 | 空气质量等级 | ||
| SO2 | NO2 | PM10 | |||
| A | 98 | 23 | 67 | SO2 | Ⅱ |
| B | 47 | 29 | 35 | SO2 | Ⅰ |
| C | 62 | 80 | 113 | PM10 | Ⅲ |
| D | 52 | 76 | 59 | NO2 | Ⅰ |
(2)汽车尾气则是城市大气中氮氧化物的主要来源之一.治理方法之一是在汽车排气管上加装“催化转化器”,使CO与NOx反应生成可参与大气生态环境循环的无毒气体,这些无毒气体是CO2、N2.
(3)SO2的排放是造成酸雨的主要因素.
①若用足量的氢氧化钠溶液吸收含二氧化硫的工业废气,写出该反应的化学反应方程式2NaOH+SO2=Na2SO3+H2O.
②若将含二氧化硫的废气通入水中,在一段时间内连续不断测定溶液的pH值,发现pH值变小,这是由于空气中的氧气也参与了相关反应,表示该变化的化学方程式是2H2SO3+O2=2H2SO4.
6.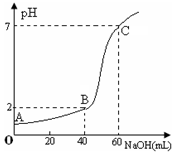 常温下,取20mL某浓度的盐酸作为待测液,用一定物质的量浓度的NaOH溶液进行滴定(假设盐酸与NaOH溶液混合后体积变化忽略不计),滴定过程中溶液的pH变化如右图所示.下列叙述不正确的是( )
常温下,取20mL某浓度的盐酸作为待测液,用一定物质的量浓度的NaOH溶液进行滴定(假设盐酸与NaOH溶液混合后体积变化忽略不计),滴定过程中溶液的pH变化如右图所示.下列叙述不正确的是( )
 常温下,取20mL某浓度的盐酸作为待测液,用一定物质的量浓度的NaOH溶液进行滴定(假设盐酸与NaOH溶液混合后体积变化忽略不计),滴定过程中溶液的pH变化如右图所示.下列叙述不正确的是( )
常温下,取20mL某浓度的盐酸作为待测液,用一定物质的量浓度的NaOH溶液进行滴定(假设盐酸与NaOH溶液混合后体积变化忽略不计),滴定过程中溶液的pH变化如右图所示.下列叙述不正确的是( )| A. | 所用盐酸的浓度是0.09mol•L─1,NaOH溶液浓度为0.03mol•L─1 | |
| B. | 在B点,溶液中离子浓度关系为:c(Cl─)>c(Na+)>c(OH-)>c(H+) | |
| C. | A、B、C三点水的电离程度大小依次为:C>B>A | |
| D. | 滴定前,锥形瓶用待测液润洗,导致盐酸浓度偏低 |
5.能源短缺是人类社会面临的重大问题,利用化学反应可实现多种形式的能量相互转化.请回答以下问题:
(1)由气态基态原子形成1mol化学键释放的最低能量叫键能.从化学键的角度分析,化学反应的过程就是旧键断裂和新键的形成过程.已知反应:N2(g)+3H2(g)?2NH3(g)△H=-93kJ•mol-1.试根据表中所列键能数据,计算a 的数值为391kJ/mol.
(2)甲醇是一种可再生能源,具有广泛的开发和应用前景.已知在常压下有如下变化:
①2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(g)△H=a kJ/mol
②H2O(g)═H2O(l)△H=b kJ/mol
写出液态甲醇完全燃烧生成二氧化碳和液态水的热化学方程式:2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=(a+4b)kJ/mol.
(3)已知:HCN(aq)与NaOH(aq)反应的焓变△H=-12.1kJ•mol-1; HCl(aq)与NaOH(aq)反应的焓变△H=-55.6kJ•mol-1.则HCN在水溶液中电离的焓变△H等于+43.5kJ•mol-1.
(4)已知:H2(g)+$\frac{1}{2}$O2(g)═H2O(1)△H=-285.83kJ•mol-1
CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=-282.9kJ•mol-1;
若氢气与一氧化碳的混合气体完全燃烧可生成5.4g H2O(l),并放出114.3kJ的热量,则混合气中CO的物质的量为0.1mol(计算结果保留一位小数)
(1)由气态基态原子形成1mol化学键释放的最低能量叫键能.从化学键的角度分析,化学反应的过程就是旧键断裂和新键的形成过程.已知反应:N2(g)+3H2(g)?2NH3(g)△H=-93kJ•mol-1.试根据表中所列键能数据,计算a 的数值为391kJ/mol.
| 化学键 | H-H | N-H | N≡N |
| 键能/kJ•mol-1 | 436 | a | 945 |
①2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(g)△H=a kJ/mol
②H2O(g)═H2O(l)△H=b kJ/mol
写出液态甲醇完全燃烧生成二氧化碳和液态水的热化学方程式:2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=(a+4b)kJ/mol.
(3)已知:HCN(aq)与NaOH(aq)反应的焓变△H=-12.1kJ•mol-1; HCl(aq)与NaOH(aq)反应的焓变△H=-55.6kJ•mol-1.则HCN在水溶液中电离的焓变△H等于+43.5kJ•mol-1.
(4)已知:H2(g)+$\frac{1}{2}$O2(g)═H2O(1)△H=-285.83kJ•mol-1
CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=-282.9kJ•mol-1;
若氢气与一氧化碳的混合气体完全燃烧可生成5.4g H2O(l),并放出114.3kJ的热量,则混合气中CO的物质的量为0.1mol(计算结果保留一位小数)
3. 常温下,向50mL溶有0.1molCl2的氯水中滴加2mol/L的NaOH溶液,得到溶液pH随所加NaOH溶液体积的变化图象如下.下列说法正确的是( )
常温下,向50mL溶有0.1molCl2的氯水中滴加2mol/L的NaOH溶液,得到溶液pH随所加NaOH溶液体积的变化图象如下.下列说法正确的是( )
 常温下,向50mL溶有0.1molCl2的氯水中滴加2mol/L的NaOH溶液,得到溶液pH随所加NaOH溶液体积的变化图象如下.下列说法正确的是( )
常温下,向50mL溶有0.1molCl2的氯水中滴加2mol/L的NaOH溶液,得到溶液pH随所加NaOH溶液体积的变化图象如下.下列说法正确的是( )| A. | 若a点pH=4,且c(Cl-)=m c(ClO-),则Ka(HClO)=$\frac{1{0}^{-4}}{m+1}$ | |
| B. | 若x=100,b点对应溶液中:c(OH-)>c(H+),可用pH试纸测定其pH | |
| C. | 若y=200,c点对应溶液中:c(OH-)-c(H+)=2c(Cl-)+c(HClO) | |
| D. | b~c段,随NaOH溶液的滴入,$\frac{c(HClO)}{c(Cl{O}^{-})}$逐渐增大 |
2.在25℃时,FeS的Ksp=6.3×10-18,CuS的Ksp=1.3×10-36,ZnS的Ksp=1.3×10-24.下列有关说法中正确的是( )
| A. | 25℃时,CuS的溶解度大于ZnS的溶解度 | |
| B. | 25℃时,向含有等物质的量的FeCl2、CuCl2的混合液中逐滴加入Na2S,最先出现沉淀的是FeS | |
| C. | 除去ZnCl2溶液中的Cu2+,可以选用FeS作沉淀剂 | |
| D. | 将足量CuSO4溶解在0.1 mol/L的H2S溶液中,S2-能达到的最大浓度为$\sqrt{1.3}$×10-18mol/L |
1.向m g镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体b L.向反应后的溶液中加入c mol/L 氢氧化钾溶液V mL,使金属离子刚好沉淀完全,得到的沉淀质量为n g.再将得到的沉淀灼烧至质量不再改变为止,得到固体p g.则下列关系正确的是( )
| A. | c=$\frac{b}{11.2V}$ | B. | p=m+$\frac{{V}_{c}}{125}$ | C. | n=m+17Vc | D. | $\frac{17}{9}$m<p<$\frac{5}{3}$m |
20.在常温时,将a1ml b1mol/L CH3COOH溶液加入到a2ml b2mol/L NaOH溶液中,下列结论正确的是( )
| A. | 如果a1=a2,b1=b2,则混合溶液中c(CH3COO-)=c(Na+) | |
| B. | 如果混合溶液的PH=7,则混合溶液中c(CH3COO-)>c(Na+) | |
| C. | 如果混合溶液的PH<7,则a1b1=a2b2 | |
| D. | 如果a1=a2,且混合溶液的PH<7,则b1>b2 |
18.下列各组离子或分子能大量共存,当加入相应试剂后会发生化学变化,且发生反应的离子方程式书写正确的是( )
0 162151 162159 162165 162169 162175 162177 162181 162187 162189 162195 162201 162205 162207 162211 162217 162219 162225 162229 162231 162235 162237 162241 162243 162245 162246 162247 162249 162250 162251 162253 162255 162259 162261 162265 162267 162271 162277 162279 162285 162289 162291 162295 162301 162307 162309 162315 162319 162321 162327 162331 162337 162345 203614
| 离子组 | 加入试剂 | 离子方程式 | |
| A | NH4+、Fe2+、SO42- | 少量Ba(OH)2溶液 | SO42-+2NH4++Ba2++2OH-=BaSO4↓+2NH3•5H2O |
| B | Mg2+、HCO3-、Cl-、 | 过量NaOH溶液 | Mg2++2HCO3-+4OH-=2H2O+Mg(OH)2↓+2CO32- |
| C | K+、NH3•H2O、CO32- | 通入少量CO2 | 2OH-+CO2=CO32-+H2O |
| D | Fe3+、NO3-、HSO3- | NaHSO4溶液 | HSO3-+H+=SO2↑+H2O |
| A. | A | B. | B | C. | C | D. | D |