7.用分液漏斗可以分离的一组液体混合物的是( )
| A. | 碘和苯 | B. | 乙醇和水 | C. | 苯和CCl4 | D. | 汽油和水 |
6.下列有机物中,属于烃的衍生物且含有两种官能团的是( )
| A. | CH3Cl | B. | CH3CH2OH | C. | CH2═CHBr | D. | CH2=CH2 |
5.实验室制取少量N2常利用的反应是NaNO2+NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$NaCl+N2↑+2H2O,关于该反应的说法正确( )
| A. | NaNO2是还原剂 | B. | 生成1个N2时转移的电子数为6个 | ||
| C. | NH4Cl中的N元素被还原 | D. | N2既是氧化产物又是还原产物 |
3.下列有关化学实验的操作中,一般情况下不能相互接触的是( )
| A. | 过滤操作中,玻璃棒与三层滤纸 | |
| B. | 过滤操作中,漏斗下端管口与烧杯内壁 | |
| C. | 分液操作中,分液漏斗下端管口与烧杯内壁 | |
| D. | 用胶头滴管向试管滴加液体时,滴管尖端与试管内壁 |
2.已知W、X、Y、Z为短周期元素,W、Z同主族,X、Y、Z同周期,W的气态氢化物的稳定性大于Z的气态氢化物的稳定性,X、Y为金属元素,X的阳离子的氧化性小于Y的阳离子的氧化性.下列说法正确的是( )
| A. | W的气态氢化物的沸点一定高于Z的气态氢化物的沸点 | |
| B. | W与X形成的化合物中只含离子键 | |
| C. | X、Y、Z、W的原子半径依次减小 | |
| D. | 若W与Y原子序数相差5,则二者形成化合物的化学式一定为Y2W3 |
1.Na2FeO4(Fe为+6价)是一种高效多功能水处理剂,应用前景十分看好.一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4+6Na2O2═2Na2FeO4+2Na2O+2Na2SO4+O2↑,(已知Na2O2中O为-1价)对此反应下列说法中正确的是( )
| A. | Na2O2只作氧化剂,O2是还原产物 | |
| B. | Na2FeO4既是氧化产物又是还原产物 | |
| C. | 由上述方程式可知氧化性:Na2FeO4>Na2O2>O2 | |
| D. | 2 mol FeSO4发生反应时,反应中共有8 mol电子转移 |
18.汽车尾气里含有的NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:汽车内燃机燃烧的高温引起氮气和氧气反应,这是汽车尾气里含有NO气体的原因之一.已知不同温度时,反应N2(g)+O2(g)?2NO(g)的平衡常数.
(1)假定该反应是在恒容条件下进行,判断该反应达到平衡的标志AD.
A.消耗1mol N2同时生成1mol O2 B.混合气体密度不变
C.混合气体平均相对分子质量不变 D.2v(N2)正=v(NO)逆
(2)将N2、O2的混合气体充入恒温恒容密闭容器中,下列变化趋势正确的是AC(填字母序号).
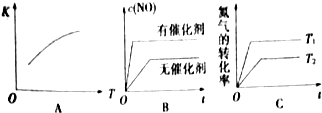
(3)在2400℃时向2L密闭容器中充入N2和O2各1mol,平衡时N2的转化率是4%(保留整数);平衡后再向其中充入1molNO,重新达到化学平衡状态,与原平衡状态相比,此时平衡混合气中NO的体积分数不变(填“变大”、“变小”或“不变”).
(4)为了减轻大气污染,人们提出通过以下反应来处理汽车尾气2NO(g)+2CO(g)?N2(g)+2CO2(g)△H=a kJ•mol-1,为了测定在某种催化剂作用下该反应的反应速率,t℃时在一等容的密闭容器中,在上述条件下该反应能自发进行,某科研机构用气体传感器测得了不同时间的NO和CO的浓度如下表(CO2和N2的起始浓度均为0).
请回答下列问题:
①a小于0(填“大于”或“小于”).
②假设在密闭容器中发生上述处理汽车尾气反应,达到平衡时改变下列条件,能提高NO转化率的是
CD.
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积.
③t℃时2NO(g)+2CO(g)?N2(g)+2CO2(g)反应的平衡常数K=5000.
0 162143 162151 162157 162161 162167 162169 162173 162179 162181 162187 162193 162197 162199 162203 162209 162211 162217 162221 162223 162227 162229 162233 162235 162237 162238 162239 162241 162242 162243 162245 162247 162251 162253 162257 162259 162263 162269 162271 162277 162281 162283 162287 162293 162299 162301 162307 162311 162313 162319 162323 162329 162337 203614
| 温度 | 1760℃ | 2400℃ | 2730℃ |
| 平衡常数 | 2.4×10-4 | 6.4×10-3 | 8.9×10-3 |
A.消耗1mol N2同时生成1mol O2 B.混合气体密度不变
C.混合气体平均相对分子质量不变 D.2v(N2)正=v(NO)逆
(2)将N2、O2的混合气体充入恒温恒容密闭容器中,下列变化趋势正确的是AC(填字母序号).

(3)在2400℃时向2L密闭容器中充入N2和O2各1mol,平衡时N2的转化率是4%(保留整数);平衡后再向其中充入1molNO,重新达到化学平衡状态,与原平衡状态相比,此时平衡混合气中NO的体积分数不变(填“变大”、“变小”或“不变”).
(4)为了减轻大气污染,人们提出通过以下反应来处理汽车尾气2NO(g)+2CO(g)?N2(g)+2CO2(g)△H=a kJ•mol-1,为了测定在某种催化剂作用下该反应的反应速率,t℃时在一等容的密闭容器中,在上述条件下该反应能自发进行,某科研机构用气体传感器测得了不同时间的NO和CO的浓度如下表(CO2和N2的起始浓度均为0).
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/10-4mol/L | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| c(CO)/10-3mol/L | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
①a小于0(填“大于”或“小于”).
②假设在密闭容器中发生上述处理汽车尾气反应,达到平衡时改变下列条件,能提高NO转化率的是
CD.
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积.
③t℃时2NO(g)+2CO(g)?N2(g)+2CO2(g)反应的平衡常数K=5000.
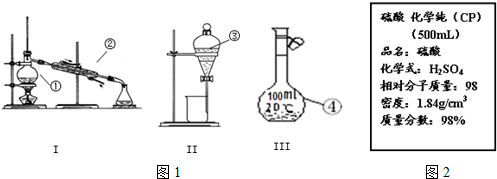
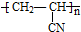 )混合物制作而成的复合材料.工业上用氧化铝电解冶铝的化学方程式为2Al2O3(熔融)$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑;聚丙烯腈单体分子中位于同一平面的原子数目最多为7个.
)混合物制作而成的复合材料.工业上用氧化铝电解冶铝的化学方程式为2Al2O3(熔融)$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑;聚丙烯腈单体分子中位于同一平面的原子数目最多为7个.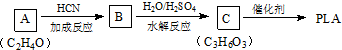
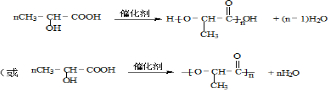 .
.