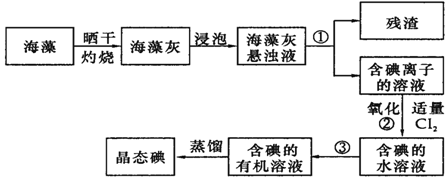
14.下列离子检验的方法正确的是( )
| A. | 某溶液$\stackrel{+AgNO_{3}溶液}{→}$生成白色沉淀,说明原溶液中有Cl- | |
| B. | 某溶液$\stackrel{+NaOH溶液}{→}$生成蓝色沉淀,说明原溶液中有Cu2+ | |
| C. | 某溶液$\stackrel{+BaCl_{2}溶液}{→}$生成白色沉淀,说明原溶液中有SO42- | |
| D. | 某溶液$\stackrel{+KOH溶液}{→}$生成红褐色沉淀,说明原溶液中有Mg2+ |
12.为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应措施.化学反应的焓变通常用实验进行测定,也可进行理论推算.
(1)实验测得,4.6g乙醇(CH3CH2OH)在氧气中充分燃烧生成二氧化碳气体和液态水时释放出136.68kJ的热量,试写出表示乙醇燃烧热的热化学方程式:CH3CH2OH(l)+3O2(g)═2CO2(g)+3H2O(l)△H=-1366.8kJ/mol
(2)从化学键的角度分析,化学反应的过程就是反应物的化学键断裂和生成物的化学键形成的过程.在化学反应过程中,拆开化学键需要消耗能量,形成化学键双会释放能量.
已知反应N2(g)+3H2(g)═2NH3(g)△H=akJ•mol-1.
试根据表中所列键能数据计算a的数值:-93
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算.
已知:C(石墨,s)+O2(g)═CO2(g)H1=-393.5kJ•mol-1①2H2(g)+O2(g)═2H2O(l)H2=-571.6kJ•mol-1②2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H3=-2599kJ•mol-1③
根据盖期定律,计算298K时由C(石墨,s)和H2(g)生成1molC2H2(g)反应的焓变+227.7kJ•mol-.(写出简要的计算过程).
(1)实验测得,4.6g乙醇(CH3CH2OH)在氧气中充分燃烧生成二氧化碳气体和液态水时释放出136.68kJ的热量,试写出表示乙醇燃烧热的热化学方程式:CH3CH2OH(l)+3O2(g)═2CO2(g)+3H2O(l)△H=-1366.8kJ/mol
(2)从化学键的角度分析,化学反应的过程就是反应物的化学键断裂和生成物的化学键形成的过程.在化学反应过程中,拆开化学键需要消耗能量,形成化学键双会释放能量.
已知反应N2(g)+3H2(g)═2NH3(g)△H=akJ•mol-1.
| 化学键 | H-H | N-H | N≡N |
| 键能(kJ•mol-1) | 436 | 391 | 945 |
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算.
已知:C(石墨,s)+O2(g)═CO2(g)H1=-393.5kJ•mol-1①2H2(g)+O2(g)═2H2O(l)H2=-571.6kJ•mol-1②2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H3=-2599kJ•mol-1③
根据盖期定律,计算298K时由C(石墨,s)和H2(g)生成1molC2H2(g)反应的焓变+227.7kJ•mol-.(写出简要的计算过程).
9.下列各选项中所述的两个量,前者比后者大的是( )
| A. | 25℃时,pH均为3的HCl和FeCl3溶液中水的电离程度 | |
| B. | 25℃时,pH均为2的H2SO4溶液和盐酸中氢离子的物质的量浓度 | |
| C. | 物质的量浓度相等的(NH4)2SO4溶液和(NH4)2SO3溶液中NH4+的浓度 | |
| D. | 将pH=4的盐酸和醋酸分别稀释成pH=5的溶液,所加水的量 |
8.已知化合物B3N3H6(硼氮苯)与苯的分子结构相似,分别为硼氮苯的一氯代物、二氯取代物(B3N3H4Cl2)的同分异构体的数目为 ( )
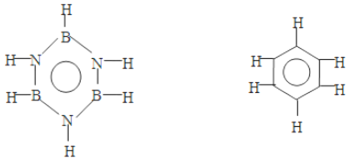
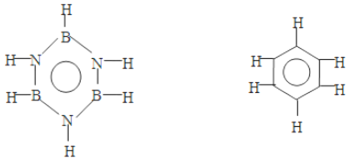
| A. | 2,3 | B. | 1,4 | C. | 2,4 | D. | 4,6 |
7.下列各组物质中,互为同分异构体的是( )
| A. | CH3CH2CH2CH2CH3和CH3CH(CH3)2 | B. | CH2=C(CH3)2和CH2=CHCH=CH2 | ||
| C. | O2和O3 | D. | CH3CH2OH和CH3-O-CH3 |
6.已知丁基(-C4H9)有四种结构,某烃的结构简式为 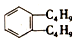 ,该烃可能的结构有( )
,该烃可能的结构有( )
 ,该烃可能的结构有( )
,该烃可能的结构有( )| A. | 16种 | B. | 14种 | C. | 12种 | D. | 10种 |
5.已知乙炔与苯蒸气完全燃烧的热化学方程式分别如下:
①2C2H2(g)+5O2(g)═4CO2(g)+2H2O(1)△H=-2600KJ/mol
②2C6H6(g)+15O2(g)═6CO2(g)+6H2O(1)△H=-6590KJ/mol
下列说法正确的是( )
0 162019 162027 162033 162037 162043 162045 162049 162055 162057 162063 162069 162073 162075 162079 162085 162087 162093 162097 162099 162103 162105 162109 162111 162113 162114 162115 162117 162118 162119 162121 162123 162127 162129 162133 162135 162139 162145 162147 162153 162157 162159 162163 162169 162175 162177 162183 162187 162189 162195 162199 162205 162213 203614
①2C2H2(g)+5O2(g)═4CO2(g)+2H2O(1)△H=-2600KJ/mol
②2C6H6(g)+15O2(g)═6CO2(g)+6H2O(1)△H=-6590KJ/mol
下列说法正确的是( )
| A. | 2mol C2H2(g)完全燃烧生成气态水时放热大于2600kJ | |
| B. | 2mol C6H6(1)完全燃烧生成液态水时放热大于6590kJ | |
| C. | 相同条件下,等质量的C2H2(g)与C6H6(g)完全燃烧,C6H6(g)放热更多 | |
| D. | C2H2(g)三聚生成C6H6(g)的过程属于放热反应 |