10.化学与材料、生活和环境密切相关.下列说法正确的是( )
| A. | 糖、油脂、蛋白质都可以生水解反应 | |
| B. | 天然纤维、聚酚纤维、光导纤维都属于有机高分子材料 | |
| C. | 大力实施矿物燃料脱硫、脱硝技术以减少硫、氮氧化物排放 | |
| D. | 镀锌铁或镀锡铁镀层破损后仍将通过牺牲阳极的阴极保护法防止腐蚀 |
9.X、Y、W、Z为四种短周期主族元素,在周期表中的位置如图所示.W原子的最外层电子数与电子层数相同,下列说法正确的是( )
| X | Y | ||
| W | Z |
| A. | X只能形成一种氢化物 | |
| B. | W、X、Y的原子半径依次增大 | |
| C. | X的简单氢化物的热稳定性比Y的小 | |
| D. | W的最高价氧化物对应的水化物能溶于稀氨水 |
8.下列有关NaClO和NaCl混合溶液的叙述正确的是( )
| A. | 该溶液中,H+、NH4+、SO42-、I-可以大量共存 | |
| B. | 该溶液中,Ag+、K+、NO3-、NH4+可以大量共存 | |
| C. | 该溶液中,Fe2+、Fe3+、Cl-、NO3-可以大量共存 | |
| D. | 向该溶液中加入浓盐酸,每产生1 molCl2,转移电子约为6.02×1023个 |
7.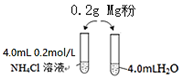 某校化学课外学习小组发现将镁粉按图投入纯水中现象不明显,而投入氯化铵溶液中,两者立即发生反应,产生大量气泡.经检验该过程产生两种气体,其中一种气体有刺激性气味.
某校化学课外学习小组发现将镁粉按图投入纯水中现象不明显,而投入氯化铵溶液中,两者立即发生反应,产生大量气泡.经检验该过程产生两种气体,其中一种气体有刺激性气味.
(1)实验开始时用校准过的pH传感器测定纯水的pH,发现纯水的pH总是在7.30左右,其原因可能是因为气温低于25℃时,Kw小于1.0×10-14,纯水的pH略大于7
(2)请设计简单的实验方案检验上述实验中有刺激性气味的气体:将湿润的红色石蕊试纸放在试管口看是否变蓝,如果变蓝,则有氨气生成,否则没有氨气生成(或者用蘸有浓盐酸的玻璃棒放在试管口,看是否有白烟生成,如果有白烟生成,则有氨气,否则没有氨气)
(3)实验中0.2mol/L氯化铵溶液的pH为5.90,请用离子方程式解释原因:NH4++H2O?NH3•H2O+H+
(4)该小组同学为探究镁与氯化铵溶液反应的原因设计了如下实验方案:
①上述探究实验1-2选用的盐酸为D(填字母).
A、1mol•L-1 B、pH=1.0 C、0.2mol•L-1 D、pH=5.90
②通过实验对比,说明NH4Cl水解产生的H+对反应影响小于NH4+对反应影响(填“小于”、“大于”或“等于”).
(5)该小组同学继续探究镁粉与氯化铵溶液反应剧烈的影响因素.
①实验2-1与实验2-2中实验现象说明Cl-对反应速率的影响很小,请补充完成实验方案所需的试剂.
②实验3-1与实验3-2的结论说明NH4+对反应速率影响很大,则两支试管中实验现象的不同之处是NH4NO3溶液(左试管)和KNO3溶液(右试管)分别与Mg粉反应,左试管反应剧烈,有大量气泡生成,右试管反应很少,没有气泡生成
(6)写出镁与氯化铵溶液反应生成Mg2+的离子方程式Mg+2 NH4+=Mg2++2NH3↑+H2↑.
 某校化学课外学习小组发现将镁粉按图投入纯水中现象不明显,而投入氯化铵溶液中,两者立即发生反应,产生大量气泡.经检验该过程产生两种气体,其中一种气体有刺激性气味.
某校化学课外学习小组发现将镁粉按图投入纯水中现象不明显,而投入氯化铵溶液中,两者立即发生反应,产生大量气泡.经检验该过程产生两种气体,其中一种气体有刺激性气味.(1)实验开始时用校准过的pH传感器测定纯水的pH,发现纯水的pH总是在7.30左右,其原因可能是因为气温低于25℃时,Kw小于1.0×10-14,纯水的pH略大于7
(2)请设计简单的实验方案检验上述实验中有刺激性气味的气体:将湿润的红色石蕊试纸放在试管口看是否变蓝,如果变蓝,则有氨气生成,否则没有氨气生成(或者用蘸有浓盐酸的玻璃棒放在试管口,看是否有白烟生成,如果有白烟生成,则有氨气,否则没有氨气)
(3)实验中0.2mol/L氯化铵溶液的pH为5.90,请用离子方程式解释原因:NH4++H2O?NH3•H2O+H+
(4)该小组同学为探究镁与氯化铵溶液反应的原因设计了如下实验方案:
| 序号 | 实验试剂 | 实验现象 | |
| 实验1-1 | 0.20g镁粉 | 3.0mL 0.2mol/LNH4Cl溶液 | 反应明显,有气泡产生 |
| 实验1-2 | 0.20g镁粉 | 3.0mL盐酸 | 反应不明显,几乎没有气泡产生 |
A、1mol•L-1 B、pH=1.0 C、0.2mol•L-1 D、pH=5.90
②通过实验对比,说明NH4Cl水解产生的H+对反应影响小于NH4+对反应影响(填“小于”、“大于”或“等于”).
(5)该小组同学继续探究镁粉与氯化铵溶液反应剧烈的影响因素.
| 实验序号 | 实验试剂 | |
| 实验2-1 | 0.20g镁粉 | 3.0 mL 0.2mol/LNaCl溶液 |
| 实验2-2 | 0.20g镁粉 | 3.0 mL0.2mol/LNaNO3溶液 |
| 实验3-1 | 0.20g镁粉 | 3.0mL0.2mol/L NH4NO3溶液 |
| 实验3-2 | 0.20g镁粉 | 3.0mL0.2mol/L KNO3溶液 |
②实验3-1与实验3-2的结论说明NH4+对反应速率影响很大,则两支试管中实验现象的不同之处是NH4NO3溶液(左试管)和KNO3溶液(右试管)分别与Mg粉反应,左试管反应剧烈,有大量气泡生成,右试管反应很少,没有气泡生成
(6)写出镁与氯化铵溶液反应生成Mg2+的离子方程式Mg+2 NH4+=Mg2++2NH3↑+H2↑.
4.关于几种分子中的化学键描述不正确的是( )
| A. | 苯每个碳原子的未参加杂化的 2p 轨道形成大π键 | |
| B. | CH4中的 4 个 C-H 键都是 H 的 1s 轨道与 C 的 2p 轨道形成的 s-pσ键 | |
| C. | C2H4 中,每个碳原子的 sp2 杂化轨道形成σ键、未杂化的2p 轨道形成π键 | |
| D. | 乙炔分子中,每个碳原子都有两个未杂化的 2p 轨道形成π键 |
2.如图是实验室制备氯气并进行一系列相关实验的装置(夹持仪器已略).
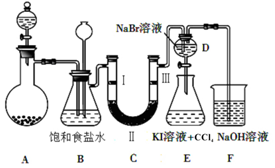
(1)制备氯气选用的药品为固体二氧化锰和浓盐酸,图示装置还缺少的一种仪器为酒精灯.装置B中饱和食盐水的作用是除去Cl2中的HCl气体;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:B中长颈漏斗中液面上升,形成水柱.
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入d(填字母).
(3)设计装置D、E的目的是比较氯、溴、碘单质的氧化性强弱. 当向D中缓缓通入少量氯气时,可以看到无色溶液逐渐变为黄色,打开活塞,将装置D中少量溶液加入装置E中,振荡.观察到的现象是E中溶液分为两层,下层(苯层)为紫红色.
(4)装置F中用足量的NaOH溶液吸收余氯,试写出相应的离子方程式:2OH-+Cl2=Cl-+ClO-+H2O.
0 162006 162014 162020 162024 162030 162032 162036 162042 162044 162050 162056 162060 162062 162066 162072 162074 162080 162084 162086 162090 162092 162096 162098 162100 162101 162102 162104 162105 162106 162108 162110 162114 162116 162120 162122 162126 162132 162134 162140 162144 162146 162150 162156 162162 162164 162170 162174 162176 162182 162186 162192 162200 203614

(1)制备氯气选用的药品为固体二氧化锰和浓盐酸,图示装置还缺少的一种仪器为酒精灯.装置B中饱和食盐水的作用是除去Cl2中的HCl气体;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:B中长颈漏斗中液面上升,形成水柱.
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入d(填字母).
| a | b | c | d | |
| Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(4)装置F中用足量的NaOH溶液吸收余氯,试写出相应的离子方程式:2OH-+Cl2=Cl-+ClO-+H2O.
 锂-磷酸氧铜电池正极的活性物质是Cu4O(PO4)2,可通过下列反应制备:
锂-磷酸氧铜电池正极的活性物质是Cu4O(PO4)2,可通过下列反应制备: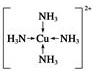 .
. 的名称是3,3,5,5-四甲基庚烷;
的名称是3,3,5,5-四甲基庚烷;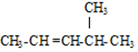 的名称是4-甲基-2-戊烯;
的名称是4-甲基-2-戊烯; ,则键线式为
,则键线式为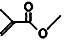 的物质的分子式为C5H8O2;
的物质的分子式为C5H8O2; 的一氯代物有5种;
的一氯代物有5种;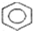 -CH2-C≡CCH2-CH3,其中共平面的碳原子最多可能有15个.
-CH2-C≡CCH2-CH3,其中共平面的碳原子最多可能有15个.