16.已知常温下向AgCl饱和溶液中滴加一定浓度的KI溶液,可观察到白色沉淀逐渐变成黄色.由此可知下列有关说法正确的是( )
| A. | 相同温度下,Ksp(AgI)>Ksp(AgCl) | |
| B. | 由于AgCl与AgI的饱和水溶液几乎都不导电说明这两种物质均为非电解质 | |
| C. | 分别用等体积的蒸馏水和0.01 mol/L KI溶液洗涤AgI沉淀,用水洗涤沉淀损失量大 | |
| D. | 将AgCl与AgI的饱和溶液等体积混合后,再加入足量浓AgNO3溶液,只有AgI沉淀生成 |
13.某学习小组对硫代硫酸钠的相关性质进行探究.
Ⅰ通过硫代硫酸钠与硫酸反应的有关实验,研究反应速率的影响因素,实验过程数据记录如下.
(1)硫代硫酸钠与硫酸反应的离子方程式是S2O32-+2H+═S↓+SO2↑+H2O.
(2)A和B的组合比较,所研究的问题是温度对化学反应速率的影响.
(3)在上述实验中,反应速率最慢的是(填实验序号)C.
Ⅱ对Na2S2O3的其他部分性质进行了理论预测以及实验探究(反应均在溶液中进行).
(4)探究①中进行的实验操作是取pH试纸于玻璃片上,用玻璃棒蘸取硫代硫酸钠于pH试纸的中部,将试纸颜色与标准比色卡对照.
(5)产生探究②中的现象的原因是(用离子方程式表示)S2O32-+4Cl2+5H2O═2SO42-+8Cl-+10H+.
Ⅲ查阅资料发现,在照片冲印过程中,要将曝光后的底片浸泡在过量Na2S2O3溶液中,Na2S2O3可以和涂在胶片上的Ag+反应形成可溶性的无色离子[Ag(S2O3)2]3-,从而起到定影的作用.
该组同学想验证这一过程,于是A同学将Na2S2O3溶液滴至AgNO3溶液中,发现立即生成白色沉淀,他马上停止了实验.一段时间后,发现沉淀逐渐变为黑色,过滤.他认为黑色物质可能是Ag2O或Ag2S.
B同学在A同学分析、实验的基础上分析过滤所得滤液,发现滤液中除含未反应完的AgNO3外,只含有少量Na+和SO42-.
(6)B同学认为根据以上分析,即能判断黑色物质是Ag2S.请简述B同学做出如上判断的理由是溶液中有SO42-,说明有硫元素升价,所以体系中必须有元素降价.若生成Ag2O,体系中无元素降价;所以只能是有一部分硫元素降为-2价,生成Ag2S..
(7)A同学未能验证定影过程的原因可能是定影过程要求将Ag+与过量Na2S2O3溶液反应生成可溶性的无色离子[Ag(S2O3)2]3-(Na2S2O3过量,而A同学将Na2S2O3溶液滴至AgNO3溶液中(AgNO3过量),由于反应物的比例关系不同,因此反应现象不同.
Ⅰ通过硫代硫酸钠与硫酸反应的有关实验,研究反应速率的影响因素,实验过程数据记录如下.
实验序号 | 反应温度/℃ | 参加反应的物质 | ||||
| Na2S2O3 | H2SO4 | H2O | ||||
| V/ml | c/(mol•L-1) | V/ml | c/(mol•L-1) | V/ml | ||
| A | 40 | 5 | 0.1 | 10 | 0.1 | 5 |
| B | 20 | 5 | 0.1 | 10 | 0.1 | 5 |
| C | 20 | 5 | 0.1 | 5 | 0.1 | 10 |
(2)A和B的组合比较,所研究的问题是温度对化学反应速率的影响.
(3)在上述实验中,反应速率最慢的是(填实验序号)C.
Ⅱ对Na2S2O3的其他部分性质进行了理论预测以及实验探究(反应均在溶液中进行).
| 预测 | 实验操作 | 实验现象 | ?现象解释 | |
| 探究① | Na2S2O3溶液呈碱性 | 溶液pH=8 | S2O32-+H2O HS2O3-+OH- | |
| 探究② | Na2S2O3有还原性 | 向新制氯水中滴加Na2S2O3溶液 | 氯水颜色变浅 |
(5)产生探究②中的现象的原因是(用离子方程式表示)S2O32-+4Cl2+5H2O═2SO42-+8Cl-+10H+.
Ⅲ查阅资料发现,在照片冲印过程中,要将曝光后的底片浸泡在过量Na2S2O3溶液中,Na2S2O3可以和涂在胶片上的Ag+反应形成可溶性的无色离子[Ag(S2O3)2]3-,从而起到定影的作用.
该组同学想验证这一过程,于是A同学将Na2S2O3溶液滴至AgNO3溶液中,发现立即生成白色沉淀,他马上停止了实验.一段时间后,发现沉淀逐渐变为黑色,过滤.他认为黑色物质可能是Ag2O或Ag2S.
B同学在A同学分析、实验的基础上分析过滤所得滤液,发现滤液中除含未反应完的AgNO3外,只含有少量Na+和SO42-.
(6)B同学认为根据以上分析,即能判断黑色物质是Ag2S.请简述B同学做出如上判断的理由是溶液中有SO42-,说明有硫元素升价,所以体系中必须有元素降价.若生成Ag2O,体系中无元素降价;所以只能是有一部分硫元素降为-2价,生成Ag2S..
(7)A同学未能验证定影过程的原因可能是定影过程要求将Ag+与过量Na2S2O3溶液反应生成可溶性的无色离子[Ag(S2O3)2]3-(Na2S2O3过量,而A同学将Na2S2O3溶液滴至AgNO3溶液中(AgNO3过量),由于反应物的比例关系不同,因此反应现象不同.
12.在100℃时,将0.40mol 的二氧化氮气体充入2L抽真空的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到如下表数据:
以下说法不正确的是( )
| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n (NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n (N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
| A. | 从反应开始到20s时,NO2的平均反应速率为0.15 mol•L-1min-1 | |
| B. | 达平衡后,混合气体的平均摩尔质量为69g/mol | |
| C. | 达平衡后,若升高温度器气体颜色变深,则可推知升高温度后反应平衡常数K减小 | |
| D. | 达平衡后,如向该密闭容器中再充入0.32 mol He气,并把容器体积扩大为4L,则平衡将向左移动 |
10.在一定条件下,将A和B各0.32mol充入10L恒容密闭容器中,发生反应:A(g)+B(g)?2C(g)△H<0,反应过程中测定的数据如表,下列说法正确的是( )
| t/min | 0 | 2 | 4 | 7 | 9 |
| n(B)/mol | 0.32 | 0.24 | 0.22 | 0.20 | 0.20 |
| A. | 反应前2 min的平均速率v(C)=0.004 mol/(L•min) | |
| B. | 其他条件不变,降低温度,反应达到新平衡前v (逆)>v (正) | |
| C. | 其他条件不变,起始时向容器中充入0.64mol A和0.64mol B,平衡时n(C)<0.48mol | |
| D. | 其他条件不变,向平衡体系中再充入0.32mol A,再次平衡时,B的转化率增大 |
9.Na2O2是强氧化剂,也是航天航空、水下作业的供氧剂.
(1)Na2O2作供氧剂时,主要与人呼出的CO2反应,写出该反应的化学方程式,并用双线桥标明电子转移的方向和数目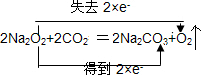 .
.
(2)航空和水下作业有时也会产生污染性气体,某学习小组欲探究Na2o2能否完全吸收氮氧化物、硫氧化物等污染性气体,设计了如下装置(未画完):
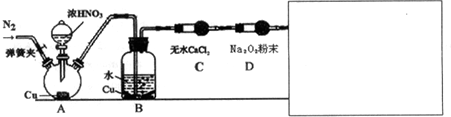
【资料信息】①酸性条件下,NO和NO2都能与MnO4-(H+)反应生成NO3-和Mn2+
②稀硝酸与Cu反应缓慢 ③2NO+Na2O2=2NaNO2
请在答题卷方框内补充完整装置示意图,并做必要标注.补充装置的作用是检验污染气体是否完全被Na2O2吸收,同时可防止污染气体排放到空气中.
(3)该学习小组中甲、乙、丙三位同学设计实验如下,完成表中空格(乙和丙同学对装置和试剂上进行了优化):
写出乙同学实验中D装置发生的化学方程式2NO2+Na2O2=2NaNO3.
(1)Na2O2作供氧剂时,主要与人呼出的CO2反应,写出该反应的化学方程式,并用双线桥标明电子转移的方向和数目
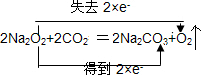 .
.(2)航空和水下作业有时也会产生污染性气体,某学习小组欲探究Na2o2能否完全吸收氮氧化物、硫氧化物等污染性气体,设计了如下装置(未画完):

【资料信息】①酸性条件下,NO和NO2都能与MnO4-(H+)反应生成NO3-和Mn2+
②稀硝酸与Cu反应缓慢 ③2NO+Na2O2=2NaNO2
请在答题卷方框内补充完整装置示意图,并做必要标注.补充装置的作用是检验污染气体是否完全被Na2O2吸收,同时可防止污染气体排放到空气中.
(3)该学习小组中甲、乙、丙三位同学设计实验如下,完成表中空格(乙和丙同学对装置和试剂上进行了优化):
| 实验学生 | 实验操作 | 现象与结论 |
| 甲 | 滴入浓硝酸前,需先打开弹簧夹,通入一段时间N2,目的是将装置中的空气排出.关闭弹簧夹,打开分液漏斗活塞,加入适量浓硝酸后关闭活塞. | 酸性高锰酸钾溶液不褪色,说明Na2O2能完全吸收NO, |
| 乙 | 去掉装置B,直接将A、C装置相连.打开分液漏斗活塞,加入适量浓硝酸后关闭活塞. | 与甲同学现象相似,说明Na2O2能完全吸收NO2 |
| 丙 | 在乙同学装置的基础上,将A装置中浓硝酸换成浓硫酸,并进行加热,(或将分液漏斗中的试剂换为浓硫酸,将铜换为亚硫酸钠粉末),打开分液漏斗活塞,加入适量试剂后关闭活塞. | 与甲同学现象相似,说明Na2O2能完全吸收NO2 |
7.某兴趣学习小组的同学就用如图5个装置进行常见物质的制取,并探究其性质(图中a、b、c表示止水夹),请对其进行完善或评价,试回答下列问题:
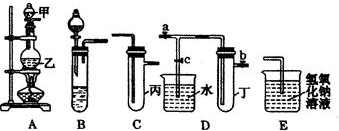
(1)将A、C、E相连后,以二氧化锰和浓盐酸(填写名称)为原料制取Cl2,仪器乙的名称是圆底烧瓶.
(2)利用(1)中装置和药品,在丙中加入适量水,即可制得氯水.将所得氯水分为两份,进行Ⅰ、Ⅱ两个实验,实验操作、现象、结论如下:
实验Ⅰ获得结论不合理请说明理由:没有事先证明干燥的氯气无漂白性
实验Ⅱ获得结论是否合理?不合理(填“合理”或“不合理”).请写出产生气泡的离子方程式HCO3-+H+=CO2↑+H2O
(3)利用(1)中装置还可设计一个简单的实验比较Cl-和S2-的还原性强弱.若C中加入硫酸钾溶液,则C中预期出现的现象是产生淡黄色沉淀.
(4)将B、D、E装置相连接(打开止水夹a和止水夹b,关闭止水夹c),在B中盛装浓硝酸和铜片(将铜片放在有孔塑料板上),可制得NO2.一段时间后,欲用D装置探究NO2与水的反应,其操作步骤为:先关闭a、b,打开c再双手紧握(或微热)试管丁,使NO2逸出与水接触以使烧杯中的水进入试管丁,观察现象,E装置的作用是吸收尾气防止污染空气.
0 161905 161913 161919 161923 161929 161931 161935 161941 161943 161949 161955 161959 161961 161965 161971 161973 161979 161983 161985 161989 161991 161995 161997 161999 162000 162001 162003 162004 162005 162007 162009 162013 162015 162019 162021 162025 162031 162033 162039 162043 162045 162049 162055 162061 162063 162069 162073 162075 162081 162085 162091 162099 203614

(1)将A、C、E相连后,以二氧化锰和浓盐酸(填写名称)为原料制取Cl2,仪器乙的名称是圆底烧瓶.
(2)利用(1)中装置和药品,在丙中加入适量水,即可制得氯水.将所得氯水分为两份,进行Ⅰ、Ⅱ两个实验,实验操作、现象、结论如下:
| 实验序号 | 实验操作 | 现象 | 结论 |
| Ⅰ | 将所得氯水滴入品红溶液 | 品红溶液褪色 | 氯气与水反应的产物有漂白性 |
| Ⅱ | 向所得氯水中加入碳酸氢钠粉末 | 有无色气泡产生 | 氯气与水反应至少产生一种酸性强于碳酸的物质 |
实验Ⅱ获得结论是否合理?不合理(填“合理”或“不合理”).请写出产生气泡的离子方程式HCO3-+H+=CO2↑+H2O
(3)利用(1)中装置还可设计一个简单的实验比较Cl-和S2-的还原性强弱.若C中加入硫酸钾溶液,则C中预期出现的现象是产生淡黄色沉淀.
(4)将B、D、E装置相连接(打开止水夹a和止水夹b,关闭止水夹c),在B中盛装浓硝酸和铜片(将铜片放在有孔塑料板上),可制得NO2.一段时间后,欲用D装置探究NO2与水的反应,其操作步骤为:先关闭a、b,打开c再双手紧握(或微热)试管丁,使NO2逸出与水接触以使烧杯中的水进入试管丁,观察现象,E装置的作用是吸收尾气防止污染空气.
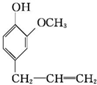 )可用于配制康乃馨型香精以及制异丁香酚和香兰素等,合成丁子香酚的一种路线如下:
)可用于配制康乃馨型香精以及制异丁香酚和香兰素等,合成丁子香酚的一种路线如下: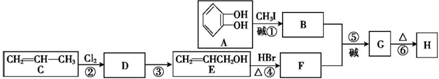
 (X代表卤素原子);
(X代表卤素原子);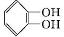 +CH3I$\stackrel{碱}{→}$
+CH3I$\stackrel{碱}{→}$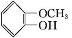 +HI.
+HI.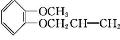 .
.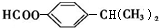 (任写一种).
(任写一种).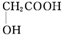 )及化合物A为原料经如下步骤可合成邻苯氧乙酸酚酯:
)及化合物A为原料经如下步骤可合成邻苯氧乙酸酚酯: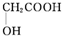 $\stackrel{反应条件Ⅰ}{→}$G$→_{②A/碱}^{①Na_{2}CO_{3}溶液}$H$\stackrel{酸化}{→}$$\stackrel{反应条件Ⅱ}{→}$
$\stackrel{反应条件Ⅰ}{→}$G$→_{②A/碱}^{①Na_{2}CO_{3}溶液}$H$\stackrel{酸化}{→}$$\stackrel{反应条件Ⅱ}{→}$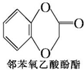
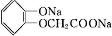 .
.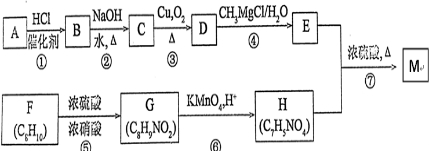
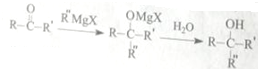
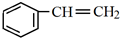 ,H中官能团的名称为羧基、硝基.
,H中官能团的名称为羧基、硝基.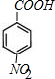 +
+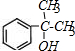 $?_{△}^{浓硫酸}$
$?_{△}^{浓硫酸}$ +H2O.
+H2O. 、
、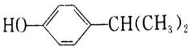 .(任写一种)
.(任写一种)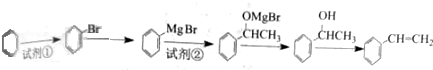
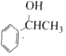 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$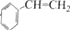 +H2O.
+H2O.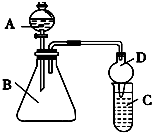 某同学为探究元素周期表中元素性质的递变规律,设计了如下实验.
某同学为探究元素周期表中元素性质的递变规律,设计了如下实验.