19.某食品袋中有一个写着“干燥剂”的小纸袋,里面的主要成分是生石灰,对此“干燥剂”的说法正确的是( )
| A. | 小纸袋中的物质可长期持续地做干燥剂 | |
| B. | 生石灰属于盐类 | |
| C. | 此干燥剂为混合物 | |
| D. | 其中钙元素的存在形态为游离态 |
18.下列化学用语表示正确的是( )
| A. | 氯化铁的化学式:FeCl | |
| B. | 乙烯的结构式:CH2=CH2 | |
| C. | Na2O的电子式: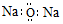 | |
| D. | KAl(SO4)2的电离方程式:KAl(SO4)2=K++Al3++2SO42- |
17.写出以下有机物的官能团名称并判断物质类别:
(1)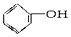 (2)CH2=CH-CH3 (3)CH3COOCH3(4)CH3-CHO (5)CH3-OH (6)CH3CH2COOH.
(2)CH2=CH-CH3 (3)CH3COOCH3(4)CH3-CHO (5)CH3-OH (6)CH3CH2COOH.
(1)
 (2)CH2=CH-CH3 (3)CH3COOCH3(4)CH3-CHO (5)CH3-OH (6)CH3CH2COOH.
(2)CH2=CH-CH3 (3)CH3COOCH3(4)CH3-CHO (5)CH3-OH (6)CH3CH2COOH.| 物质序号 | 物质类别 | 官能团名称 | 物质序号 | 物质类别 | 官能团名称 |
| (1) | (4) | ||||
| (2) | (5) | ||||
| (3) | (6) |
16.设NA表示阿伏加德罗常数.下列说法中,错误的是( )
| A. | 标准状况下,22.4 L氢气和氯气的混合气体,所含分子数为NA | |
| B. | 常温常压下,1 mol氦气含有的原子数约为NA | |
| C. | 1 mol Al3+含有核外电子数为3NA | |
| D. | t℃时,1 L pH=6的纯水中,含1×10-6NA个OH- |
15.阿伏加德罗常数约为6.02×1023mol-1,下列叙述正确的是( )
| A. | 1mol FeCl3完全水解转化为氢氧化铁胶体后能生成NA个胶粒 | |
| B. | 0.1 L 3 mol•L-1的NH4NO3溶液中含有的NH4+数目为0.3×6.02×1023 | |
| C. | 5.6g铁粉与硝酸反应失去的电子数一定为0.3×6.02×1023 | |
| D. | 4.5gSiO2晶体中含有的硅氧键数目为0.3×6.02×1023 |
14.在托盘天平两端各放一只烧杯,调节至平衡.在两只烧杯里加入等质量、等质量分数的稀盐酸,然后再左右两烧杯中分别放入质量相等的镁和铝,带充分反应后,镁有剩余,则还可以观察到的现象是( )
①天平保持平衡 ②铝也有剩余 ③天平指针偏向放镁的一方 ④天平指针偏向放铝的一方.
①天平保持平衡 ②铝也有剩余 ③天平指针偏向放镁的一方 ④天平指针偏向放铝的一方.
| A. | 只有① | B. | ①和② | C. | ②和④ | D. | 只有③ |
13.下列混合物的分离和提纯方法中,主要是从溶解性的角度考虑的是( )
| A. | 蒸发 | B. | 蒸馏 | C. | 洗气 | D. | 萃取 |
11.在100℃时,3.88g 的气体A与足量的Na2O2反应,可放出氧气,且固体的质量增加了2.28g,由此可知,A的组成为( )
| A. | 只有水蒸气 | B. | 只有二氧化碳 | ||
| C. | 水蒸气和二氧化碳 | D. | 无法确定 |
10.1mol Na2O2晶体和1mol Na2O的晶体中阴离子的个数比较,前者和后者的关系是( )
0 161874 161882 161888 161892 161898 161900 161904 161910 161912 161918 161924 161928 161930 161934 161940 161942 161948 161952 161954 161958 161960 161964 161966 161968 161969 161970 161972 161973 161974 161976 161978 161982 161984 161988 161990 161994 162000 162002 162008 162012 162014 162018 162024 162030 162032 162038 162042 162044 162050 162054 162060 162068 203614
| A. | 前者大 | B. | 前者小 | C. | 相等 | D. | 不能肯定 |