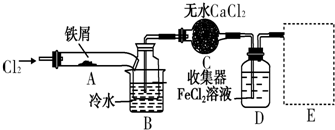
8.设NA为阿伏加德罗常数,下列有关叙述正确的是( )
| A. | 1 molCu和足量的硫粉加热反应转移的电子数是2NA | |
| B. | 铜粉溶于1L0.5mol/L稀硝酸中,当生成标况下2.24LNO时,溶液中的氮原子数为0.4NA个 | |
| C. | 常温下,4.4克二氧化碳和二氧化氮中的混合物中氧原子数为0.2NA | |
| D. | 标准状况下,11.2升氯气溶于水,转移电子数为0.5 NA |
7.下列说法正确的是( )
| A. | 胶体区别于其他分散系的本质特征是胶体可发生丁达尔效应 | |
| B. | 在一定温度和压强下,气体体积主要取决于气体分子之间的平均间距 | |
| C. | 摩尔质量与物质的量的多少有关,它等于物质的质量除以物质的量 | |
| D. | 确定物质中是否含有C、H、O、N、Cl、Br、S等元素可用元素分析仪,确定物质中是否含有哪些金属元素可用原子吸收光谱 |
6.下列物质的主要成分属于天然有机高分子的是( )
| A. | 水泥 | B. | 木材 | C. | 陶瓷 | D. | 铝合金 |
4.下列物质不属于硅酸盐产品的是( )
| A. | 青花瓷 | B. | 水泥 | C. | 石英 | D. | 玻璃 |
2.离子反应是一类重要反应,还原性Fe2+>Br-,下列有关离子方程式书写正确的是( )
| A. | 金属钠与水反应:Na+H2O═Na++OH-+H2↑ | |
| B. | Mg(OH)2与H2SO4反应:Mg2++2OH-+2H++SO42═MgSO4↓+2H2O | |
| C. | 向硫酸氢钠溶液加氢氧化钡溶液至完全沉淀:H++SO42-+OH-+Ba2+═BaSO4↓+H2O | |
| D. | FeBr2溶液与Cl2按照等物质的量反应:2Br-+Cl2═2Cl-+Br2 |
1. Ⅰ:为了减少CO的排放,某环境研究小组以CO和H2 为原料合成清洁能源二甲醚(DME),反应如下:4H2(g)+2CO(g)
Ⅰ:为了减少CO的排放,某环境研究小组以CO和H2 为原料合成清洁能源二甲醚(DME),反应如下:4H2(g)+2CO(g)
CH3OCH3(g)+H2O(g)△H=-198kJ/mol.
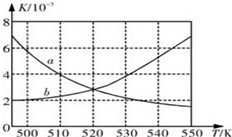
(1)如图所示能正确反应平衡常数K随温度变化关系的曲线是a(填曲线标记字母),其判断理由是正反应放热,温度升高,平衡常数减小.
(2)在一定温度下,向2.0L固定的密闭容器中充入2molH2和1molCO,经过一段时间后,反应4H2(g)+2CO(g)
CH3OCH3(g)+H2O(g) 达到平衡.反应过程中测得的部分数据见下表:
①0-20min的平均反应速率V(co)=7.5×10-3mol/(L•min);
②达平衡时,H2 的转化率为:80%;
③在上述温度下,向平衡后的2L容器中再充入0.4molH2 和0.4molCH3OCH3 (g),则化学平衡正向(向“正向”、“逆向”或“不”)移动.
(3)用Li2CO3 和Na2CO3 的熔融盐混合物作为电解质,CO为负极燃气,空气与CO2 的混合气体作为正极助燃气,制得在650℃工作的燃料电池,则负极反应式为:2CO+2CO32--4e-=4CO2当燃料电池的电路中有0.2NA个电子发生转移,则标况下生成2.24升CO2.
Ⅱ:已知在25℃时,Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20,在25℃下,向浓度均为0.1mol/L的MgCl2 和CuCl2 混合溶液中逐滴加入氨水,先生成Cu(OH)2沉淀(填化学式)生成该沉淀的离子方程式为Cu2++2NH3•H2O?Cu(OH)2↓+2NH4+.
 Ⅰ:为了减少CO的排放,某环境研究小组以CO和H2 为原料合成清洁能源二甲醚(DME),反应如下:4H2(g)+2CO(g)
Ⅰ:为了减少CO的排放,某环境研究小组以CO和H2 为原料合成清洁能源二甲醚(DME),反应如下:4H2(g)+2CO(g)CH3OCH3(g)+H2O(g)△H=-198kJ/mol.
(1)如图所示能正确反应平衡常数K随温度变化关系的曲线是a(填曲线标记字母),其判断理由是正反应放热,温度升高,平衡常数减小.
(2)在一定温度下,向2.0L固定的密闭容器中充入2molH2和1molCO,经过一段时间后,反应4H2(g)+2CO(g)
CH3OCH3(g)+H2O(g) 达到平衡.反应过程中测得的部分数据见下表:
| 时间/min | 0 | 20 | 40 | 80 | 100 |
| n(H2)/mol | 2.0 | 1.4 | 0.85 | 0.4 | - |
| n(CO)/mol | 1.0 | - | 0.425 | 0.2 | 0.2 |
| n(CH3OCH3)/mol | 0 | 0.15 | - | - | 0.4 |
| n(H2O)/mol | 0 | 0.15 | 0.2875 | 0.4 | 0.4 |
②达平衡时,H2 的转化率为:80%;
③在上述温度下,向平衡后的2L容器中再充入0.4molH2 和0.4molCH3OCH3 (g),则化学平衡正向(向“正向”、“逆向”或“不”)移动.
(3)用Li2CO3 和Na2CO3 的熔融盐混合物作为电解质,CO为负极燃气,空气与CO2 的混合气体作为正极助燃气,制得在650℃工作的燃料电池,则负极反应式为:2CO+2CO32--4e-=4CO2当燃料电池的电路中有0.2NA个电子发生转移,则标况下生成2.24升CO2.
Ⅱ:已知在25℃时,Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20,在25℃下,向浓度均为0.1mol/L的MgCl2 和CuCl2 混合溶液中逐滴加入氨水,先生成Cu(OH)2沉淀(填化学式)生成该沉淀的离子方程式为Cu2++2NH3•H2O?Cu(OH)2↓+2NH4+.
13.下列容器不能用来盛放冷的浓硫酸和浓硝酸的是( )
| A. | 铁制容器 | B. | 铝制容器 | C. | 铜制容器 | D. | 玻璃容器 |
12.NA表示阿伏加德罗常数数值,下列有关说法正确的是( )
0 161827 161835 161841 161845 161851 161853 161857 161863 161865 161871 161877 161881 161883 161887 161893 161895 161901 161905 161907 161911 161913 161917 161919 161921 161922 161923 161925 161926 161927 161929 161931 161935 161937 161941 161943 161947 161953 161955 161961 161965 161967 161971 161977 161983 161985 161991 161995 161997 162003 162007 162013 162021 203614
| A. | 18.4 mol/L的浓硫酸与等质量的水混合所得溶液的物质的量浓度大于9.2 mol/L | |
| B. | 室温下,1LpH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA | |
| C. | 50 mL 14.0 mol•L-1浓硝酸与足量铜反应,转移的电子数为0.35 NA | |
| D. | 同温同压同体积下的两种气体12C18O和14N2具有的电子数相等 |
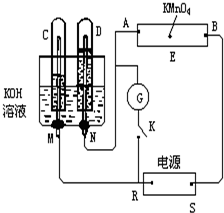 如图所示,E为沾有Na2SO4溶液的滤纸,并加入几滴酚酞.A,B分别为Pt片,压在滤纸两端,R、S为电池的电极.M、N是用多微孔的Ni的电极材料,它在碱溶液中可以视为惰性电极.G为电流计,K为开关.C、D和电解池中都充满浓KOH溶液.若在滤纸中央点上一滴紫色的KMnO4溶液,K打开,接通电源一段时间后,C、D中有气体产生.
如图所示,E为沾有Na2SO4溶液的滤纸,并加入几滴酚酞.A,B分别为Pt片,压在滤纸两端,R、S为电池的电极.M、N是用多微孔的Ni的电极材料,它在碱溶液中可以视为惰性电极.G为电流计,K为开关.C、D和电解池中都充满浓KOH溶液.若在滤纸中央点上一滴紫色的KMnO4溶液,K打开,接通电源一段时间后,C、D中有气体产生.