20.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 通常状况下,NA个N2所占的体积约为22.4L | |
| B. | 1L1mol•L-1NaOH水溶液中含有的氧原子数为NA | |
| C. | 足量Na与1molCl2完全反应,转移电子的数目为2NA | |
| D. | 1mol Na2O2中含有的阴离子数为2NA |
19.用NA表示阿伏伽德罗常数的值,下列叙述中正确的是( )
| A. | 在常温常压下,2.24L NH3与1.8g H2O,所含的质子数均为NA | |
| B. | 在常温常压下,1mol Cl2与足量的NaOH溶液完全反应,转移电子2NA | |
| C. | 在标准状况下,64g SO2 中含有的原子数为3NA | |
| D. | 在标准状况下,11.2L H2O含有的分子数为0.5NA |
17.设NA表示阿伏加德罗常数的值.下列有关说法中正确的是( )
| A. | 常温常压下,46 gN2O4中含氧原子数为2NA | |
| B. | 常温常压下,11.2 LNH3中含共价键的数目为1.5NA | |
| C. | 电解精炼铜阳极质量减少32 g时电路中转移电子总数为NA | |
| D. | 1 L 0.2 mol/LNa2SO4溶液中含有阴阳离子总数为0.6NA |
14.NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 常温下7.2 g CaO2晶体中阴离子和阳离子总数为0.3 NA | |
| B. | 1mol/L的氯化铁溶液中,若Cl-的数目为3NA,则Fe3+的数目为NA | |
| C. | 反应3H2(g)+N2(g)?2NH3(g)△H=-92 kJ/mol,当放出热量9.2 kJ时,转移电子0.6 NA | |
| D. | 标准状况下,11.2L三氯甲烷中含有含极性共价键数目为1.5NA |
12.NA表示阿伏加德罗常数,下列说法不正确的是( )
0 161825 161833 161839 161843 161849 161851 161855 161861 161863 161869 161875 161879 161881 161885 161891 161893 161899 161903 161905 161909 161911 161915 161917 161919 161920 161921 161923 161924 161925 161927 161929 161933 161935 161939 161941 161945 161951 161953 161959 161963 161965 161969 161975 161981 161983 161989 161993 161995 162001 162005 162011 162019 203614
| A. | 含NA个Na+的Na2O溶解于1 L水中,Na+的物质的量浓度为1 mol•L-1 | |
| B. | 常温常压下,5.6g乙烯与丁烯(C4H8)的混合物中氢原子数为0.8NA | |
| C. | 标准状况下,4.48 LCl2与足量的Fe反应转移电子数为0.4NA | |
| D. | 0.1 mol H218O与D2O的混合物中中子数为NA |
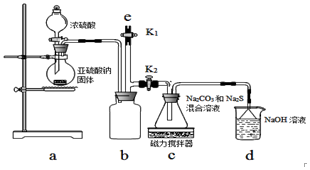 氰化钠是一种重要的基本化工原料.泄漏时会导致环境污染,可以通过喷洒双氧水或硫代硫酸钠溶液来处理.
氰化钠是一种重要的基本化工原料.泄漏时会导致环境污染,可以通过喷洒双氧水或硫代硫酸钠溶液来处理.