10.下列气体在同温度、同压强、同质量时,体积最小的是( )
| A. | CO2 | B. | CO | C. | CH4 | D. | H2 |
9.将钠投入下列溶液中,反应的剧烈程度由强到弱的是( )
①水 ②乙醇 ③0.5mol•L-1盐酸 ④0.1mol•L-1 FeCl3溶液.
①水 ②乙醇 ③0.5mol•L-1盐酸 ④0.1mol•L-1 FeCl3溶液.
| A. | ④③②① | B. | ④③①② | C. | ③④①② | D. | ①③④② |
8.下列离子方程式书写正确的是( )
| A. | NaAlO2溶液中通入过量CO2气体:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3- | |
| B. | NH4 HCO3溶液与足量的NaOH溶液反应:HCO3-+OH-═CO32-+H2O | |
| C. | 向Al2(SO4)3溶液中加入过量的NaOH溶液:Al3++3OH-═Al(OH)3↓ | |
| D. | 向FeI2溶液中通入少量Cl2:2Fe2++Cl2═2Fe3++2Cl- |
7.利用CH4和O2的反应,在KOH溶液中用铂作电极可以构成原电池.下列说法正确的是( )
| A. | 每消耗1molCH4可以向外电路提供4mole- | |
| B. | 在负极上O2获得电子,电极反应式为 O2+2H2O+4e-=4OH- | |
| C. | 外电路电子由负极流向正极,内电路电子由正极流向负极 | |
| D. | 电池放电过程中,溶液的PH不断降低 |
6.在容积可变的密闭容器中存在如下反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H<0,下列分析中正确的是( )
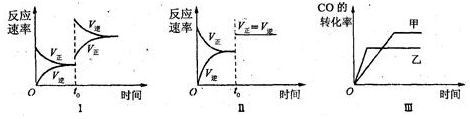

| A. | 图Ⅱ研究的只是t0时使用催化剂对反应速率的影响 | |
| B. | 图Ⅰ研究的是t0时缩小容器体积对反应速率的影响 | |
| C. | 图Ⅲ研究的是温度对化学平衡的影响,且乙的温度较高 | |
| D. | 图Ⅲ研究的是催化剂对化学平衡的影响,且甲使用了催化剂 |
4.对于可逆反应N2(g)+3H2(g)?2NH3(g)下列各项表示的是在4种不同情况下的反应速率,其中反应速率最快的是( )
| A. | V(N2)=0.01mol/(L•S) | B. | V(H2)=0.2mol/(L•S) | ||
| C. | V(H2)=0.6mol/(L•min) | D. | V(NH3)=1.2mol/(L•min) |
3.下列依据热化学方程式得出的结论正确的是( )
| A. | 已知2H2(g)+O2(g)═2H2O(g)△H=-483.6 kJ•mol-1,则氢气的燃烧热为241.8 kJ•mol-1 | |
| B. | 已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.3 kJ•mol-1,则含40.0g NaOH的稀溶液与稀醋酸完全中和,放出的热量小于57.3 kJ | |
| C. | 已知2C(s)+2O2(g)═2CO2(g)△H=a,2C(s)+O2(g)═2CO(g)△H=b,则a>b | |
| D. | 已知CH4(g)+H2O(g)═CO(g)+3 H2(g)△H=+206.1 kJ•mol-1,反应过程中使用催化剂,△H减小 |
2.有一含有Na+、Mg2+、Cl-、SO42-的溶液,已知Na+、Mg2+、Cl-的个数之比为3:7:9,则Cl-与SO42-的个数比为( )
0 161818 161826 161832 161836 161842 161844 161848 161854 161856 161862 161868 161872 161874 161878 161884 161886 161892 161896 161898 161902 161904 161908 161910 161912 161913 161914 161916 161917 161918 161920 161922 161926 161928 161932 161934 161938 161944 161946 161952 161956 161958 161962 161968 161974 161976 161982 161986 161988 161994 161998 162004 162012 203614
| A. | 9:4 | B. | 4:9 | C. | 2:1 | D. | 1:2 |