17.卤块主要成分是MgCl2,还含此外还含Fe2+、Fe3+和Mn2+等杂质离子.以卤块为原料按如图所示流程进行生产,可制得轻质氧化镁.
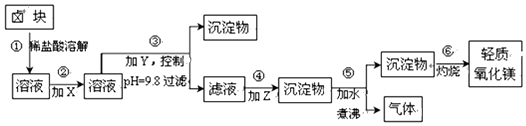
相关数据:
请根据表提供的资料回答:
(1)流程中加入的试剂X、Y、Z最佳选择依次是表2中的a、c、d(选填试剂编号).
(2)步骤②发生反应的离子方程式为2Fe2++ClO-+2H+=Cl-+2Fe3++H2O;步骤⑤中发生反应的化学方程为MgCO3+H2O $\frac{\underline{\;\;△\;\;}}{\;}$Mg(OH)2↓+CO2↑.
(3)为尽量除去杂质,步骤③控制pH为9.8时,停止加入Y.调节为该pH的目的是使Mg2+以外的杂质尽可能彻底地转化为沉淀除去.
(4)若在实验室进行步骤⑥的灼烧实验,必须用到的仪器是ABCE.
A.酒精喷灯 B.铁三角架 C.坩埚 D.蒸发皿 E.泥三角 F.烧杯 G.石棉网
(5)已知在25℃时,Ksp[Mg(OH)2)=3.2×10-11,向0.02mol•L-1的MgCL2溶液中加入NaOH固体,如要生成Mg( OH )2沉淀,应使溶液中的c( OH-)最小为4×10-5 mol•L-1.
(6)为了分析制取的产品中残留铁元素的含量,取5g产品,先将Fe3+预处理为Fe2+后配制成100mL溶液,取25.00mL,用0.01mol•L-1KMnO4标准溶液在酸性条件下进行滴定.
①滴定前是否要滴加指示剂?否(填“是”或“否”),请说明理由KMnO4溶液的紫红色可指示反应终点.
②终点时,消耗标准溶液20.00mL,则残留物中铁元素的质量分数是4.480%.
(7)判断下列操作对测定结果的影响(填“偏高“、“偏低”或“无影响”)
①若在配制标准溶液过程中,烧杯中的KMnO4溶液有少量溅出,使测定结果偏高.
②若在滴定终点读取滴定管刻度时,俯视标准液液面,使测定结果偏低.

相关数据:
| 表1:生成氢氧化物沉淀的pH | 表2:原料价格表 | |||
| 物质 | 开始沉淀 | 沉淀完全 | 物质 | 价格(元/吨) |
| Fe(OH)3 | 2.7 | 3.7 | a.漂液(含25.2%NaClO) | 450 |
| Fe(OH)2 | 7.6 | 9.6 | b.双氧水(含30%H2O2) | 1500 |
| Mn(OH)2 | 8.3 | 9.8 | c.烧碱(含98%NaOH) | 2200 |
| Mg(OH)2 | 9.6 | 11.1 | d.纯碱(含99.5%Na2CO) | 800 |
(1)流程中加入的试剂X、Y、Z最佳选择依次是表2中的a、c、d(选填试剂编号).
(2)步骤②发生反应的离子方程式为2Fe2++ClO-+2H+=Cl-+2Fe3++H2O;步骤⑤中发生反应的化学方程为MgCO3+H2O $\frac{\underline{\;\;△\;\;}}{\;}$Mg(OH)2↓+CO2↑.
(3)为尽量除去杂质,步骤③控制pH为9.8时,停止加入Y.调节为该pH的目的是使Mg2+以外的杂质尽可能彻底地转化为沉淀除去.
(4)若在实验室进行步骤⑥的灼烧实验,必须用到的仪器是ABCE.
A.酒精喷灯 B.铁三角架 C.坩埚 D.蒸发皿 E.泥三角 F.烧杯 G.石棉网
(5)已知在25℃时,Ksp[Mg(OH)2)=3.2×10-11,向0.02mol•L-1的MgCL2溶液中加入NaOH固体,如要生成Mg( OH )2沉淀,应使溶液中的c( OH-)最小为4×10-5 mol•L-1.
(6)为了分析制取的产品中残留铁元素的含量,取5g产品,先将Fe3+预处理为Fe2+后配制成100mL溶液,取25.00mL,用0.01mol•L-1KMnO4标准溶液在酸性条件下进行滴定.
①滴定前是否要滴加指示剂?否(填“是”或“否”),请说明理由KMnO4溶液的紫红色可指示反应终点.
②终点时,消耗标准溶液20.00mL,则残留物中铁元素的质量分数是4.480%.
(7)判断下列操作对测定结果的影响(填“偏高“、“偏低”或“无影响”)
①若在配制标准溶液过程中,烧杯中的KMnO4溶液有少量溅出,使测定结果偏高.
②若在滴定终点读取滴定管刻度时,俯视标准液液面,使测定结果偏低.
16.设NA为阿伏伽德罗常数的值.已知乙烯和环丙烷(C3H6)组成的混合气体的质量为28g,下列对该混合气体的说法错误的是( )
| A. | 混合气体中含有的碳碳双键数为NA | |
| B. | 混合气体中含有的碳原子数为2NA | |
| C. | 当混合气体完全燃烧时,消耗O2的分子数为3NA | |
| D. | 当混合气体完全燃烧时,转移的电子数为12NA |
15.下列有关二氧化硫的说法正确的是( )
| A. | 密度比空气小 | |
| B. | 是无色无味的气体 | |
| C. | SO2能使溴水褪色,说明SO2具有漂白性 | |
| D. | 某生产硫酸厂区紫罗兰花变成白色,说明其周围空气中可能含较高浓度SO2 |
14.下列有关物质用途的说法不正确的是( )
| A. | 聚氯乙烯可用于制食品袋 | B. | 液NH3可用作制冷剂 | ||
| C. | SiO2可用于制造光导纤维 | D. | 漂白粉可用于杀菌消毒 |
12.NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 8g CH4O中含有的C-H键数目为NA | |
| B. | 25℃时,100mL pH=8的氨水中NH4+的个数为9.9×10-8NA | |
| C. | 56g Fe和64g Cu分别与1 mol S反应转移的电子数均为2NA | |
| D. | 标准状况下,2.24 LCl2溶于水所得氯水中含氯的微粒总数为0.2NA |
10.某物质的实验式为PtCl4•2NH3,其水溶液不导电,加入AgNO3溶液也不产生沉淀以强碱处理并没有NH3放出,则关于此化合物的说法中正确的是( )
| A. | 配合物中中心原子的电荷数和配位数均为6 | |
| B. | Pt4+提供孤对电子 | |
| C. | Cl-和NH3分子均与Pt4+配位 | |
| D. | 配合物中Cl-与Pt4+配位,而NH3分子不配位 |
9.下列有关化学用语表示错误的是( )
| A. | HCN的结构式:H-C≡N | |
| B. | HClO的电子式: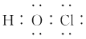 | |
| C. | 质子数为86、中子数为51的铯原子:86137Cs | |
| D. | S2-的结构示意图: |
8.在由水电离出的c(H+)=1×10-12的溶液中可能大量共存的离子组是( )
0 161807 161815 161821 161825 161831 161833 161837 161843 161845 161851 161857 161861 161863 161867 161873 161875 161881 161885 161887 161891 161893 161897 161899 161901 161902 161903 161905 161906 161907 161909 161911 161915 161917 161921 161923 161927 161933 161935 161941 161945 161947 161951 161957 161963 161965 161971 161975 161977 161983 161987 161993 162001 203614
| A. | NH4+、K+、CO32-、Cl- | B. | Al3+、Cu2+、S2-、Cl- | ||
| C. | NH4+、Cu2+、Cl-、NO3- | D. | Fe3+、K+、SCN-、NO3- |
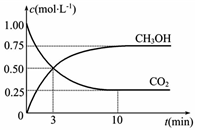 “低碳循环”引起各国的高度重视,已知煤、甲烷等可以与水蒸气反应生成以CO和H2为主的合成气,合成气有广泛应用.试回答下列问题:
“低碳循环”引起各国的高度重视,已知煤、甲烷等可以与水蒸气反应生成以CO和H2为主的合成气,合成气有广泛应用.试回答下列问题: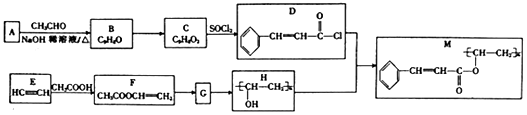
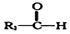 +
+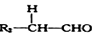 $→_{△}^{NaOH稀溶液}$
$→_{△}^{NaOH稀溶液}$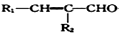 +H2O(R1、R2为羟基或氯)
+H2O(R1、R2为羟基或氯) .
.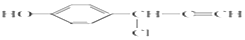 .
.