7.有机化学主要研究有机化合物所发生的反应,下列化合物中不是有机物的是( )
| A. | CO2 | B. | C2H6 | C. | C2H2 | D. | CH3OH |
4.下列说法正确的是( )
| A. | 水分子间存在氢键,所以水常温下以液态存在并且化学性质非常稳定 | |
| B. | 常温、常压下以液态存在的物质一定都是由分子构成,因此该液体一般无法导电 | |
| C. | 硫酸钾在熔融状态下离子键被削弱,形成定向移动的离子,从而导电 | |
| D. | 冰醋酸晶体溶于水的过程中即破坏了分子间作用力,也破坏了部分分子内作用力 |
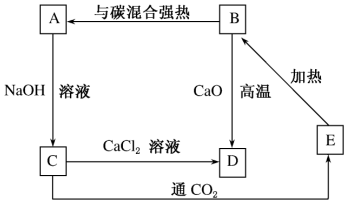
2.下表各组物质中,物质之间不可能实现如图所示转化的是( )

| 选项 | X | Y | Z | M |
| A | Fe | FeCl2 | FeCl3 | Cl2 |
| B | Mg | C | CO | CO2 |
| C | NaOH | NaCO3 | NaHCO3 | CO2 |
| D | NH3 | NO | NO2 | O2 |
| A. | A | B. | B | C. | C | D. | D |
20.下列有关反应热的叙述中正确的是( )
①已知2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ•mol-1,则氢气的燃烧热为△H=-241.8kJ•mol-1
②由单质A转化为单质B是一个吸热过程,由此可知单质B比单质A稳定
③X(g)+Y(g)?Z(g)+W(s)△H>0,恒温恒容条件下达到平衡后加入X,上述反应的△H增大
④已知:
根据上表数据可以计算出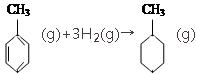 的焓变
的焓变
⑤根据盖斯定律,推知在相同条件下,金刚石或石墨燃烧生成1mol CO2气体时,放出的热量相等
⑥25℃101kPa时,1mol碳完全燃烧生成CO2气体所放出的热量为碳的燃烧热.
①已知2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ•mol-1,则氢气的燃烧热为△H=-241.8kJ•mol-1
②由单质A转化为单质B是一个吸热过程,由此可知单质B比单质A稳定
③X(g)+Y(g)?Z(g)+W(s)△H>0,恒温恒容条件下达到平衡后加入X,上述反应的△H增大
④已知:
| 共价键 | C-C | C═C | C-H | H-H |
| 键能/(kJ•mol-1) | 348 | 610 | 413 | 436 |
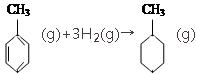 的焓变
的焓变⑤根据盖斯定律,推知在相同条件下,金刚石或石墨燃烧生成1mol CO2气体时,放出的热量相等
⑥25℃101kPa时,1mol碳完全燃烧生成CO2气体所放出的热量为碳的燃烧热.
| A. | ①②③④ | B. | ③④⑤ | C. | ④⑤ | D. | ⑥ |
19.下列有关说法正确的是( )
| A. | 在稀溶液中,H+(aq)+OH-(aq)=H2O(l);△H=-57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热等于57.3kJ | |
| B. | 在一密闭容器中发生反应2SO2+O2?2SO3,增大压强,平衡正向移动,K增大 | |
| C. | 2C(s)+O2(g)═2CO(g)△H=-221 kJ•mol-1,则C的燃烧热△H=-110.5 kJ•mol-1 | |
| D. | 向稀硫酸中加入少量硫酸铜可提高锌与稀硫酸反应生成氢气的速率 |
18.下列实验装置错误的是( )
0 161804 161812 161818 161822 161828 161830 161834 161840 161842 161848 161854 161858 161860 161864 161870 161872 161878 161882 161884 161888 161890 161894 161896 161898 161899 161900 161902 161903 161904 161906 161908 161912 161914 161918 161920 161924 161930 161932 161938 161942 161944 161948 161954 161960 161962 161968 161972 161974 161980 161984 161990 161998 203614
| A. | 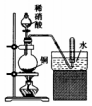 实验室制备NO | B. |  实验室制取NH3 | ||
| C. | 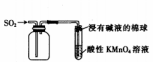 收集SO2并验证其还原性 | D. |  验证铜绿受热分解的酸性气体产物 |
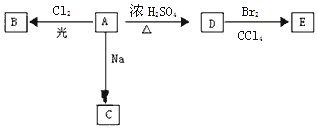
 .
.
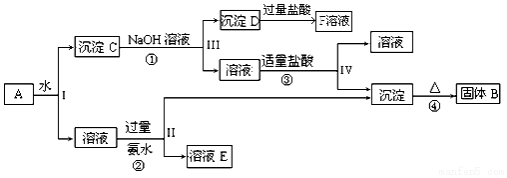
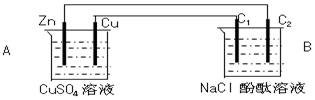 按如图装置进行实验,并回答下列问题
按如图装置进行实验,并回答下列问题