17.下列叙述错误的是( )
| A. | 共价化合物中只含共价键 | |
| B. | 离子化合物中可能含有共价键 | |
| C. | 干冰变为二氧化碳气体,因共价键被破坏需吸收能量 | |
| D. | 碳酸氢铵受热分解产生氨气不仅破坏离子键还破坏了共价键 |
16.下列叙述中,正确的是( )
| A. | 1 mol H2的质量只有在标准状况下才约为2 g | |
| B. | 在标准状况下,22.4 L由N2、N2O组成的混合气体中所含有的氮原子的物质的量约为2 mol | |
| C. | 在20℃时,1 mol任何气体的体积总比22.4 L大 | |
| D. | 1 mol H2和O2的混合气体,在标准状况下的体积大于22.4 L |
15.25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 加入H+能产生无色无味气体的溶液:OH-、K+、I-、SO32- | |
| B. | 在加入铝粉能产生H2的溶液中:NH4+、Fe2+、SO42-、NO3- | |
| C. | 0.1 mol•L-1NH4HCO3溶液中:K+、Na+、NO3-、Cl- | |
| D. | 在澄清透明的无色溶液中:Na+、Cu2+、Cl-、NO3- |
14.下列解释事实的化学(或离子)方程式正确的是( )
| A. | 盛放NaOH溶液的试剂瓶不能用玻璃塞:SiO2+2OH-═SiO32-+H2O | |
| B. | 用食醋检验牙膏中的摩擦剂碳酸钙:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| C. | 用氯化铁溶液腐蚀铜线路板:Cu+Fe3+═Fe2++Cu2+ | |
| D. | 用氢氧化钠溶液去除铝表面的氧化膜:Al2O3+2OH-═2AlO2-+H2↑ |
13.已知:还原性强弱:I->Fe2+.往100mL碘化亚铁溶液中缓慢通入3.36L(标准状况)氯气,反应完成后溶液中有一半的Fe2+被氧化成Fe3+.则原碘化亚铁溶液的物质的量浓度为( )
| A. | 1.1 mol•L-1 | B. | 1.5 mol•L-1 | C. | 1.2 mol•L-1 | D. | 1.0 mol•L-1 |
12.在电解水制取H2和O2时,为了增强导电性,常常在水中加入一些电解质,下列物质可选用( )
| A. | NaCl | B. | CuCl2 | C. | NaOH | D. | CuSO4 |
11.等物物的量的X(g)与Y(g)在密闭容器中进行可逆反应:X(g)+Y(g)?2Z(g)+W(s)△H<0,下列叙述正确的是( )
| A. | 达到平衡后再充入少量X气体,上述反应的△H增大 | |
| B. | 达到平衡时,反应速率v正(X)=2v逆(Z) | |
| C. | 达到平衡后,降低温度,正向反应速率大于逆向反应速率 | |
| D. | 达到平衡后,升高温度或增大压强都有利于该反应平衡向逆反应方向移动 |
10.从海水提取溴的过程中,有如下反应:5NaBr+NaBrO3+3H2SO4═3Br2+3Na2SO4+3H2O,与上述反应在原理上最相似的反应是( )
| A. | 2NaBr+Cl2═Br2+2NaCl | |
| B. | AlCl3+3NaAlO2+6H2O═4Al(OH)3↓+3NaCl | |
| C. | 2H2S+SO2═3S↓+2H2O | |
| D. | Cl2+H2O═HCl+HClO |
9.烷烃C5H12,与氯气发生取代反应所得的一氯取代物没有同分异构体,其结构式为( )
0 161801 161809 161815 161819 161825 161827 161831 161837 161839 161845 161851 161855 161857 161861 161867 161869 161875 161879 161881 161885 161887 161891 161893 161895 161896 161897 161899 161900 161901 161903 161905 161909 161911 161915 161917 161921 161927 161929 161935 161939 161941 161945 161951 161957 161959 161965 161969 161971 161977 161981 161987 161995 203614
| A. | 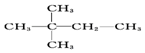 | B. |  | C. | 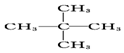 | D. | CH3CH2CH2CH2CH3 |
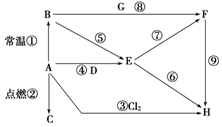 如图表示A~H八种物质的相互转化关系,其中A为金属单质,其余均为化合物,C为淡黄色粉末,D为常见的无色液体,G能使澄清石灰水变浑浊.
如图表示A~H八种物质的相互转化关系,其中A为金属单质,其余均为化合物,C为淡黄色粉末,D为常见的无色液体,G能使澄清石灰水变浑浊.