5.下列选项中的操作、现象与结论完全一致的是( )
| 操作 | 现象 | 结论 | |
| A | 向滴有酚酞的NaOH溶液中通入 Cl2 | 溶液褪色 | HClO有漂白性 |
| B | 无水乙醇与浓硫酸共热至170℃,将产生气体通入溴水 | 溴水褪色 | 乙烯和溴水发生加成反应 |
| C | 向浓度、体积都相同的Na2CO3和NaHCO3溶液中各滴加1滴酚酞 | 变红,前者红色深 | 结合H+能力: CO32->HCO3- |
| D | 用发光小灯泡分别做HCl和CH3COOH导电性实验 | 发光强度:HCl强于CH3COOH | CH3COOH是弱电解质 |
| A. | A | B. | B | C. | C | D. | D |
4.室温下,分别用0.1mol•L-1溶液进行下列实验,结论不正确的是( )
| A. | 向NaOH溶液中通SO2至pH=7:c(Na+)═c(HSO3-)+2c(SO32-) | |
| B. | 向NH4Cl溶液中加入等浓度等体积的NH3•H2O后,所得溶液呈碱性,则:c(NH4+)<c(NH3•H2O) | |
| C. | 向NH4HSO4加入等浓度等体积的NaOH溶液后后:c(NH4+)+c(NH3•H2O)═c(Na+) | |
| D. | 向CH3COOH溶液中加入少量CH3COONa晶体:$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$ 增大 |
3.下列各项中的方程式不能正确解释对应的原因或现象的是( )
| A. | 盛放碱液的试剂瓶不用玻璃塞;SiO2+2OH-═SiO32-+H2O | |
| B. | 配制FeCl3溶液时要加盐酸:Fe3++3H2O?Fe(OH)3+3H+ | |
| C. | 制Cl2时用排饱和氯化钠溶液收集气体:H2O+Cl2?Cl-+H++HClO | |
| D. | 金属钠燃烧时,火焰呈黄色:2Na+O2 $\frac{\underline{\;点燃\;}}{\;}$Na2O2 |
20.向某溶液中加入AgNO3溶液有白色沉淀生成,过滤,向沉淀中加入足量稀HNO3,沉淀部分溶解,产生无色无味气体,将该气体通入澄清石灰水,石灰水变浑浊,由此判断该溶液中一定含有( )
| A. | Cl-、SO42- | B. | NO3-、CO32- | C. | Cl-、SO32- | D. | Cl-、CO32- |
19.第3周期某主族元素的原子,在同周期中它的第一电离能仅大于Na,下列关于此元素的叙述正确的是( )
| A. | 该元素的单质能在CO2中燃烧 | |
| B. | 该元素的氢氧化物具有两性 | |
| C. | 该元素的原子半径比钠的原子半径大 | |
| D. | 1mol该元素的单质可与酸反应产生1molH2 |
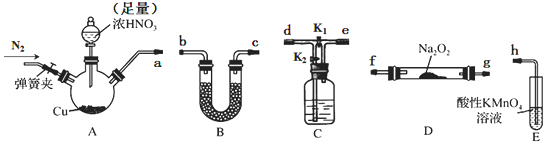
18.工业上常用亚硝酸钠(NaNO2)作媒染剂、漂白剂、钢材缓蚀剂、金属热处理剂.某兴趣小组用下列装置制备NaNO2并探究NO、NO2的某一化学性质(A中加热装置已略去).
已知:
①2NO+Na2O2═2NaNO2;
②NO能被酸性KMnO4氧化成NO3-,MnO4-被还原为Mn2+.
请回答下列问题:
(1)装置A三颈烧瓶中发生反应的化学方程式为Cu+4HNO3(浓)=Cu(NO3)2+4NO2↑+2H2O.
(2)用图中的装置制备NaNO2,其连接顺序为:a→debcfg(b与c、f与g可以交换→h(按气流方向,用小写字母表示),此时活塞K1、K2如何操作关闭K1,打开K2.
(3)E装置发生反应的离子方程式是3MnO4-+4H++5NO=3Mn2++5NO3-+2H2O.
(4)通过查阅资料,NO2或NO可能与溶液中Fe2+发生反应.某同学选择上述装置并按A→C→E顺序连接,E中装入FeSO4溶液,进行如下实验探究.
步骤②操作的目的是排尽装置中残留的NO2;步骤③C瓶中发生的化学方程式为3NO2+H2O=2HNO3+NO;
通过实验可以得出:NO(填“NO2、NO中的一种或两种”)和溶液中Fe2+发生反应使溶液呈深棕色.

已知:
①2NO+Na2O2═2NaNO2;
②NO能被酸性KMnO4氧化成NO3-,MnO4-被还原为Mn2+.
请回答下列问题:
(1)装置A三颈烧瓶中发生反应的化学方程式为Cu+4HNO3(浓)=Cu(NO3)2+4NO2↑+2H2O.
(2)用图中的装置制备NaNO2,其连接顺序为:a→debcfg(b与c、f与g可以交换→h(按气流方向,用小写字母表示),此时活塞K1、K2如何操作关闭K1,打开K2.
(3)E装置发生反应的离子方程式是3MnO4-+4H++5NO=3Mn2++5NO3-+2H2O.
(4)通过查阅资料,NO2或NO可能与溶液中Fe2+发生反应.某同学选择上述装置并按A→C→E顺序连接,E中装入FeSO4溶液,进行如下实验探究.
| 步骤 | 操作及现象 |
| ① | 关闭K2,打开K1,打开弹簧夹通一段时间的氮气,夹紧弹簧夹,开始A中反应,一段时间后,观察到E中溶液逐渐变为深棕色. |
| ② | 停止A中反应,打开弹簧夹和K2、关闭K1,持续通入N2一段时间. |
| ③ | 更换新的E装置,再通一段时间N2后关闭弹簧夹,使A中反应继续,观察到的现象与步骤①中相同. |
通过实验可以得出:NO(填“NO2、NO中的一种或两种”)和溶液中Fe2+发生反应使溶液呈深棕色.
17.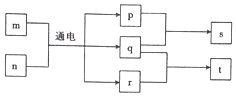 短周期元素W、X、Y、Z的原子序数依次增大,且Y、Z位于同一周期.m、n、s是由这些元素组成的二元化合物,p、q分别是W、Z两元素对应的单质,0.001mol•L-1s溶液的pH为3,t是混合溶液,且该溶液具有漂白性.上述物质的转化关系如图所示.下列说法正确的是( )
短周期元素W、X、Y、Z的原子序数依次增大,且Y、Z位于同一周期.m、n、s是由这些元素组成的二元化合物,p、q分别是W、Z两元素对应的单质,0.001mol•L-1s溶液的pH为3,t是混合溶液,且该溶液具有漂白性.上述物质的转化关系如图所示.下列说法正确的是( )
 短周期元素W、X、Y、Z的原子序数依次增大,且Y、Z位于同一周期.m、n、s是由这些元素组成的二元化合物,p、q分别是W、Z两元素对应的单质,0.001mol•L-1s溶液的pH为3,t是混合溶液,且该溶液具有漂白性.上述物质的转化关系如图所示.下列说法正确的是( )
短周期元素W、X、Y、Z的原子序数依次增大,且Y、Z位于同一周期.m、n、s是由这些元素组成的二元化合物,p、q分别是W、Z两元素对应的单质,0.001mol•L-1s溶液的pH为3,t是混合溶液,且该溶液具有漂白性.上述物质的转化关系如图所示.下列说法正确的是( )| A. | 元素Y分别与W、X、Z形成的化合物中一定含有离子键 | |
| B. | 离子半径:X<Y<Z | |
| C. | 由元素W、X组成的化合物中一定只含极性键 | |
| D. | s为强酸,r为弱碱 |
16.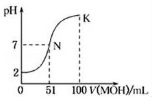 常温下,向100mL 0.01mol•L-1HA溶液中逐滴加入0.02mol•L-1的MOH溶液,图中所示曲线表示混合溶液的pH变化情况,下列说法不正确的是( )
常温下,向100mL 0.01mol•L-1HA溶液中逐滴加入0.02mol•L-1的MOH溶液,图中所示曲线表示混合溶液的pH变化情况,下列说法不正确的是( )
0 161766 161774 161780 161784 161790 161792 161796 161802 161804 161810 161816 161820 161822 161826 161832 161834 161840 161844 161846 161850 161852 161856 161858 161860 161861 161862 161864 161865 161866 161868 161870 161874 161876 161880 161882 161886 161892 161894 161900 161904 161906 161910 161916 161922 161924 161930 161934 161936 161942 161946 161952 161960 203614
 常温下,向100mL 0.01mol•L-1HA溶液中逐滴加入0.02mol•L-1的MOH溶液,图中所示曲线表示混合溶液的pH变化情况,下列说法不正确的是( )
常温下,向100mL 0.01mol•L-1HA溶液中逐滴加入0.02mol•L-1的MOH溶液,图中所示曲线表示混合溶液的pH变化情况,下列说法不正确的是( )| A. | HA为一元强酸,MOH为一元弱碱 | |
| B. | N点溶液中离子浓度大小关系为:c(M+)=c(A-)>c(H+)=c(OH-) | |
| C. | N点水的电离程度大于K点水的电离程度 | |
| D. | N→k之间曲线上任意一点都有c(M+)>c(OH-)>c(A-)>c(H+) |



