17.根据所给的信息和标志,判断下列说法错误的是( )
| A | B | C | D |
 | 碳酸氢钠药片 |  |  |
| 如图为铝热反应的实验装置,工业上利用铝热反应大量冶炼金属铁 | 如图现象为丁达尔效应,丁达尔效应可用于鉴别溶液和胶体 | 如图药品属抗酸药,可治疗胃酸过多 | 看到有该标志的丢弃物,应远离并报警 |
| A. | A | B. | B | C. | C | D. | D |
16.某同学通过系列实验探究Mg及其化合物的性质,操作正确且能达到目的是( )
| A. | 将水加入浓硫酸中得到稀硫酸,置镁条于其中探究Mg的活泼性 | |
| B. | 将NaOH溶液缓慢滴入MgSO4溶液中,观察Mg(OH)2沉淀的生成 | |
| C. | 将Mg(OH)2浊液直接倒入已装好滤纸的漏斗中过滤,洗涤并收集沉淀 | |
| D. | 将镁蒸气在氮气中冷却得到镁粉 |
15.研究反应物的化学计量数与产物之间的关系时,使用类似数轴的方法可以收到的直观形象的效果.下列表达不正确的是( )
| A. | 分散质粒子直径与分散系种类: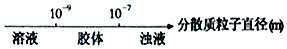 | |
| B. | NaOH溶液与CO2反应后溶液中的钠盐: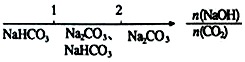 | |
| C. | AlCl3溶液中滴加NaOH溶液后铝的存在形式: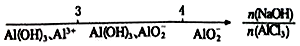 | |
| D. | Na与O2反应的产物: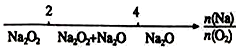 |
14.用NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 相同质量的铝,分别与足量的盐酸和氢氧化钠溶液反应放出的氢气体积一定不相同 | |
| B. | 56gFe与足量盐酸反应转移电子数为3NA | |
| C. | 任何条件下,22.4LNH3与18gH2O所含电子数均为10NA | |
| D. | 46gNO2和N2O4的混合物含有的原子数为3NA |
13.设 NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 10mL 18mol/L 浓硫酸与足量铜加热充分反应,其中有 0.09NA 个 H2SO4 体现 了氧化性 | |
| B. | 将 5.6g 铁在 3.36LCl2 中点燃,二者一定能恰好完全反应 | |
| C. | 100mL 1mol/L 硫酸溶液中,有 0.1mol H2SO4分子 | |
| D. | 标准状况下,22.4 L CO2和 CO 混合气体中含有的碳原 子数约为 NA |
12.下列实验能达到预期目的是( )
| A. | 检验溶液中是否含有 CO32-:滴加稀盐酸,将产生的气体通入澄清石灰水 | |
| B. | 检验溶液中是否含有 NH4+:先滴加浓 NaOH 溶液并加热,再用湿润的红色石 蕊试纸 | |
| C. | 检验溶液中是否含有 Fe2+:先滴加氯水,再滴加 KSCN 溶液 | |
| D. | 检验溶液中是否含有 SO42-:先滴加氯化钡溶液,再滴加稀盐酸 |
11.NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 2 g氢气所含原子数为NA | |
| B. | 常温常压下,1.06gNa2CO3含有的Na+离子数为0.02NA | |
| C. | 在常温常压下,11.2LN2所含原子数为NA | |
| D. | 2.7g金属铝和足量盐酸反应,失去的电子数目为0.2NA |
10.将相同状况下等体积的SO2和Cl2充分混合后,通入加有品红的氯化钡溶液,可观察到的现象是( )
| A. | 褪色但无沉淀 | B. | 不褪色但有沉淀 | ||
| C. | 褪色且有沉淀 | D. | 不褪色也没有沉淀 |
9.下列反应中,不属于氧化还原反应的是( )
0 161712 161720 161726 161730 161736 161738 161742 161748 161750 161756 161762 161766 161768 161772 161778 161780 161786 161790 161792 161796 161798 161802 161804 161806 161807 161808 161810 161811 161812 161814 161816 161820 161822 161826 161828 161832 161838 161840 161846 161850 161852 161856 161862 161868 161870 161876 161880 161882 161888 161892 161898 161906 203614
| A. | 2H2O2═2H2O+O2↑ | B. | 2FeCl2+Cl2═2FeCl3 | ||
| C. | Pb2++2Cl-═PbCl2↓ | D. | Sn2++2Fe3+═Sn4++2Fe2+ |