1.用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,向所得的溶液中加入0.05mol Cu2(OH)2CO3后恰好恢复到电解前的浓度和pH.则电解过程中转移的电子为( )
| A. | 0.1 mol | B. | 0.2 mol | C. | 0.3 mol | D. | 0.4 mol |
20.研究CO2在海洋中的转移和归宿,是当今海洋科学研究的前沿领域.已知CO2溶于海水主要以4种无机碳形式存在,其中HCO3-占95%,请按要求回答:
(1)CO2溶于水转化为HCO3-的方程式为:CO2+H2O?H2CO3,H2CO3?HCO3-+H+,对于此过程能说明已经达到平衡状态的是BD
A.混合体系中的碳总量保持不变 B.混合液的pH保持不变
C.HCO3-与H2CO3的浓度相等 D.HCO3-的百分含量保持不变
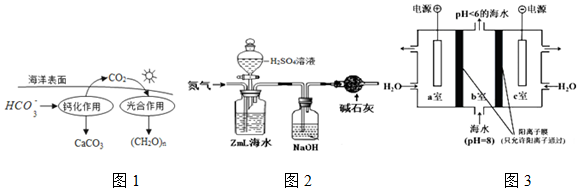
(2)在海洋循环中,通过如图1所示的途径固碳.写出钙化作用的离子方程式:2HCO3-+Ca2+=CaCO3↓+CO2↑+H2O.
(3)海水中溶解无机碳占海水总碳的95%以上,其准确测量是研究海洋碳循环的基础,测量溶解无机碳,可采用如下方法:
①气提、吸收CO2.用N2从酸化后的海水中吹出CO2并用碱液吸收(装置示意图如图2),该装置中干燥管的作用是防止空气中的二氧化碳进入被氢氧化钠溶液吸收.
②滴定.若Z mL海水中的无机碳恰好使NaOH吸收液完全转化为200mL的NaHCO3溶液,再用ymol/L的标准盐酸溶液滴定,有关数据记录如表:
根据相关数据,计算海水中溶解的无机碳的浓度$\frac{200y}{Z}$mol/L
(4)利用如图3所示装置从海水中提取CO2,有利于减少环境温室气体含量,结合方程式简述提取CO2的原理a室:2H2O-4e=4H++O2↑,氢离子通过阳离子交换膜进入b室,发生反应:H++HCO3-=CO2↑+H2O.
(1)CO2溶于水转化为HCO3-的方程式为:CO2+H2O?H2CO3,H2CO3?HCO3-+H+,对于此过程能说明已经达到平衡状态的是BD

A.混合体系中的碳总量保持不变 B.混合液的pH保持不变
C.HCO3-与H2CO3的浓度相等 D.HCO3-的百分含量保持不变
(2)在海洋循环中,通过如图1所示的途径固碳.写出钙化作用的离子方程式:2HCO3-+Ca2+=CaCO3↓+CO2↑+H2O.
(3)海水中溶解无机碳占海水总碳的95%以上,其准确测量是研究海洋碳循环的基础,测量溶解无机碳,可采用如下方法:
①气提、吸收CO2.用N2从酸化后的海水中吹出CO2并用碱液吸收(装置示意图如图2),该装置中干燥管的作用是防止空气中的二氧化碳进入被氢氧化钠溶液吸收.
②滴定.若Z mL海水中的无机碳恰好使NaOH吸收液完全转化为200mL的NaHCO3溶液,再用ymol/L的标准盐酸溶液滴定,有关数据记录如表:
| 测定序号 | NaHCO3溶液的体积/mL | 盐酸标准液滴定管中的读数/mL | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 1.50 | 21.52 |
| 2 | 20.00 | 1.80 | 25.62 |
| 3 | 20.00 | 0.20 | 20.18 |
(4)利用如图3所示装置从海水中提取CO2,有利于减少环境温室气体含量,结合方程式简述提取CO2的原理a室:2H2O-4e=4H++O2↑,氢离子通过阳离子交换膜进入b室,发生反应:H++HCO3-=CO2↑+H2O.
19.将两个铂电极插入KOH溶液中,向两极分别通入CH4和O2,构成甲烷燃料电池.已知,通入CH4的一极,其电极反应式是CH4+10OH--8e-═CO32-+7H2O,下列叙述不正确的是( )
| A. | 正极发生还原反应 2O2+4H2O+8e-═8OH- | |
| B. | 通入CH4的电极为负极 | |
| C. | 该电池使用一段时间后应补充KOH | |
| D. | 燃料电池工作时,溶液中的OH-向正极移动 |
18.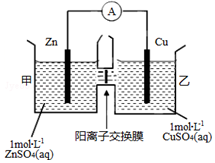 锌铜原电池装置如图所示,中间被阳离子交换膜隔开且只允许阳离子和水分子通过,下列有关叙述正确的是( )
锌铜原电池装置如图所示,中间被阳离子交换膜隔开且只允许阳离子和水分子通过,下列有关叙述正确的是( )
 锌铜原电池装置如图所示,中间被阳离子交换膜隔开且只允许阳离子和水分子通过,下列有关叙述正确的是( )
锌铜原电池装置如图所示,中间被阳离子交换膜隔开且只允许阳离子和水分子通过,下列有关叙述正确的是( )| A. | 铜电极上发生氧化反应 | |
| B. | 外电路中电子由Cu流向Zn | |
| C. | 电池工作一段时间后,乙池溶液的总质量增加 | |
| D. | 电池工作一段时间后,甲池的C(SO42-)增大 |
17.下列离子组不能在溶液中大量共存并会同时产生沉淀和气体的是( )
| A. | Fe2+、NO3-、K+、Cl- | B. | K+、Al3+、HCO3-、Cl- | ||
| C. | H+、Ca2+、HCO3-、Cl- | D. | Ca2+、HCO3-、OH-、NO3- |
16.已知反应:
①2CH3OH(g)?CH3OCH3(g)+H2O(g)△H1=-23.9kJ/mol
②2CH3OH(g)═C2H4(g)+2H2O(g)△H2=-29.1kJ/mol
③CH3CH2OH(g)═CH3OCH3(g)△H3=+50.7kJ/mol
在C2H4(g)+H2O(g)=CH3CH2OH(g)△H4中,△H4等于( )
①2CH3OH(g)?CH3OCH3(g)+H2O(g)△H1=-23.9kJ/mol
②2CH3OH(g)═C2H4(g)+2H2O(g)△H2=-29.1kJ/mol
③CH3CH2OH(g)═CH3OCH3(g)△H3=+50.7kJ/mol
在C2H4(g)+H2O(g)=CH3CH2OH(g)△H4中,△H4等于( )
| A. | -48.5kJ/mol | B. | +48.5kJ/mol | C. | -45.5kJ/mol | D. | +45.5kJ/mol |
15.如图是一些常见有机物的转化关系,关于反应①~⑦的说法不正确的是( )
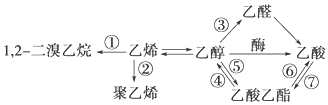

| A. | 反应①是加成反应 | B. | 只有反应②是加聚反应 | ||
| C. | 只有反应⑦是取代反应 | D. | 反应③是氧化反应 |
13.可逆反应mA(s)+nB(g)?eC(g)+fD(g),反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(p)的关系如图.下列叙述正确的是( )
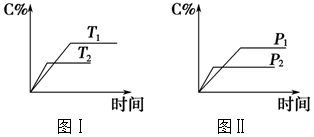

| A. | 化学方程式中m+n<e+f | |
| B. | 达平衡后,若升温,平衡左移 | |
| C. | 达平衡后,加入催化剂则C%增大 | |
| D. | 达平衡后,增加A的量有利于平衡向右移动 |
12.下列有关说法正确的是( )
0 161679 161687 161693 161697 161703 161705 161709 161715 161717 161723 161729 161733 161735 161739 161745 161747 161753 161757 161759 161763 161765 161769 161771 161773 161774 161775 161777 161778 161779 161781 161783 161787 161789 161793 161795 161799 161805 161807 161813 161817 161819 161823 161829 161835 161837 161843 161847 161849 161855 161859 161865 161873 203614
| A. | 常温下,0.1 mol•L-1 NH4Cl溶液的pH=1 | |
| B. | 工业上电解饱和食盐水时,以石墨为阴极,铁棒为阳极 | |
| C. | 反应CO2(g)+C(s)═2CO(g)在高温下可自发进行,则该反应的△H>0 | |
| D. | 常温下,在AgCl悬浊液中加入少量NaCl饱和溶液,[Ag+]减小,Ksp(AgCl)减小 |