12.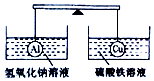 在杠杆的两端分别挂着质量和体积都相同的空心铝球和铜球,此时杠杆平衡.然后将两球分别浸没在氢氧化钠溶液和硫酸铁溶液中片刻,如图,则下列说法正确的是( )
在杠杆的两端分别挂着质量和体积都相同的空心铝球和铜球,此时杠杆平衡.然后将两球分别浸没在氢氧化钠溶液和硫酸铁溶液中片刻,如图,则下列说法正确的是( )
 在杠杆的两端分别挂着质量和体积都相同的空心铝球和铜球,此时杠杆平衡.然后将两球分别浸没在氢氧化钠溶液和硫酸铁溶液中片刻,如图,则下列说法正确的是( )
在杠杆的两端分别挂着质量和体积都相同的空心铝球和铜球,此时杠杆平衡.然后将两球分别浸没在氢氧化钠溶液和硫酸铁溶液中片刻,如图,则下列说法正确的是( )| A. | 两烧杯中均无气泡产生 | B. | 左边烧杯中的溶液质量增加了 | ||
| C. | 在浸没过程中,杠杆始终保持平衡 | D. | 右边铜球质量不变 |
11.含有11.2g KOH的稀溶液与1L 0.1mol/L的H2SO4溶液反应,放出11.46kJ的热量,表示该反应中和热的化学方程式为( )
| A. | KOH(aq)+$\frac{1}{2}$H2SO4(aq)═$\frac{1}{2}$K2SO4(aq)+H2O(l)△H=-11.46 kJ/mol | |
| B. | 2KOH(aq)+H2SO4(aq)═K2SO4(aq)+2H2O(l)△H=-11.46 kJ/mol | |
| C. | 2KOH(aq)+H2SO4(aq)═K2SO4(aq)+2H2O(l)△H=-114.6 kJ/mol | |
| D. | KOH(aq)+$\frac{1}{2}$H2SO4(aq)═$\frac{1}{2}$K2SO4(aq)+H2O(l)△H=-57.3 kJ/mol |
9.下列说法或化学用语表达正确的是( )
| A. | s能级的原子轨道呈球形,处在该轨道上的电子只能在球壳内运动 | |
| B. | p能级的原子轨道呈纺锤形,随着能层的增加,p能级原子轨道也在增多 | |
| C. | 某原子的电子排布式为1s22s2 2p63s2 3p63d54s1属于激发态 | |
| D. | Fe2+的电子排布式为1s22s2 2p63s2 3p63d6 |
8.已知20°C时AgBr的溶解度为8.4×10-6AgCl的溶解度为1.5×10-4将AgCl与AgBr的饱和溶液等体积混合,再加入足量浓硝酸银,发生的反应为( )
| A. | AgCl沉淀多于AgBr沉淀 | B. | AgCl和AgBr沉淀等量生成 | ||
| C. | AgCl沉淀少于AgBr沉淀 | D. | 只有AgBr沉淀生成 |
5.CO2与NO混合气体VL,通过足量Na2O2充分反应后,剩余气体体积可能为(假设NO与Na2O2不发生反应,不考虑NO2与N2O4相互转化)( )
| A. | $\frac{V}{2}$L | B. | $\frac{V}{3}$L | C. | $\frac{5V}{6}$L | D. | VL |
4. 向20mL0.5mol•L-1的醋酸溶液中逐滴加入等物质的量浓度的烧碱溶液,测定混合溶液的温度变化如图所示.下列关于混合溶液的说法,错误的是( )
向20mL0.5mol•L-1的醋酸溶液中逐滴加入等物质的量浓度的烧碱溶液,测定混合溶液的温度变化如图所示.下列关于混合溶液的说法,错误的是( )
 向20mL0.5mol•L-1的醋酸溶液中逐滴加入等物质的量浓度的烧碱溶液,测定混合溶液的温度变化如图所示.下列关于混合溶液的说法,错误的是( )
向20mL0.5mol•L-1的醋酸溶液中逐滴加入等物质的量浓度的烧碱溶液,测定混合溶液的温度变化如图所示.下列关于混合溶液的说法,错误的是( )| A. | 溶液pH:b>c>a | |
| B. | a点:c(H+)-c(OH-)=$\frac{1}{2}$[c(CH3COO-)-c(CH3COOH)] | |
| C. | a到b,溶液中可能存在:c(CH3COO-)=c(Na+) | |
| D. | b到c,溶液中可能存在:c(CH3COO-)=c(OH-) |
3.已知:草酸又名乙二酸,其一级电离常数Ka1=5.9×10-2,二级电离常数Ka2=6.4×10-5.常温下,向10mL 0.01mol•L-1 NaHC2O4溶液中滴加0.01mol•L-1 NaOH溶液,随着NaOH溶液体积的增加,溶液中离子浓度关系正确的是( )
0 161627 161635 161641 161645 161651 161653 161657 161663 161665 161671 161677 161681 161683 161687 161693 161695 161701 161705 161707 161711 161713 161717 161719 161721 161722 161723 161725 161726 161727 161729 161731 161735 161737 161741 161743 161747 161753 161755 161761 161765 161767 161771 161777 161783 161785 161791 161795 161797 161803 161807 161813 161821 203614
| A. | V(NaOH)=10时,c(OH-)+c(H2C2O4)═c(C2O42-)+c(H+) | |
| B. | V(NaOH)=100 mL时,可能存在c(Na+)>2c(C2O42-)+c(HC2O4-) | |
| C. | V(NaOH)=1000 mL时,c(Na+)>c(HC2O4-)>c(C2O42-)>c(H2C2O4) | |
| D. | V(NaOH)=10 mL时,溶液中c(H+)=1×10-12 mol/L |