7.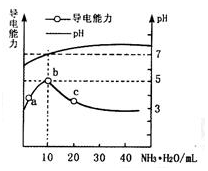 常温下,向10mL 0.1mol•L-1的HR溶液中逐滴滴入0.1mol•L-1的NH3•H2O溶液,所得溶液pH及导电能力变化如图.下列分析不正确的是( )
常温下,向10mL 0.1mol•L-1的HR溶液中逐滴滴入0.1mol•L-1的NH3•H2O溶液,所得溶液pH及导电能力变化如图.下列分析不正确的是( )
 常温下,向10mL 0.1mol•L-1的HR溶液中逐滴滴入0.1mol•L-1的NH3•H2O溶液,所得溶液pH及导电能力变化如图.下列分析不正确的是( )
常温下,向10mL 0.1mol•L-1的HR溶液中逐滴滴入0.1mol•L-1的NH3•H2O溶液,所得溶液pH及导电能力变化如图.下列分析不正确的是( )| A. | a~b点导电能力增强,说明HR为弱酸 | B. | b点溶液pH=7,此时酸碱恰好中和 | ||
| C. | c点溶液存在c(NH4+)>c(R-)、c(OH-)>c(H+) | D. | b、c两点水的电离程度:b<c |
6.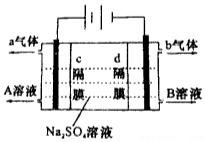 双隔膜电解池的结构示意简图如图所示,利用该装置可以电解硫酸钠溶液以制取硫酸和氢氧化钠,并得到氢气和氧气.对该装置及其原理判断正确的是( )
双隔膜电解池的结构示意简图如图所示,利用该装置可以电解硫酸钠溶液以制取硫酸和氢氧化钠,并得到氢气和氧气.对该装置及其原理判断正确的是( )
 双隔膜电解池的结构示意简图如图所示,利用该装置可以电解硫酸钠溶液以制取硫酸和氢氧化钠,并得到氢气和氧气.对该装置及其原理判断正确的是( )
双隔膜电解池的结构示意简图如图所示,利用该装置可以电解硫酸钠溶液以制取硫酸和氢氧化钠,并得到氢气和氧气.对该装置及其原理判断正确的是( )| A. | a气体为氢气,b气体为氧气 | |
| B. | A溶液为NaOH,B为H2SO4 | |
| C. | c隔膜为阳离子交换膜、d隔膜为阴离子交换膜 | |
| D. | 该电解反应的总方程式可以表示为:2Na2SO4+6H2O$\frac{\underline{\;通电\;}}{\;}$2H2SO4+4NaOH+O2↑+2H2↑ |
5.X、Y、Z、M、N属于短周期元素,且原子序数依次增大、X、M同主族,可形成离子化合物MX,Z、N同主族,可形成NZ2、NZ3两种分子,Y与X形成的一种气态化合物在标准状况下的密度为0.76g/L.下列说法不正确的是( )
| A. | M与Z形成的化合物阳、阴离子个数比均为2:1 | |
| B. | X与Z形成的某种化合物与NZ2反应可生成一种强酸 | |
| C. | Y的含氧酸是强酸 | |
| D. | Z、M、N三种元素组成的某种化合物可与N的最高价氧化物的水化物反应生成N的氧化物 |
4.下列离子方程式的书写及评价,均合理的是( )
| 选项 | 离子方程式 | 评价 |
| A | 将2molCl2通入到含lmolFeI2的溶液中:2Fe2++2I-+2Cl2═2Fe3++I2+4Cl- | 正确:Cl2过量,可将Fe2+、I-均氧化 |
| B | 稀硝酸中加过量铁粉:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O | 正确:过量的Fe还原了Fe3+ |
| C | 过量SO2通入到NaClO 溶液中:ClO-+SO2+H2O═HSO3-+HClO | 正确:说明酸性:H2SO3强于HClO |
| D | Mg(HCO3)2溶液与足量的NaOH 溶液反应:Mg2++HCO3-+OH-═MgCO3↓+H2O+CO32- | 正确:酸式盐与碱反应生成正盐和水 |
| A. | A | B. | B | C. | C | D. | D |
3.若NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 含lmolH2SO4的浓硫酸与足量铜在加热条件下反应,转移的电子总数为NA | |
| B. | 0.1 L0.5mol/LCH3COOH 溶液中含有的氢离子为0.05NA | |
| C. | 粗铜精炼时阳极质量减少6.4g,则外电路上通过0.2NA电子 | |
| D. | 1molCH3COONa和少量CH3COOH溶于水所得到的中性溶液中,CH3COO-的数目为NA |
2.将氢气、甲烷、乙醇等物质在氧气中嫩烧时的化学能直接转化为电能的装置叫燃料电池.此种电池能量利用率可高达80%,产物污染也少.下列有关燃料电池说法错误的是( )
| A. | 上述燃料电池的负极反应材料是氢气、甲烷、乙醇等物质 | |
| B. | 氮氧燃料电池常用于肮天飞行器,原因之一是该电池的产物为水,经过处理之后可供宇肮员使用 | |
| C. | 乙醇燃料电池的常用KOH溶液,该电池的负极反应为C2H5OH-12e-+3H2O═CO2↑+12H+ | |
| D. | 甲烷碱性燃料电池工作时OH-定向移动到负极 |
1.下列说法中,正确的是( )
①纯铁不容易生锈
②Na2O2可用作潜水艇供氧剂
③铝在空气中耐腐蚀,所以铝是不活泼金属
④缺钙会引起骨质疏松,缺铁会引起贫血
⑤泡沫灭火器是利用Al2(SO4)3和饱和碳酸钠溶液混合产生的CO2来灭火
⑥Al2O3、MgO均是很好的耐火材料
⑦明矾是净水剂,可杀菌消毒.
①纯铁不容易生锈
②Na2O2可用作潜水艇供氧剂
③铝在空气中耐腐蚀,所以铝是不活泼金属
④缺钙会引起骨质疏松,缺铁会引起贫血
⑤泡沫灭火器是利用Al2(SO4)3和饱和碳酸钠溶液混合产生的CO2来灭火
⑥Al2O3、MgO均是很好的耐火材料
⑦明矾是净水剂,可杀菌消毒.
| A. | ①②④⑥ | B. | ②④⑤⑦ | C. | ③④⑥⑦ | D. | ②④⑤⑥ |
19.常温下,下列有关叙述正确的是( )
| A. | NaB溶液的pH=8,c(Na+)-c(B-)=0.99×10-5mol/L | |
| B. | Na2CO3溶液中,2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) | |
| C. | pH相等的①NH4Cl、②(NH4)2SO4、③NH4HSO4三种溶液中,c(NH4+)大小顺序为:①=②>③ | |
| D. | 10 mL pH=12的氢氧化钠溶液中加入pH=2的HA至pH刚好等于7,所得溶液体积V(总)≥20mL |
18.如图1为甲烷和O2构成的燃料电池示意图,电解质为KOH溶液,图2为电解AlCl3溶液的装置,电极材料均为石墨.用该装置进行实验,反应开始后观察到x电极附近出现白色沉淀.下列说法正确的是( )
0 161591 161599 161605 161609 161615 161617 161621 161627 161629 161635 161641 161645 161647 161651 161657 161659 161665 161669 161671 161675 161677 161681 161683 161685 161686 161687 161689 161690 161691 161693 161695 161699 161701 161705 161707 161711 161717 161719 161725 161729 161731 161735 161741 161747 161749 161755 161759 161761 161767 161771 161777 161785 203614

| A. | A处通入的气体为CH4,电极反应式为:CH4+10OH--8e-═CO32-+7H2O | |
| B. | 图2中电解AlCl3溶液的总反应为:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH- | |
| C. | 图1中电解质溶液的pH增大 | |
| D. | 电解池中Cl-向x极移动 |
