4.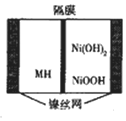 一种新型金属氢化物镍电池(MH-Ni电池,MH为贮氢材料)工作原理如图所示.下列有关说法正确的是( )
一种新型金属氢化物镍电池(MH-Ni电池,MH为贮氢材料)工作原理如图所示.下列有关说法正确的是( )
 一种新型金属氢化物镍电池(MH-Ni电池,MH为贮氢材料)工作原理如图所示.下列有关说法正确的是( )
一种新型金属氢化物镍电池(MH-Ni电池,MH为贮氢材料)工作原理如图所示.下列有关说法正确的是( )| A. | 隔膜为阴离子交换膜 | |
| B. | 电池的电解液可为硫酸 | |
| C. | 充电时阳极反应为H2O+M+e-═MH+OH- | |
| D. | 放电时负极反应为Ni(OH)2+OH--e-═NiOOH+H2O |
3.根据下列实验操作预测的实验现象正确的是( )
| A | 实验操作 | 预测的实验现象 |
| B | 向Na2CO3溶液中滴加盐酸 | 立即有气体逸出 |
| C | 将浓硫酸滴加到盛有铜片的试管中,并将蘸有品红溶液的试纸置于试管口 | 试纸褪色 |
| D | 铅箔在酒精灯火焰上加热 | 铝熔化但不会滴下 |
| 向淀粉的水解液中加入新制Cu(OH)2悬浊液并加热 | 一定有砖红色沉淀生成 |
| A. | A | B. | B | C. | C | D. | D |
2.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,2.24L丁烷中C-C键数目为0.4NA | |
| B. | 0.1mol葡萄糖分子中官能团数目为0.6NA | |
| C. | 28g N2和NO组成的混合物中分子数目可能为0.9NA | |
| D. | 1L pH=13的NaOH溶液中,Na+数目为0.1NA |
1.下列有关材料的说法错误的是( )
| A. | 铁制品在潮湿空气中更易锈蚀 | |
| B. | 二氧化硅常用于制造光导纤维 | |
| C. | 实验室中经过滤可得到纳米碳酸钙固体 | |
| D. | 聚乙烯可作食品包装材料 |
18.短周期主族元素W、X、Y、Z原子序数依次增大,W是原子半径最小的短周期元素,W、Y同主族,X、Z同主族,且X、Z的原子序数之和是W、Y原子序数之和的2倍,下列叙述不正确的是( )
| A. | W和X形成的化合物可能含有非极性共价键 | |
| B. | X和Z形成的化合物常温下可能为固态 | |
| C. | W、X、Y、Z四种元素组成的化合物的水溶液可能呈酸性 | |
| D. | W、X、Y、Z四种元素两两之间均能形成化合物 |
17.有关胶体与溶液的说法正确的是( )
0 161533 161541 161547 161551 161557 161559 161563 161569 161571 161577 161583 161587 161589 161593 161599 161601 161607 161611 161613 161617 161619 161623 161625 161627 161628 161629 161631 161632 161633 161635 161637 161641 161643 161647 161649 161653 161659 161661 161667 161671 161673 161677 161683 161689 161691 161697 161701 161703 161709 161713 161719 161727 203614
| A. | 胶体粒子带电,溶液溶质粒子不带电 | |
| B. | 渗析实验可以鉴别胶体和溶液 | |
| C. | 胶体与溶液都可以通过滤纸、半透膜和分子筛 | |
| D. | 丁达尔效应可以区分胶体和溶液 |
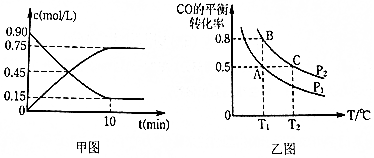
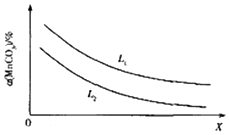 MnO2是常见的氧化剂、催化剂和活性电极材料.
MnO2是常见的氧化剂、催化剂和活性电极材料.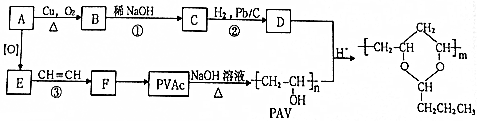

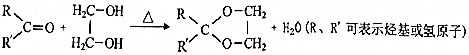
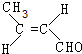 ,该分子中最多有9个原子共平面;
,该分子中最多有9个原子共平面; $→_{△}^{NaOH}$
$→_{△}^{NaOH}$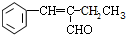 +H2O;
+H2O;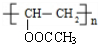 ;
;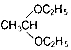 .
.
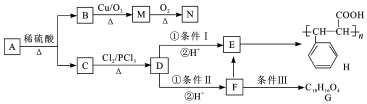
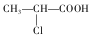 +HCl
+HCl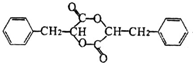 .
.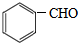 +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$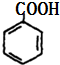 +Cu2O↓+2H2O.
+Cu2O↓+2H2O.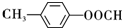 .
.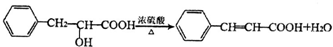 .
.