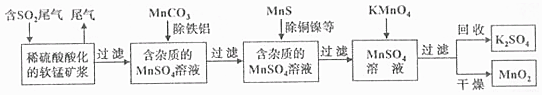
15.25℃时,下列溶液中的微粒浓度关系正确的是( )
| A. | pH=3的0.1mol•L-1的NaHC2O4溶液中:c(C2O42-)<c(H2C2O4) | |
| B. | 0.1mol•L-1的Na2S溶液中:2c(Na+)=c(S2-)+c(HS-)+c(H2S) | |
| C. | pH=4的CH3COOH溶液中:$\frac{c(O{H}^{-})}{c({H}^{+})}$=1×10-10 | |
| D. | 等物质的量浓度、等体积的NaF溶液和HF溶液混合所得的稀溶液中:c(H+)+c(Na+)=c(F-)+c(OH-) |
14.相同质量的下列烃,在空气中充分燃烧产生二氧化碳最少的是( )
| A. | C2H2 | B. | C3H6 | C. | C4H10 | D. | C6H6 |
13.如图是温度和压强对反应 X+Y?2Z 影响的示意图.下列叙述正确的是( )
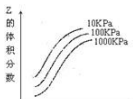

| A. | 上述可逆反应的正反应为放热反应 | |
| B. | X、Y、Z 均为气态 | |
| C. | X 和 Y 中只有一种是气态,Z 为气态 | |
| D. | 上述反应的正反应的△S<0 |
12.12mol/L的盐酸50ml与足量的MnO2在加热条件下反应,可以制得的Cl2的物质的量为( )
| A. | 0.3mol | B. | 小于0.15mol | C. | 0.15~0.3mol | D. | 0.15mol |
10.500mL KNO3和Cu(NO3)2的混合溶液中c(NO3-)=6.0mol•L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4L气体(标准状况),假定电解后溶液体积仍为500mL,下列说法正确的是( )
| A. | 原混合溶液中c(K+)为1 mol•L-1 | |
| B. | 上述电解过程中共转移4 mol电子 | |
| C. | 电解得到的Cu的物质的量为0.5 mol | |
| D. | 电解后溶液中c(H+)为2 mol•L-1 |
9.己知常温常压下.P2和P4燃烧的热化学方程式分别为:
2P2(g)+5O2(g)=P4O10(s)△H=-2695.4kJ/mol
P4(g)+5O2(g)=P4O10(s)△H=-2925.1kJ/mol
则下列说法正确的是( )
2P2(g)+5O2(g)=P4O10(s)△H=-2695.4kJ/mol
P4(g)+5O2(g)=P4O10(s)△H=-2925.1kJ/mol
则下列说法正确的是( )
| A. | 2P2(g)=P4(g)△H=-229.7 kJ•mol-1 | B. | P2制P4是放热反应 | ||
| C. | P2比P4更加稳定 | D. | 等质量时P2比P4具有的能量高 |
8.下列关于能量变化的说法不正确的是( )
0 161520 161528 161534 161538 161544 161546 161550 161556 161558 161564 161570 161574 161576 161580 161586 161588 161594 161598 161600 161604 161606 161610 161612 161614 161615 161616 161618 161619 161620 161622 161624 161628 161630 161634 161636 161640 161646 161648 161654 161658 161660 161664 161670 161676 161678 161684 161688 161690 161696 161700 161706 161714 203614
| A. | 冰融化成水放出热量 | |
| B. | 化学键断裂过程一定放出能量 | |
| C. | 生成物的总能量一定低于反应物的总能量 | |
| D. | 化学键的断裂和形成是化学反应中能量变化的主要原因 |
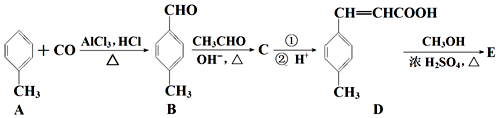
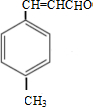 ;D→E的反应类型为酯化反应.
;D→E的反应类型为酯化反应.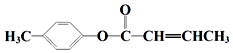 是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为
是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为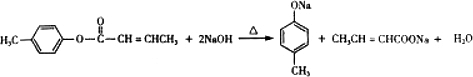 .
. .
.