4.在体积不变的绝热密闭容器中,一定量SO2与1molO2在催化剂作用下发生反应:2SO2(g)+O2(g)$?_{加热}^{催化剂}$2SO3(g)△H=-QkJ/mol(Q>0).当气体的物质的量减少0.5mol时反应达到平衡.下列叙述正确的是( )
| A. | 再通入1molO2,平衡正向移动,平衡常数不变 | |
| B. | 降低温度,正反应速率先减小后增大 | |
| C. | 平衡时SO2气体的转化率为50% | |
| D. | 该条件下反应放出0.5QkJ的热量 |
2.碘酸钾是一种白色结晶粉末,无臭无味,酸性条件下碘酸钾是一种较强的氧化剂,与氢碘酸、二氧化硫等还原性物质作用,被还原为单质碘,在碱性介质中,碘酸钾能被氯气、次氯酸盐等氧化为高碘酸钾.碘酸钾在常温下稳定,加热至560℃开始分解.工业生产碘酸钾的流程如下,在反应器中发生反应的化学方程式为:I2+KClO3+H2O→KH(IO3)2+KCl+Cl2↑(未配平)
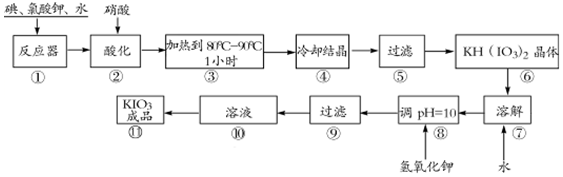
(1)已知步骤①反应器发生的反应中,两种还原产物所得电子数相同,请配平该反应的化学方程式:6I2+11KClO3+3H2O=6KH(IO3)2+5KCl+3Cl2↑;
(2)步骤②中,用稀酸酸化的作用是促进氯气从反应混合物中逸出;
(3)步骤③要保持溶液微沸1小时以完全排出氯气,排出氯气的原因为Cl2能将KIO3氧化成KIO4;
(4)参照下表碘酸钾的溶解度,步骤11得到碘酸钾晶体,你建议的方法是蒸发浓缩、冷却结晶.

(1)已知步骤①反应器发生的反应中,两种还原产物所得电子数相同,请配平该反应的化学方程式:6I2+11KClO3+3H2O=6KH(IO3)2+5KCl+3Cl2↑;
(2)步骤②中,用稀酸酸化的作用是促进氯气从反应混合物中逸出;
(3)步骤③要保持溶液微沸1小时以完全排出氯气,排出氯气的原因为Cl2能将KIO3氧化成KIO4;
(4)参照下表碘酸钾的溶解度,步骤11得到碘酸钾晶体,你建议的方法是蒸发浓缩、冷却结晶.
| 温度/℃ | 0 | 10 | 20 | 40 | 60 | 80 |
| KIO3g/100g水 | 4.60 | 6.27 | 8.08 | 12.6 | 18.3 | 24.8 |
1.下列离子方程式书写不正确的是( )
| A. | 将H2S气体通入Fecl3溶液中:H2S+2Fe3+=2Fe2++S↓+2H+ | |
| B. | Si与NaOH溶液反应:Si+2OH-+H2O=SiO32-+2H2↑ | |
| C. | 将Cl2和SO2体积比1:1同时通入水中:Cl2+SO2+2H2O=4H++SO42-+2Cl- | |
| D. | 将CO2气体通入饱和Na2CO3溶液中:CO2+H2O+CO32-=2HCO3- |
20.对下列实验装置图,有关说法不正确的是( )


| A. | 图甲根据实验现象证明酸性强弱:硝酸>碳酸>硅酸 | |
| B. | 图乙制备金属锰 | |
| C. | 图丙滴定管中溶液的液面读数为22.40mL | |
| D. | 图丁检验乙醇与浓硫酸加热至170℃产生的气体,必须有除杂装置X |
19.下列叙述正确的是( )
| A. | 同质量的H2和Cl2相比,H2的分子数多 | |
| B. | Na2O2的摩尔质量为78g | |
| C. | 0.1molH2SO4含有氢原子数的精确值为1.204×1023 | |
| D. | 1molKCl含有阿伏加德罗常数个KCl分子 |
18.下列实验操作或方法中,正确的是( )
| A. | 海水淡化------蒸馏 | |
| B. | 将碘单质从沙子提取出来--------过滤 | |
| C. | 盐水中获得食盐--------萃取分液 | |
| D. | 稀释浓硫酸时将水慢慢加入浓硫酸中 |
17.下列微粒中,既有氧化性,又有还原性的是( )
| A. | Mg | B. | SO2 | C. | Zn2+ | D. | Cl- |
16.下列事实不能用平衡移动原理解释的是( )
0 161473 161481 161487 161491 161497 161499 161503 161509 161511 161517 161523 161527 161529 161533 161539 161541 161547 161551 161553 161557 161559 161563 161565 161567 161568 161569 161571 161572 161573 161575 161577 161581 161583 161587 161589 161593 161599 161601 161607 161611 161613 161617 161623 161629 161631 161637 161641 161643 161649 161653 161659 161667 203614
| A. | 蒸干AlCl3溶液,无法得到无水AlCl3 | |
| B. | 用稀H2SO4洗涤BaSO4沉淀,可减少沉淀损失量 | |
| C. | 氯水中加入少量CaCO3粉末,可以提高漂白能力 | |
| D. | 滴加CuSO4溶液可以加快Zn与稀H2SO4反应的速率 |
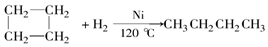
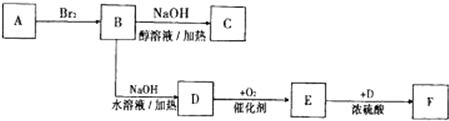
 ;C
;C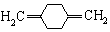 ;
;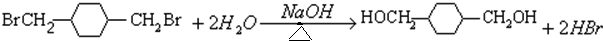 ;E→F:
;E→F: .
.