20.化学与生产生活密切相关,下列物质的用途及解释均正确的是( )
| 选项 | 用途 | 解释 |
| A | 可用FeCl3溶液刻蚀铜制电路板 | Fe3+的氧化性强于Cu2+ |
| B | 碳与石英反应可冶炼粗硅 | 碳的非金属性比硅强 |
| C | 四氯化碳可用于灭火 | 四氯化碳的沸点高 |
| D | 酸性KMnO4溶 液可漂白织物 | KMnO4有强氧化性 |
| A. | A | B. | B | C. | C | D. | D |
19.“2015•8•12”天津港爆炸中有一定量的氰化物泄露.氰化物多数易溶于水,有剧毒,易造成水污染.已知部分弱酸的电离平衡常数如下表:
(1)根据价键规则,写出H2CO3的结构式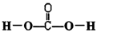 .
.
(2)下列能用于判断氮、碳两种元素非金属性强弱的是abcd(填序号)
a.气态氢化物的稳定性强弱 b.最高价氧化物对应水化物酸性强弱
c.Al2O3+N2+3C=2AlN+3CO d.比较在周期表中的位置
(3)0.01mol/L的NaCN溶液pH=9,用离子方程式表示呈碱性的原因CN-+H2O?HCN+OH-. 请判断该溶液中:c(CN-) c(OH-)(填“>”、“<”或“=”)
(4)含CN-的污水危害很大,处理该污水时,可在催化剂TiO2作用下用NaClO将CN-氧化成CNO-.CNO-在酸性条件下继续被NaClO氧化生成N2与CO2.某环保部门用下图装置进行实验,以证明该处理方法的有效性并测定CN-被处理的百分率.
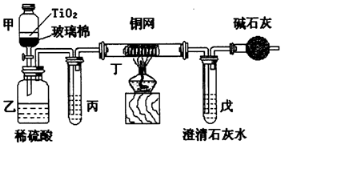
将浓缩后含CN-的废水与过量NaClO溶液的混合液(其中CN-浓度为0.05mol/L)200ml倒入甲中,塞上橡皮塞,一段时间后,打开活塞,使溶液全部放入乙中,关闭活塞.
①甲中反应的离子方程式为CN-+ClO-=CNO-+Cl-,乙中反应的离子方程式为2CNO-+3ClO-+2H+=N2↑+2CO2↑+H2O+3Cl-.
②上述实验是通过测定CO2的量来确定CN-的处理效果.若丙中的试剂是饱和食盐水,且丙、丁都是除杂装置,则乙中产生的气体除CO2、N2外,还可能含有的杂质气体是HCl、Cl2,戊中盛有足量的石灰水,若实验后戊中生成0.9g沉淀,则CN-被处理的百分率为90%.
(5)装置中碱石灰的作用是防止空气中的CO2进入戊,影响对产物的测定.
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | Ki=1.77×10-4 | Ki=5.0×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
 .
.(2)下列能用于判断氮、碳两种元素非金属性强弱的是abcd(填序号)
a.气态氢化物的稳定性强弱 b.最高价氧化物对应水化物酸性强弱
c.Al2O3+N2+3C=2AlN+3CO d.比较在周期表中的位置
(3)0.01mol/L的NaCN溶液pH=9,用离子方程式表示呈碱性的原因CN-+H2O?HCN+OH-. 请判断该溶液中:c(CN-) c(OH-)(填“>”、“<”或“=”)
(4)含CN-的污水危害很大,处理该污水时,可在催化剂TiO2作用下用NaClO将CN-氧化成CNO-.CNO-在酸性条件下继续被NaClO氧化生成N2与CO2.某环保部门用下图装置进行实验,以证明该处理方法的有效性并测定CN-被处理的百分率.

将浓缩后含CN-的废水与过量NaClO溶液的混合液(其中CN-浓度为0.05mol/L)200ml倒入甲中,塞上橡皮塞,一段时间后,打开活塞,使溶液全部放入乙中,关闭活塞.
①甲中反应的离子方程式为CN-+ClO-=CNO-+Cl-,乙中反应的离子方程式为2CNO-+3ClO-+2H+=N2↑+2CO2↑+H2O+3Cl-.
②上述实验是通过测定CO2的量来确定CN-的处理效果.若丙中的试剂是饱和食盐水,且丙、丁都是除杂装置,则乙中产生的气体除CO2、N2外,还可能含有的杂质气体是HCl、Cl2,戊中盛有足量的石灰水,若实验后戊中生成0.9g沉淀,则CN-被处理的百分率为90%.
(5)装置中碱石灰的作用是防止空气中的CO2进入戊,影响对产物的测定.
17.化学与生产、生活、社会密切相关.下列有关说法中不正确的是( )
| A. | 在日常生活中,电化腐蚀是造成钢铁腐蚀的主要原因 | |
| B. | 明矾水解时产生具有吸附性的胶体粒子,可以用于饮用水的杀菌消毒 | |
| C. | SO2具有漂白性,可用于漂白纸浆,但不可以用于漂白食品 | |
| D. | 纯碱可用于生产普通玻璃,日常生活中也可用纯碱溶液来除去物品表面的油污 |
16.下列不能表示2mol HCl的是( )
| A. | 2mol/L的稀盐酸1L | B. | 73gHCl | ||
| C. | 44.8LHCl | D. | 1.204×1024个HCl分子 |
15.下列有关试剂的保存方法,正确的是( )
| A. | 少量金属钠密封保存在水中 | |
| B. | 新制的氯水通常保存在无色试剂瓶中 | |
| C. | 氢氧化钠溶液保存在有玻璃塞的玻璃试剂瓶中 | |
| D. | 氢氟酸保存在塑料瓶中 |
14.某溶液中加入铝粉能产生氢气,在该溶液中可能大量共存的离子组是( )
| A. | SiO32- K+ Fe3+ Cl- | B. | NO3- K+ Mg2+ SO42- | ||
| C. | ClO- Na+ HCO3- SCN- | D. | SO42- Mg2+ Cl- H+ |
13.下列关于物质的用途或变化,说法正确的是( )
0 161455 161463 161469 161473 161479 161481 161485 161491 161493 161499 161505 161509 161511 161515 161521 161523 161529 161533 161535 161539 161541 161545 161547 161549 161550 161551 161553 161554 161555 161557 161559 161563 161565 161569 161571 161575 161581 161583 161589 161593 161595 161599 161605 161611 161613 161619 161623 161625 161631 161635 161641 161649 203614
| A. | 高纯度的硅单质用于制作光导纤维 | |
| B. | Al2O3熔点很高,可用作耐火材料 | |
| C. | SO2可以用来漂白面条 | |
| D. | N2与O2在放电条件下直接化合生成NO2 |
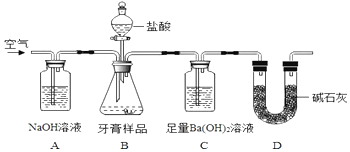 化学兴趣小组对某品牌牙膏中摩擦剂成分及其含量进行以下探究:
化学兴趣小组对某品牌牙膏中摩擦剂成分及其含量进行以下探究: