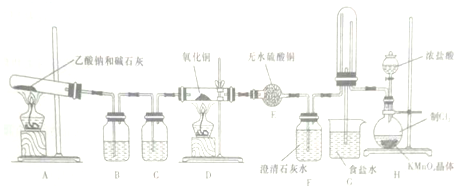
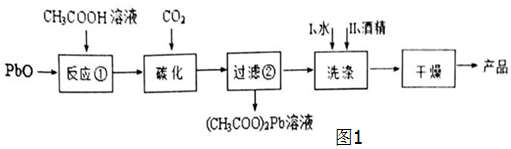
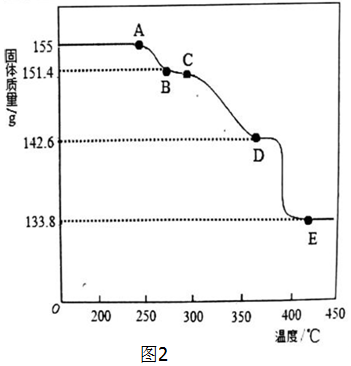
10.NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,3.36L氧气与2.4g碳反应,生成CO2分子数为0.2NA | |
| B. | 标准状况下,1.12LCl2发生反应转移的电子数一定为0.1NA | |
| C. | lL0.lmol•L-1氨水中NH3•H2O分子数为0.1NA | |
| D. | 10g46%酒精(C2H5OH)中含氧原子总数大于0.1NA |
9.下列颜色变化不是因为发生化学变化而产生的是( )
| A. | 漂白粉使某些有机颜料褪色 | |
| B. | 一氧化氮气体在空气中变为红棕色 | |
| C. | 用二氧化硫漂白纸浆、毛、丝、草帽辫等 | |
| D. | 向红墨水中投入活性炭,红色褪去 |
8.下列化合物能用相应元素的单质直接化合生成的是( )
①CuS ②FeS ③Al2S3 ④Fe2S3 ⑤Cu2S ⑥FeCl2 ⑦H2S ⑧FeCl3.
①CuS ②FeS ③Al2S3 ④Fe2S3 ⑤Cu2S ⑥FeCl2 ⑦H2S ⑧FeCl3.
| A. | ②③⑤⑦⑧ | B. | ①④⑥⑦ | C. | ①②③⑦⑧ | D. | ②③⑤⑥⑦⑧ |
7.下列离子方程式书写正确的是( )
| A. | 用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+=Cu2++2Fe2+ | |
| B. | 钠和冷水反应:Na+2H2O=Na++OH-+H2↑ | |
| C. | 将氯气溶于水制备次氯酸:Cl2+H2O=2H++Cl-+ClO- | |
| D. | 氢氧化钡溶液与稀硫酸反应:SO42-+Ba2+=BaSO4↓ |
2.有机物M、N、Q之间的转化关系为 ,下列说法正确的是( )
,下列说法正确的是( )
 ,下列说法正确的是( )
,下列说法正确的是( )| A. | M的同分异构体有3种(不考虑立体异构) | |
| B. | N分子中所有原子共平面 | |
| C. | Q的名称为异丙烷 | |
| D. | M、N、Q均能与Br2反应 |
1.无机化合物可根据其组成和性质进行分类:
(1)Na、K、H、O、C、S、N中任两种或三种元素组成合适的物质,将化学式分别填在表②的后面;(只需填一种)
(2)写出⑦转化为⑧的化学方程式2SO2+O2$\frac{\underline{\;催化剂\;}}{△}$2SO3;
(3)写出Cu和①的浓溶液反应的化学方程式Cu+2H2SO4(浓)═Cu SO4 +SO2↑+2H2O;
(4)实验室制备⑨常用NH4Cl和Ca(OH)2 反应,检验该气体的方法是用湿润的红色石蕊试纸放于试管口,试纸变蓝.
0 161423 161431 161437 161441 161447 161449 161453 161459 161461 161467 161473 161477 161479 161483 161489 161491 161497 161501 161503 161507 161509 161513 161515 161517 161518 161519 161521 161522 161523 161525 161527 161531 161533 161537 161539 161543 161549 161551 161557 161561 161563 161567 161573 161579 161581 161587 161591 161593 161599 161603 161609 161617 203614
(1)Na、K、H、O、C、S、N中任两种或三种元素组成合适的物质,将化学式分别填在表②的后面;(只需填一种)
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
| 化学式 | ①H2SO4 ②HNO3 | ③NaOH ④KOH | ⑤Na2SO4 ⑥K2SO4 | ⑦SO2 ⑧SO3 | ⑨NH3 |
(3)写出Cu和①的浓溶液反应的化学方程式Cu+2H2SO4(浓)═Cu SO4 +SO2↑+2H2O;
(4)实验室制备⑨常用NH4Cl和Ca(OH)2 反应,检验该气体的方法是用湿润的红色石蕊试纸放于试管口,试纸变蓝.
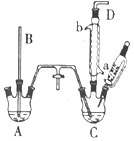 氯苯是重要的有机化工产品,是染料、医药、有机合成的中间体,工业上常用“间歇法”制取.反应原理、实验装置图(加热装置都已略去)如下:
氯苯是重要的有机化工产品,是染料、医药、有机合成的中间体,工业上常用“间歇法”制取.反应原理、实验装置图(加热装置都已略去)如下: +Cl2$\stackrel{FeCl_{3}}{→}$
+Cl2$\stackrel{FeCl_{3}}{→}$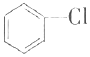 +HCl
+HCl