11.下列离子方程式对应的化学方程式正确的是( )
| A. | H++OH-═H2O CH3COOH+NaOH═CH3COONa+H2O | |
| B. | Ba2++SO42-═BaSO4↓ Ba(OH)2+H2SO4═BaSO4↓+2H2O | |
| C. | CO32-+2H+═CO2↑+H2O CaCO3+2HCl═CaCl2+CO2↑+H2O | |
| D. | Al(OH)3+OH-═AlO2-+2H2O Al(OH)3+NaOH═NaAlO2+2H2O |
10.实验室中配制250mL 0.10mol•L-1NaOH溶液时,必须使用到的玻璃仪器是( )
| A. |  锥形瓶 | B. |  试管 | C. |  分液漏斗 | D. |  容量瓶 |
9.基态原子的4p轨道填充电子为半充满的元素,其原子序数是( )
| A. | 15 | B. | 24 | C. | 33 | D. | 51 |
7.设NA为阿伏加德罗常数的值,下列有关叙述不正确的是( )
| A. | 1 mol甲基(-CH3)所含电子数为9NA | |
| B. | 标准状况下,22.4 L己烷中含氢原子数目为14NA | |
| C. | 标准状况下,B2H6和C2H4的混合气体22.4 L,所含的电子数约为16NA | |
| D. | 26 g C2H2和苯蒸气的混合气体中所含的C原子数为2NA |
6.下列物质中不能使溴水因发生化学反应而褪色,但能使酸性KMnO4溶液褪色的是( )
| A. | 乙烯 | B. | 苯 | C. | 乙苯 | D. | 乙烷 |
5.已知0.1mol•L-1NaHSO3溶液显酸性,且c(SO32-)<c(HSO3-),下列措施不能使溶液中c(SO32-)=c(HSO3-)>0的是.( )
| A. | 加入少量新制氯水 | B. | 加入一定量的小苏打溶液 | ||
| C. | 加入一定量的氢氧化钡固体 | D. | 加入一定量的Na2SO3固体 |
4.25℃时,下列各组离子在相应的条件下可能大量共存的是( )
| A. | 0.1mol•L-1 AlC13溶液中:K+、Na+、HCO3-、SO42- | |
| B. | 能与Al反应生成H2的溶液:NH4+、Ca2+、NO3-、Cl- | |
| C. | 能使pH试纸显深红色的溶液:Fe3+、Cl-、Ba2+、I-、SCN- | |
| D. | $\frac{{K}_{W}}{c(O{H}^{-})}$=10-12mol•L-1的无色溶液中:Na+、CO32-、Cl-、K+ |
3.有关下列四个常用电化学装置的叙述中,正确的是( )
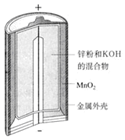 | 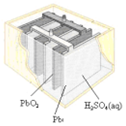 | 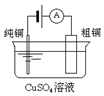 | 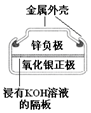 |
| 图Ⅰ碱性锌锰电池 | 图Ⅱ铅蓄电池 | 图Ⅲ电解精炼铜 | 图Ⅳ银锌纽扣电池 |
| A. | 图Ⅰ所示电池中,锌为负极,MnO2的作用是催化剂 | |
| B. | 图II所示电池二氧化铅为正极,放电过程中硫酸浓度不变 | |
| C. | 图III所示装置工作过程中,电解质溶液中Cu2+浓度始终不变 | |
| D. | 图IV所示电池工作过程中,Ag2O是氧化剂 |
2.如图所示,a、b、c、d四个烧杯中都盛有稀硫酸,下列说法正确的是( )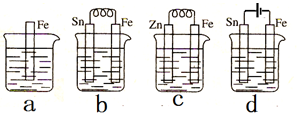
0 161401 161409 161415 161419 161425 161427 161431 161437 161439 161445 161451 161455 161457 161461 161467 161469 161475 161479 161481 161485 161487 161491 161493 161495 161496 161497 161499 161500 161501 161503 161505 161509 161511 161515 161517 161521 161527 161529 161535 161539 161541 161545 161551 161557 161559 161565 161569 161571 161577 161581 161587 161595 203614

| A. | 装置b中Sn极附近溶液的pH将减小 | |
| B. | 装置c中用锌保护铁的方法称为牺牲阴极的阳极保护法 | |
| C. | 装置d中反应的离子方程式为Fe+2H+$\frac{\underline{\;电解\;}}{\;}$Fe2++H2↑ | |
| D. | 图a、b、c、d中纯铁被腐蚀的速率由快到慢的顺序是b>a>c>d |