5.如图是自然界中N、S两种元素的循环过程:根据图内容,判断下列说法正确的是( )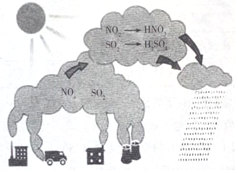

| A. | 图示过程表示了地球臭氧层的破坏过程 | |
| B. | 图中涉及的氧化物均为酸性氧化物 | |
| C. | 机动车尾气含有N的氧化产物 | |
| D. | 图示中描述的过程所涉及的反应均为氧化还原反应 |
4.制取水处理剂C1O2(其部分性质如下表所示)的方法之一是利用草酸(H2C2O4)与氯酸钾反应,反应的化学方程式为2KC1O3+aH2C2O4+H2SO4=2C1O2↑+K2SO4+2CO2↑+bH2O.下列有关该反应的说法不正确的是( )
| 熔点/℃ | 沸点/℃ | 水溶性 |
| -59.5 | 11.0 | 极易溶解 |
| A. | 化学方程式中的a=l,b=2 | |
| B. | 草酸起到还原剂的作用 | |
| C. | KC1O3中只有Cl元素被还原 | |
| D. | 在标准状况下生成5.6L C1O2,转移0.2mol电子 |
3.雾霾严重地威胁着人们生命生存的生态环境.下列有关措施不可行的是( )
| A. | 对燃煤进行脱硫,减少向大气排放SO2 | |
| B. | 对含SO2、NO2等工业废气进行无害处理后,再排放到大气中 | |
| C. | 为增加工业产值,大力兴建水泥厂、炼钢厂 | |
| D. | 对汽车等交通工具采用清洁燃料,如天然气、甲醇等 |
2.下列事实与共价键的强弱有关的是( )
| A. | HF的沸点高于HCl | B. | 金刚石的熔点比晶体硅高 | ||
| C. | 稀有气体一般很难发生化学反应 | D. | 常温下单质溴呈液态、碘呈固态 |
1.下列关于电解质的叙述正确的是( )
| A. | 易溶于水的电解质一定是强电解质 | |
| B. | 强电解质在水溶液中以离子形式存在 | |
| C. | 难溶于水的电解质一定是弱电解质 | |
| D. | 强电解质溶液的导电性一定比弱电解质强 |
20.硫酸氢钠溶于水的过程中( )
| A. | 只破坏离子键 | |
| B. | 既破坏离子键,也破坏共价键 | |
| C. | 只破坏共价键 | |
| D. | 既破坏离子键,也破坏分子间作用力 |
19.关于CH4说法错误的是( )
| A. | 固态时属于分子晶体 | B. | 正四面体结构的分子 | ||
| C. | 与CCl4结构相似、分子间存在氢键 | D. | 含极性键的非极性分子 |
18.CoCl2•6H2O是一种饲料营养强化剂.一种利用水钴矿(主要成分为Co2O3、Co(OH)3,还含少量Fe2O3、Al2O3、MnO等)制取CoCl2•6H2O的工艺流程如图1:
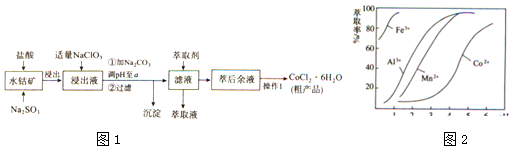
已知:
①浸出液含有的阳离子主要有H+、CO2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表(金属离子浓度为0.01mol/L):
③CoCI2•6H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴.
(1)写出浸出过程中Co2O3发生反应的离子方程式:Co2O3+SO32-+4H+=2Co2++SO42-+2H2O.
(2)写出NaClO3发生反应的主要离子方程式:ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O;若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式:ClO3-+5Cl-+6H+=3Cl2↑+3H2O.
(3)惰性电极电解CoCl2溶液的阳极电极反应式为2Cl--2e-=Cl2↑.(注:横坐标依次为1-6;单位PH)
(4)“操作1”中包含3个基本实验操作,它们依次是蒸发浓缩、冷却结晶和过滤.制得的CoCl2•6H2O在烘干时需减压烘干的原因是降低烘干温度,防止产品分解.
(5)萃取剂对金属离子的萃取率与pH的关系如图向“滤液”中加入萃取剂的目的是除去锰离子,其使用的最佳pH范围是B.
A. 2.0~2.5B. 3.0~3.5C. 4.0~4.5D. 5.0~5.5
(6)力测定粗产品中CoCl2•H2O的含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2•6H2O的质量分数大于100%,其原因可能是粗产品含有可溶性氯化物或晶体失去了部分结晶水.(答一条即可)

已知:
①浸出液含有的阳离子主要有H+、CO2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表(金属离子浓度为0.01mol/L):
| 淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)写出浸出过程中Co2O3发生反应的离子方程式:Co2O3+SO32-+4H+=2Co2++SO42-+2H2O.
(2)写出NaClO3发生反应的主要离子方程式:ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O;若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式:ClO3-+5Cl-+6H+=3Cl2↑+3H2O.
(3)惰性电极电解CoCl2溶液的阳极电极反应式为2Cl--2e-=Cl2↑.(注:横坐标依次为1-6;单位PH)
(4)“操作1”中包含3个基本实验操作,它们依次是蒸发浓缩、冷却结晶和过滤.制得的CoCl2•6H2O在烘干时需减压烘干的原因是降低烘干温度,防止产品分解.
(5)萃取剂对金属离子的萃取率与pH的关系如图向“滤液”中加入萃取剂的目的是除去锰离子,其使用的最佳pH范围是B.
A. 2.0~2.5B. 3.0~3.5C. 4.0~4.5D. 5.0~5.5
(6)力测定粗产品中CoCl2•H2O的含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2•6H2O的质量分数大于100%,其原因可能是粗产品含有可溶性氯化物或晶体失去了部分结晶水.(答一条即可)
17.在100mL的混合液中,硝酸和硫酸的物质的量浓度分别是0.3mol•L-1、0.15mol•L-1,向该混合液中加入2.56g铜粉,加热,待充分反应后,所得溶液中铜离子的物质的量浓度是( )
0 161386 161394 161400 161404 161410 161412 161416 161422 161424 161430 161436 161440 161442 161446 161452 161454 161460 161464 161466 161470 161472 161476 161478 161480 161481 161482 161484 161485 161486 161488 161490 161494 161496 161500 161502 161506 161512 161514 161520 161524 161526 161530 161536 161542 161544 161550 161554 161556 161562 161566 161572 161580 203614
| A. | 0.15 mol•L-1 | B. | 0.225 mol•L-1 | C. | 0.30 mol•L-1 | D. | 0.45 mol•L-1 |
 2016年11月3日20点43分,中国首枚重型运载火箭“长征五号”在海南文昌航天发射场顺利点火升空.
2016年11月3日20点43分,中国首枚重型运载火箭“长征五号”在海南文昌航天发射场顺利点火升空.