19.下列有关化学用语表示正确的是( )
| A. | Na2O的电子式: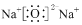 | B. | F-的结构示意图: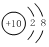 | ||
| C. | 中子数为20的Ar原子:${\;}_{18}^{20}$Al | D. | 苯甲酸的结构简式: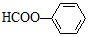 |
16.下列有关有机化合物的说法正确的是( )
| A. | CH2=CHCH3分子中所有原子在一个平面上 | |
| B. | 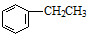 的同分异构体中,苯环上的一氯代物只有一种的结构有4种 的同分异构体中,苯环上的一氯代物只有一种的结构有4种 | |
| C. | CH2=CHCH2OH能发生加成发应、取代反应、氧化反应等 | |
| D. | 苯乙烯(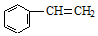 )能使溴水褪色,1mol苯乙烯与溴水反应时最多消耗4mol Br2 )能使溴水褪色,1mol苯乙烯与溴水反应时最多消耗4mol Br2 |
15.设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
| A. | 在标准状况下,22.4 L C2H6中含共价键的数目为6 NA | |
| B. | 5 g KHCO3与CaCO3混合固体中阴离子数目为0.05 NA | |
| C. | 常温下,1 L 0.1 mol•L-1CH3COONa溶液中CH3COO-离子数目为0.1 NA | |
| D. | 在Na2O2与H2O的反应中,当转移0.2 NA个电子时生成的O2体积为2.24 L |
14.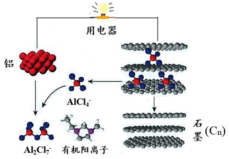 近期,科学家成功研制出一种可在一分钟内完成充放电的超常性能铝离子电池.该电池内部的A1Cl4-和有机阳离子构成电解质溶液,其放电工作原理如图所示.下列说法不正确的是( )
近期,科学家成功研制出一种可在一分钟内完成充放电的超常性能铝离子电池.该电池内部的A1Cl4-和有机阳离子构成电解质溶液,其放电工作原理如图所示.下列说法不正确的是( )
 近期,科学家成功研制出一种可在一分钟内完成充放电的超常性能铝离子电池.该电池内部的A1Cl4-和有机阳离子构成电解质溶液,其放电工作原理如图所示.下列说法不正确的是( )
近期,科学家成功研制出一种可在一分钟内完成充放电的超常性能铝离子电池.该电池内部的A1Cl4-和有机阳离子构成电解质溶液,其放电工作原理如图所示.下列说法不正确的是( )| A. | 放电时,铝为负极、石墨为正极 | |
| B. | 充电时,A1Cl4-向石墨电极移动 | |
| C. | 放电时,负极的电极反应式为A1十7A1Cl4--3e-=4 A12Cl7- | |
| D. | 充电时,电子从石墨电极直接经导线流入铝电极,然后再经电解质溶液流回石墨电极 |
13.wg铁粉和铝粉的混合物和过量的NaOH反应,然后过滤,将沉淀完全收集后,放蒸发皿中加热,直至被加热的物质质量不再变化.取出蒸发皿中的物质称量仍为wg.求原混合物中铝粉的质量分数是( )
| A. | 27.6% | B. | 30% | C. | 47% | D. | 78% |
12.对于密闭容器中进行的可逆反应:2SO2(g)+O2(g) $?_{加热}^{催化剂}$2SO3(g),下列能判断该反应已经达到化学平衡状态的是( )
| A. | SO2、O2、SO3的浓度相等 | B. | SO2、O2、SO3的浓度不再发生变化 | ||
| C. | SO2、O2、SO3在密闭容器中共存 | D. | 反应停止,正、逆反应速率都等于零 |
11.常温下,在由水电离产生的H+浓度为1×10?13mol/L 的溶液中,一定能大量共存的离子组是( )
0 161358 161366 161372 161376 161382 161384 161388 161394 161396 161402 161408 161412 161414 161418 161424 161426 161432 161436 161438 161442 161444 161448 161450 161452 161453 161454 161456 161457 161458 161460 161462 161466 161468 161472 161474 161478 161484 161486 161492 161496 161498 161502 161508 161514 161516 161522 161526 161528 161534 161538 161544 161552 203614
| A. | K+、Cl-、NO3-、Fe2+ | B. | K+、Mg2+、I-、SO42- | ||
| C. | K+、Ca2+、Cl-、HCO3- | D. | Na+、Cl-、NO3-、S042- |
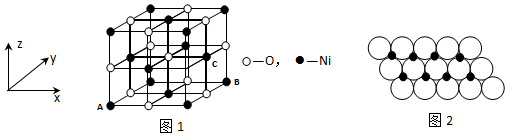
 ,Ni与CO能形成配合物Ni(CO)4,该分子中σ键与π键个数比为1:1.
,Ni与CO能形成配合物Ni(CO)4,该分子中σ键与π键个数比为1:1.