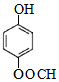
9.在四支试管中分别加入少量不同的无色无味溶液进行如下操作,结论正确的是( )
| 操作 | 现象 | 结论 | |
| A | 先加硝酸,再滴加BaCl2溶液 | 产生白色沉淀 | 原溶液中一定有SO42- |
| B | 先加入H2O2溶液,再加KSCN溶液 | 溶液呈血红色 | 原溶液中一定有Fe2+ |
| C | 用洁净铂丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中一定有Na+、无K+ |
| D | 滴加NaOH溶液,加热,将湿润红色石蕊试纸置于试管口 | 试纸变蓝 | 原溶液中一定有NH4+ |
| A. | A | B. | B | C. | C | D. | D |
8.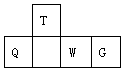 短周期元素T、Q、W、G在元素周期表中的相对位置如图所示,其中Q是无机非金属材料的主角.下列判断正确的是( )
短周期元素T、Q、W、G在元素周期表中的相对位置如图所示,其中Q是无机非金属材料的主角.下列判断正确的是( )
 短周期元素T、Q、W、G在元素周期表中的相对位置如图所示,其中Q是无机非金属材料的主角.下列判断正确的是( )
短周期元素T、Q、W、G在元素周期表中的相对位置如图所示,其中Q是无机非金属材料的主角.下列判断正确的是( )| A. | 原子半径:W<T | |
| B. | 最简单气态氢化物的热稳定性:Q<T | |
| C. | 最高价氧化物对应水化物的酸性:W<Q | |
| D. | 简单离子的还原性:W<G |
7.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 常温常压下,8g O2含有4NA个电子 | |
| B. | 1L 0.1mol•L-1的氨水中有0.1NA个NH4+ | |
| C. | 标准状况下,22.4L盐酸含有NA个HCl分子 | |
| D. | 1 mol苯乙烯中含碳碳双键数为4NA |
6.下列有关化学用语表示正确的是( )
| A. | CO2的电子式: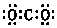 | B. | 中子数为21的钾原子:${\;}_{19}^{40}$K | ||
| C. | 甲烷分子的球棍模型: | D. | 氯离子的结构示意图: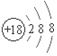 |
4.下列指定反应的化学方程式或离子方程式书写正确的是( )
| A. | 乙醇和浓硫酸混合加热至140℃,CH3CH2OH$→_{140℃}^{浓硫酸}$CH2=CH2↑+H2O | |
| B. | 1-溴丙烷与氢氧化钠的乙醇溶液供热:CH3CH2CH2Br+NaOH$→_{△}^{乙醇}$CH3CH2CH2OH+NaBr | |
| C. | 苯酚钠溶液中通入少量的CO2:2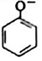 +H2O+CO2→2 +H2O+CO2→2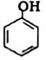 +CO${\;}_{3}^{2-}$ +CO${\;}_{3}^{2-}$ | |
| D. | 乙醛在碱性条件下被新制的氧化铜氧化:CH3CHO+2Cu(OH)2+OH-$\stackrel{△}{→}$CH3COO-+CuO↓+3H2O |
3.下列有关化学用语表示正确的是( )
| A. | 乙烯的比例模型: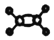 | B. | 四氯化碳的电子式: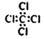 | ||
| C. | 苯酚的结构式: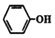 | D. | 乙醛的结构式:CH3CHO |
2.下列说法正确的是( )
| A. | 酶属于碳水化合物,是生物体中重要的催化剂 | |
| B. | 纤维素为天然高分子化合物,遇碘水会变蓝色 | |
| C. | 某些卤代烃能破坏臭氧层,使卤代烃的使用受到限制 | |
| D. | 某有机物的1H核磁共振谱图中特征峰的数目就是氢原子数 |
1.X、Y、Z、W 为四种短周期主族元素,且原子序数依次增大.已知X原子的最外层电子数是其电子层数的2倍,Y是地壳中含量最高的元素,Y原子的最层电子数是W原子最外层电子数的2倍,Z原子的最外层上只有一个电子.下列说法正确的是( )
| A. | 原子半径:r(Z)>r(W)>r(X)>r(Y) | |
| B. | Y与Z 两种元素只能形成一种化合物 | |
| C. | 最高价氧化物对应水化物的碱性:Z<W | |
| D. | X的简单气态氢化物的热稳定性比Y的强 |
20.在给定条件下,下列选项中所示的物质间转化都能一步实现的是( )
0 161357 161365 161371 161375 161381 161383 161387 161393 161395 161401 161407 161411 161413 161417 161423 161425 161431 161435 161437 161441 161443 161447 161449 161451 161452 161453 161455 161456 161457 161459 161461 161465 161467 161471 161473 161477 161483 161485 161491 161495 161497 161501 161507 161513 161515 161521 161525 161527 161533 161537 161543 161551 203614
| A. | Na$→_{点燃}^{O_{2}}$Na2O2$→_{点燃}^{CO_{2}}$Na2CO3 | |
| B. | Fe$→_{点燃}^{O_{2}}$Fe2O3$\stackrel{H_{2}SO_{4}}{→}$Fe2(SO4)3 | |
| C. | Al2O3$\stackrel{H_{2}O}{→}$Al(OH)3$\stackrel{盐酸}{→}$AlCl3 | |
| D. | S$→_{点燃}^{O_{2}}$SO3$\stackrel{H_{2}O}{→}$H2SO4 |
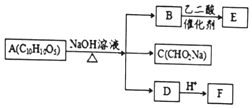 某芳香化合物A有如下转化:
某芳香化合物A有如下转化: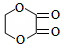 1mol F 最多消耗2mol NaOH.
1mol F 最多消耗2mol NaOH.